Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

a) Xét mC : mH : mO = 64,865% : 13,51% : 21,625%
=> nC : nH : nO = \(\dfrac{64,865}{12}:\dfrac{13,51}{1}:\dfrac{21,625}{16}=4:10:1\)
=> CTPT: (C4H10O)n hay C4nH10nOn ( n thuộc N*)
Xét độ bất bão hòa \(=\dfrac{2.4n+2-10n}{2}=\dfrac{2-2n}{2}=1-n\ge0\)
=> n = 1
Vậy CTPT: C4H10O
CTCT:
(1) \(CH_3-CH_2-CH_2-CH_2OH\)
(2) \(CH_3-CH_2-CH\left(OH\right)-CH_3\)
(3) \(CH_3-CH\left(CH_3\right)-CH_2OH\)
(4) \(CH_3-C\left(OH\right)\left(CH_3\right)-CH_3\)
(5) \(CH_3-CH_2-CH_2-O-CH_3\)
(6) \(CH_3-CH\left(CH_3\right)-O-CH_3\)
(7) \(CH_3-CH_2-O-CH_2-CH_3\)
b) Xét mC : mH : mN = 61,017% : 15,254% : 23,729%
=> \(n_C:n_H:n_N=\dfrac{61,017}{12}:\dfrac{15,254}{1}:\dfrac{23,729}{14}=3:9:1\)
=> CTPT: (C3H9N)n hay C3nH9nNn ( n thuộc N*)
Xét độ bất bão hòa \(\dfrac{2.3n+2-9n+n}{2}=1-n\)
=> n = 1
=> CTPT: C3H9N
CTCT:
(1) \(CH_3-CH_2-CH_2-NH_2\)
(2) \(CH_3-CH\left(NH_2\right)-CH_3\)
(3) \(CH_3-CH_2-NH-CH_3\)
(4) \(\left(CH_3\right)N\)
a)
\(CTTQ:C_aH_bO_z\left(a,b,z:nguyên,dương\right)\\ Ta.có:a:b:z=\dfrac{64,865\%}{12}:\dfrac{13,51\%}{1}:\dfrac{100\%-\left(64,865\%+13,51\%\right)}{16}\\ =0,054:0,1351:0,0135=4:10:1\\ \Rightarrow a=4;b=10;z=1\\ \Rightarrow CTPT:C_4H_{10}O\\ CTCT:CH_3-CH_2-CH_2-CH_2-OH\left(1\right)\\ CH_3-CH\left(CH_3\right)-CH_2-OH\left(2\right)\\ CH_3-CH_2-CH\left(CH_3\right)-OH\left(3\right)\\ CH_3-C\left(OH\right)-CH\left(CH_3\right)-CH_3\left(4\right)\\ CH_3-CH_2-CH_2-O-CH_3\left(5\right)\\ CH_3-CH\left(CH_3\right)-O-CH_3\left(6\right)\\ CH_3-CH_2-O-CH_2-CH_3\left(7\right)\)
Gọi tên:
(1) Ancol butylic
(2) 2 - metylpropan - 1 - ol
(3) Butan - 2 - ol
(4) 2 - metylpropan - 2 - ol
(5) metylpropyl ete
(6) Isopropylmetyl ete
(7) Đietyl ete

Ba chất đồng phân có công thức phân tử giống nhau. Đốt X ta chỉ được C O 2 và H 2 O , vậy các chất trong X có chứa C, H và có thể có chứa O.
Theo định luật bảo toàn khối lượng :
m C O 2 + m H 2 O = m X + m O 2 = 5,1(g)
Mặt khác mCO2: mH2O = 11:6
Từ đó tìm được: m C O 2 = 3,30 g và m H 2 O = 1,80 g
Khối lượng C trong 3,30 g
C
O
2
: 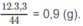
Khối lương H trong 1,80 g
H
2
O
: 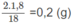
Khối lượng O trong 1,50 g X : 1,50 - 0,9 - 0,2 = 0,4 (g).
Các chất trong X có dạng C x H y O z
x : y : z = 0,075 : 0,2 : 0,025 = 3 : 8 : 1.
Công thức đơn giản nhất là C 3 H 8 O .
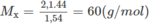
⇒ CTPT cũng là C 3 H 8 O .
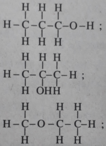
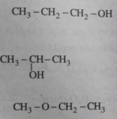

1. Trong dãy đồng đẳng của benzen, chỉ có C 6 H 6 và C 7 H 8 là không có đồng phân là hợp chất thơm.
A và B ở trong dãy đó và MA < MB vậy A là C 6 H 6 và B là C 7 H 8 .
Chất C cách chất A hai chất trong dãy đồng đẳng nghĩa là chất C phải hơn chất A ba nguyên tử cacbon. Công thức phân tử chất C là C 9 H 12 .
2. Giả sử trong 48,8 g hỗn hợp X có a mol A, b mol B và c mol C; ta có :
78a + 92b + 120c = 48,8 (1)
a = c (2)
C 6 H 6 + 7,5 O 2 → 6 C O 2 + 3 H 2 O
a 7.5a
C 7 H 8 + 9 O 2 → 7 C O 2 + 4 H 2 O
b 9b
C 9 H 12 + 12 O 2 → 9 C O 2 + 6 H 2 O
c 12c
7,5a + 9b + 12c 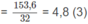
Giải hệ (1), (2), (3), tìm được a = c = 0,2 ; b = 0,1.
Từ đó tính được thành phần phần phần trăm về khối lượng của hỗn hợp X :
C 6 H 6 : 31,9%; C 7 H 8 : 18,9%; C 9 H 12 : 49,2%

Đáp án D
mC : mH : mO : mN = 40,449 : 7,865 : 35,956 : 15,73
=> nC : nH : nO : nN = 3,37 : 7,865 : 2,25 : 1,12 = 3 : 7 : 2 : 1
=> C3H7O2N
X + NaOH tạo muối
Có : nX = nmuối = 0,05 mol
=> Mmuối = 97g => NH2CH2COONa

Giải thích: Đáp án B
Công thức phân tử C3H7O2N (M = 87) → nX = 0,05 mol
→ muối có dạng RCOONa → Mmuoi = R + 67 = 97 → R = 30 (H2N−CH2− )

1. CTĐGN là C 7 H 8 O
2. CTPT là C 7 H 8 O
3. Có 5 CTCT phù hợp :
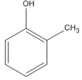 (2-metylphenol (A1))
(2-metylphenol (A1))
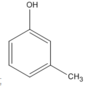 (3-metylphenol (A2))
(3-metylphenol (A2))
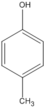 (4-metylphenol (A3))
(4-metylphenol (A3))
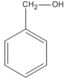 (ancol benzylic (A4))
(ancol benzylic (A4))
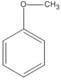 ( metyl phenyl ete (A5))
( metyl phenyl ete (A5))
4. Có phản ứng với Na: A1, A2, A3, A4;
Có phản ứng với dung dịch NaOH: A1, A2, A3.

Số mol ankin trong mỗi phần 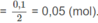
Khi đốt cháy hoàn toàn phần (1):
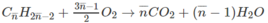
Cứ 1 mol C n H 2 n - 2 tạo ra ( n −1) mol H 2 O
Cứ 0,5. 10 - 1 mol C n H 2 n - 2 tạo ra 0,13 mol H 2 O
Như vậy trong hỗn hợp A phải có ankin có số nguyên tử cacbon nhỏ hơn 3,6 tức là phải có C 2 H 2 hoặc C 3 H 4 .
Nếu có C 2 H 2 thì số mol chất này ở phần 2 là:
n = 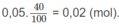
Khi chất này tác dụng với dung dịch A g N O 3 trong N H 3 :
C 2 H 2 + 2 A g N O 3 + 2 N H 3 → C 2 A g 2 ↓ + 2 N H 4 N O 3
0,02 mol 0,02 mol
Khối lượng 0,02 mol C 2 A g 2 là: 0,02. 240 = 4,8 (g) > 4,55 g.
Vậy hỗn hợp A không thể có C 2 H 2 mà phải có C 3 H 4 .
Khi chất này tác dụng với dung dịch A g N O 3 trong N H 3 :
C 3 H 4 + A g N O 3 + N H 3 → C 3 H 3 A g ↓ + N H 4 N O 3
0,02 mol 0,02 mol 0,02 mol
Khối lượng C 3 H 3 A g là 0,02.147 = 2,94 (g).
Số mol A g N O 3 đã phản ứng với các ankin là: 0,25.0,12 = 0,03 (mol): trong đó lượng A g N O 3 tác dụng với C 3 H 4 là 0,02 mol, vậy lượng A g N O 3 tác dụng với ankin khác là 0,01 mol.
Trong phần 2, ngoài 0,02 mol C 3 H 4 còn 0,03 mol 2 ankin khác. Vậy mà lượng A g N O 3 phản ứng chỉ là 0,01 mol, do đó trong 2 ankin còn lại, chỉ có 1 chất có phản ứng với A g N O 3 , 1 chất không có phản ứng:
C n H 2 n - 2 + A g N O 3 + N H 3 → C n H 2 n - 3 A g ↓ + N H 4 N O 3
0,01 mol 0,01 mol 0,01 mol
Khối lượng 0,010 mol C n H 2 n - 3 A g là: 4,55 - 2,94 = 1,61(g).
Khối lượng 1 mol C n H 2 n - 3 A g là 161 g.
14n + 105 = 161 ⇒ n = 4.
Công thức phân tử là C 4 H 6 và CTCT: C H 3 - C H 2 - C ≡ C H (but-1-in)
Đặt công thức chất ankin chưa biết là C n ' H 2 n ' - 2 :
C 3 H 4 + 4 O 2 → 3 C O 2 + 2 H 2 O
0,02 mol 0,04 mol
C 4 H 6 + 5,5 O 2 → 4 C O 2 + 3 H 2 O
0,01 mol 0,03 mol
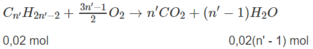
Tổng số mol H 2 O : 0,04 + 0,03 + 0,02(n' - 1) = 0,13 ⇒ n' = 4.
Chất ankin thứ ba có CTPT C 4 H 6 nhưng không tác dụng với A g N O 3 nên CTCT là C H 3 - C ≡ C - C H 3 (but-2-in).
Thành phần về khối lượng:
Propin chiếm: 33,1%; but-1-in : 22,3%; but-2-in: 44,6%.

a) Ta có:
%O = 100% - %C - %H = 100% - 66,67% - 11,11% = 22,22%
⇒ MX = 2,25.32 = 72
Gọi công thức phân tử của X là CxHyOz
Ta có tỉ số:
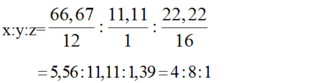
⇒ Công thức đơn giản nhất của X là C4H8O
Gọi công thức phân tử của X là (C4H8O)n
⇒ MX = (4.12 + 8 + 16)n = 72n = 72 ⇒ n = 1
⇒ Công thức phân tử của X là C4H8O
b) X không tác dụng được với dung dịch AgNO3 trong NH3, khi tác dụng với hiđro sinh ra X1, X1 tác dụng natri giải phóng hiđro ⇒ X là xeton
CTCT và tên gọi của X là:
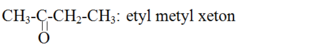
Tham khảo:
Đặt công thức phân tử của X là CxHyFz.
Ta có: x : y : z =\(\dfrac{\%C}{12}\) :\(\dfrac{\%H}{1}\): \(\dfrac{\%F}{19}\) = \(\dfrac{23.08}{12}\) :\(\dfrac{3.84}{1}\) :\(\dfrac{73.08}{19}\) = 1,923 : 3,84 : 3,84 = 1 : 2 : 2.
=> Công thức đơn giản nhất của X là: CH2F2. => CxHyOz = (CH2F2)n. Lại có phân tử khối của X là 52 => (12.1 + 1.2 + 19).n = 52 Þ n = 1.
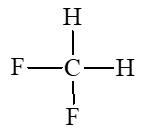
Vậy X là CH2F2, có công thức cấu tạo:
Gọi công thức phân tử của X là \(C_xH_yF_t\)
Theo đề, ta có: \(x:y:t=\dfrac{23.08}{12}:\dfrac{3.84}{1}:\dfrac{73.08}{19}\)
=>x:y:t=1:2:2
=>Công thức đơn giản nhất sẽ là \(CH_2F_2\)
=>Công thức phân tử của X sẽ có dạng là: \(\left(CH_2F_2\right)_x\)
Theo đề, ta có: x(1*12+2*2+2*19)=52
=>x=1
=>X là \(CH_2F_2\)
Công thức cấu tạo là: