Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Giải thích: Đáp án C
3 chất đều phản ứng cộng với Br2 và có không quá 3 C
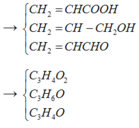
X + NaOH chỉ có 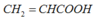 phản ứng →
phản ứng → ![]() = 0,02 mol
= 0,02 mol
Xét 0,1 mol hỗn hợp có
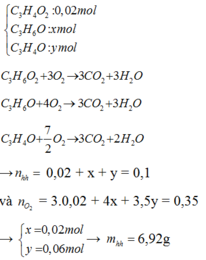
Trong 17,3g hỗn hợp lượng chất gấp 2,5 lần so với 6,92 gam hỗn hợp
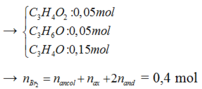

Đáp án D
chú ý: gọi k là số π trong X thì ∑nCO2 – ∑nH2O = (k – 1)nX
→ nπ trong X – nX = ∑nCO2 – ∑nH2O (phân biệt số mol π và số π nhé.!).
đặt x = ngốc –COO trong X thì ∑nO trong X = 2x mol và nπCO trong X = x mol.
Bảo toàn O phương trình đốt cháy có ∑nCO2 = 0,87 + x mol.
Theo đó nπ trong X = 0,4 + x mol. Thật chú ý: π trong X gồm πC=C phản ứng được với Br2
(1πC=C + 1Br) và πCO (trong COO không phản ứng được với Br2).
→ Rõ luôn số mol Br2 phản ứng với 0,33 mol X là 0,4 mol. Chọn đáp án D

Đáp án B
Hướng dẫn
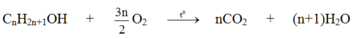
CT của M là: CnH2n+2Oa ; nCO2 = 35,2/44 = 0,8 mol ;
nH2O = 19,8/18 = 1,1 mol
=> nCO2(M) = 0,8 – 0,2 = 0,6 mol => n = 3.
X tác dụng Na thu được 0,3 mol H2 => M là ancol 2 chức
=> C3H8O2



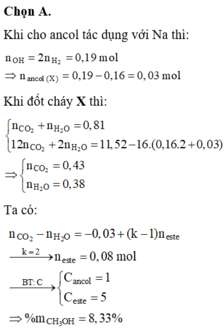
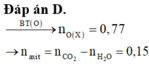
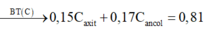
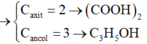
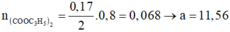
Ancol đơn chức có dạng ROH
Cho m gam X tác dụng với Na dư.
\(2ROH+2Na\rightarrow2RONa+H_2\)
\(C_2H_4\left(OH\right)_2+2Na\rightarrow C_2H_4\left(ONa\right)_2+H_2\)
Ta có:
\(2n_{H2}=n_{ROH}+2n_{C2H4\left(OH\right)2}=n_{ROH}+0,1.2=0,43\)
\(\Rightarrow n_{ROH}=0,23\left(mol\right)\)
Vì etylen glycol no mà X tác dụng vừa đủ 0,26 mol brom nên ROH không no.
\(\frac{n_{Br2}}{n_{KOH}}=\frac{0,26}{0,23}=1,13\) lẻ( tỉ số này phải là số nguyên)
Mình viết lại hợp chất + với phương pháp bơm khí 0,26 mol H2 vào như sau:
\(\left\{{}\begin{matrix}O:0,1mol\\H2O:0,215.2-0,1=0,33mol\\CH2:\dfrac{1,125.2+0,26+0,1}{3}=0,87mol\end{matrix}\right.\)
Từ đó ➜m=14.0,87 + 0,33.18 + 0,1.16 - 0,26.2 = 19,2 ( gam )