Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án B
Tính số mol các khí trong B:
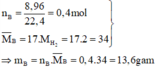
Đặt số mol các khí trong B là NO : a mol ; NO2 : b mol
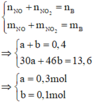
Số mol của M là: n M = 32 M m o l
Gọi n là hóa trị của M
Sơ đồ phản ứng:


Kim loại M có hóa trị n (n= 1,2,3)
nN2O = 6,72/22,4 = 0,3 mol => ne nhận = 0,3.8 = 2,4 mol
Áp dụng định luật bảo toàn electron => ne kim loại M nhường = 2,4 mol
Quá trình oxi hóa Quá trình khử
M → M+n + ne 2N+5 + 8e → N+12
\(\dfrac{2,4}{n}\) <----- 2,4 2,4<---- 0,3
=> nM = 2,4/n và phân tử khối M = \(21,6:\dfrac{2,4}{n}\) = 9n
=> n =3 và MM = 27 , kim loại M là nhôm (Al)

Hòa tan hoàn toàn 15,2 gam hỗn hợp gồm Fe và Cu trong dung dịch HNO3, thu được dung dịch X và 4,48 lút khí NO. Cho 3,96 gam kim loại Mg vào X đến khi phản ứng xảy ra hoàn toàn, thu được 224ml khí NO và m gam chất rắn không tan. biết NO là sản phẩm khử duy nhất của N+5. Gía trị cảu m là
A. 6,4 B.12,8 C.9,6 D.4,8

a)\(\left\{{}\begin{matrix}n_{Cu}=x\left(mol\right)\\n_{Al}=y\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}64x+27y=9,1\\BTe:2x+3y=0,5\cdot1\end{matrix}\right.\Rightarrow\left\{{}\begin{matrix}x=0,1\\y=0,1\end{matrix}\right.\)
\(\%m_{Cu}=\dfrac{0,1\cdot64}{9,1}\cdot100\%=70,33\%\)
\(\%m_{Al}=100-70,33\%=29,67\%\)
b)\(\left\{{}\begin{matrix}n_{NO_2}+n_{NO}=0,5\\\dfrac{n_{NO_2}}{n_{NO}}=\dfrac{2}{1}\end{matrix}\right.\Rightarrow\left\{{}\begin{matrix}n_{NO_2}=\dfrac{1}{3}\\n_{NO}=\dfrac{1}{6}\end{matrix}\right.\)
Gọi \(\left\{{}\begin{matrix}n_{Cu}=a\left(mol\right)\\n_{Al}=b\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}64a+27b=9,1\\BTe:2x+3y=\dfrac{1}{3}\cdot1+\dfrac{1}{6}\cdot3\end{matrix}\right.\Rightarrow\left\{{}\begin{matrix}a=\dfrac{4}{115}\\b=\dfrac{527}{2070}\end{matrix}\right.\)
\(\%m_{Cu}=\dfrac{\dfrac{4}{115}\cdot64}{9,1}\cdot100\%=24,46\%\)
\(\%m_{Al}=100\%-24,46\%=75,54\%\)
\(n_{HNO_3}=2n_{NO_2}+4n_{NO}=2\cdot\dfrac{1}{3}+4\cdot\dfrac{1}{6}=\dfrac{4}{3}mol\)
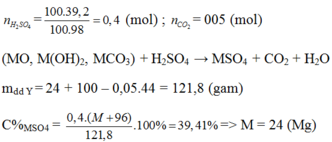

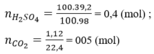

Ta có: \(\left\{{}\begin{matrix}n_{NO}+n_{N_2}=\dfrac{5,6}{22,4}\\30n_{NO}+28n_{N_2}=7,2\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}n_{NO}=0,1\left(mol\right)\\n_{N_2}=0,15\left(mol\right)\end{matrix}\right.\)
Giả sử M có số oxi hóa n.
BT e, có: n.nM = 3nNO + 10nN2
\(\Rightarrow n_M=\dfrac{1,8}{n}\left(mol\right)\)
\(\Rightarrow M_M=\dfrac{21,6}{\dfrac{1,8}{n}}=12n\left(g/mol\right)\)
Với n = 2 thì MM = 24 (g/mol) là thỏa mãn.
Vậy: M là Mg.