Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Chọn C
Gọi số mol của Fe và Al lần lượt là x và y mol

Muối trong dung dịch A gồm x mol F e S O 4 và 0,5y mol A l 2 ( S O 4 ) 3


Phản ứng nhiệt nhôm:
2 A l + F e 2 O 3 → t 0 A l 2 O 3 + 2 F e ( 1 )
Phần 1 tác dụng với dung dịch NaOH dư không sinh ra khí → hỗn hợp B không có Al dư. Vậy hỗn hợp B gồm A l 2 O 3 , Fe và có thể có F e 2 O 3 dư.
4,4 gam chất rắn không tan có thể gồm Fe và F e 2 O 3 d ư
Phần 2: tác dụng với H 2 S O 4 loãng dư → chỉ có Fe phản ứng sinh ra khí
n H 2 = 1,12 22,4 = 0,05
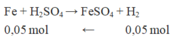
Khối lượng F e 2 O 3 dư ở phần 2 = 4,4 – mFe = 4,4 – 0,05.56 = 1,6 gam.
n F e 2 O 3 p u b d đ = 2. 1 2 . n F e ( p 2 ) = 0,05 m o l
Khối lượng F e 2 O 3 ban đầu: 0,05.160 + 1,6.2 = 11,2 gam.
⇒ Chọn B.





BTKL
mX + mdd HNO3 = mdd X + mH2O + m↑
=> mdd X = 11,6 + 87,5 – 30 . 0,1 – 46 . 0,15 = 89,2g
=> C%Fe(NO3)3 = 13,565%
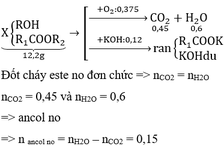


Theo de bai ta co : \(\left\{{}\begin{matrix}nAl=\dfrac{12,42}{27}=0,46\left(mol\right)\\nY=\dfrac{1,344}{22,4}=0,06\left(mol\right)\end{matrix}\right.\)
Goi x ,y lan luot la so mol cua N2O va N2
Ta co PTHH :
(1) \(8Al+30HNO3->8Al\left(NO3\right)3+3N2O\uparrow+15H2O\)
8/3x mol........................8/3x mol.................xmol
\(\left(2\right)10Al+36HNO3->10Al\left(NO3\right)3+3N2\uparrow+18H2O\)
10/3ymol..............................10/3ymol..............ymol
Ta co : x + y = 0,06
Ta co :
\(M_Y=18.2=36\left(\dfrac{g}{mol}\right)\)
Ta co so do duong cheo :
=> y = x
=> 2x = 0,06 => x = 0,03 (mol) ; y = 0,03 mol
Theo 2 PTHH ta co :
\(nAl=nAl\left(NO3\right)3=\dfrac{8}{3}x+\dfrac{10}{3}y=0,18\left(mol\right)\)
Vi nAl(ban dau) = 0,46
=> nAl(du) = 0,46 - 0,18 = 0,28 (mol)
=> Al du tiep tuc phan ung voi HNO3 du
Ta co PTHH 3 :
\(8Al+30HNO3->8Al\left(NO3\right)3+3NH4NO3+9H2O\)
0,28mol.......................0,28mol...............0,105mol
=> DD X thu duoc bao gom Al(NO3)3 va NH4NO3
=> Chat ran thu duoc sau khi co can la : Al(NO3)3 va NH4NO3
Ta co :
\(m\left(chat-ran\right)=mAl\left(NO3\right)3+mNH4NO3=\left(0,18+0,28\right).213+0,105.80=106,38\left(g\right)\)
Vi chua duoc hoc cach can bang Electron nen hoi dai =="
Hòa tan hoàn toàn 12,42 gam Al bằng dung dịch HNO 3 loãng (dư), thu được dung dịch X và 1,344 lít (ở đktc) hỗn hợp khí Y gồm hai khí là N 2 O và N 2 . Tỉ khối của hỗn hợp khí Y so với khí H 2 là 18. Cô cạn dung dịch X, thu được m gam chất rắn khan. tính giá trị của m.
Bài làm
nAl=0.46=>necho=1.38
dùng đường chéo=>nenhận=0.03(10+8)=0.54
=>necho>nenhận
=>có NH4NO3 và nNH4NO3=(1.38-0.54)/8=0.105
=>h2 muối sau p/ư bao gồm Al(NO3)3 và NH4NO3
m=0.46(213)+0.105(80)=106.38