Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

a, PT: \(Zn+2HCl\rightarrow ZnCl_2+H_2\)
\(2Al+6HCl\rightarrow2AlCl_3+3H_2\)
Gọi: \(\left\{{}\begin{matrix}n_{Zn}=x\left(mol\right)\\n_{Al}=y\left(mol\right)\end{matrix}\right.\) ⇒ 65x + 27y = 17,05 (1)
Ta có: \(n_{H_2}=\dfrac{9,52}{22,4}=0,425\left(mol\right)\)
Theo PT: \(n_{H_2}=n_{Zn}+\dfrac{3}{2}n_{Al}=x+\dfrac{3}{2}y=0,425\left(2\right)\)
Từ (1) và (2) \(\Rightarrow\left\{{}\begin{matrix}n_{Zn}=0,2\left(mol\right)\\n_{Al}=0,15\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}m_{Zn}=0,2.65=13\left(g\right)\\m_{Al}=0,15.27=4,05\left(g\right)\end{matrix}\right.\)
b, Theo PT: \(\left\{{}\begin{matrix}n_{ZnCl_2}=n_{Zn}=0,2\left(mol\right)\\n_{AlCl_3}=n_{Al}=0,15\left(mol\right)\end{matrix}\right.\) \(\Rightarrow\left\{{}\begin{matrix}C_{M_{ZnCl_2}}=\dfrac{0,2}{0,5}=0,4\left(M\right)\\C_{M_{AlCl_3}}=\dfrac{0,15}{0,5}=0,3\left(M\right)\end{matrix}\right.\)
c, Ta có: m dd HCl = 1,05.500 = 525 (g)
m dd sau pư = mhh + m dd HCl - mH2 = 541,2 (g)
\(\Rightarrow\left\{{}\begin{matrix}C\%_{ZnCl_2}=\dfrac{0,2.136}{541,2}.100\%\approx5,03\%\\C\%_{AlCl_3}=\dfrac{0,15.133,5}{541,2}.100\%\approx3,7\%\end{matrix}\right.\)

Gọi \(\left\{{}\begin{matrix}n_{Al}=x\left(mol\right)\\n_{Fe}=y\left(mol\right)\end{matrix}\right.\)
\(n_{H_2}=\dfrac{4,48}{22,4}=0,2mol\)
\(2Al+6HCl\rightarrow2AlCl_3+3H_2\)
\(Fe+2HCl\rightarrow FeCl_2+H_2\)
Theo pt: \(\Rightarrow\left\{{}\begin{matrix}3x+y=0,2\\27x+56y=5,5\end{matrix}\right.\Rightarrow\left\{{}\begin{matrix}x=\dfrac{19}{470}\\y=\dfrac{37}{470}\end{matrix}\right.\)
\(\%m_{Al}=\dfrac{\dfrac{19}{470}\cdot27}{5,5}\cdot100\%=19,84\%\)
\(\%m_{Fe}=100\%-19,84\%=80,16\%\)

PTHH: \(Mg+2HCl\rightarrow MgCl_2+H_2\uparrow\)
\(MgO+2HCl\rightarrow MgCl_2+H_2O\)
a) Ta có: \(n_{H_2}=\dfrac{11,2}{22,4}=0,5\left(mol\right)=n_{Mg}\)
\(\Rightarrow\%m_{Mg}=\dfrac{0,5\cdot24}{16}=75\%\) \(\Rightarrow\%m_{MgO}=25\%\)
b) Ta có: \(\left\{{}\begin{matrix}n_{Mg}=0,5\left(mol\right)\\n_{MgO}=\dfrac{16\cdot25\%}{40}=0,1\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow n_{HCl}=2n_{Mg}+2n_{MgO}=1,2\left(mol\right)\) \(\Rightarrow m_{ddHCl}=\dfrac{1,2\cdot36,5}{20\%}=219\left(g\right)\)
c) Theo các PTHH: \(\left\{{}\begin{matrix}n_{H_2}=0,5\left(mol\right)\\n_{MgCl_2}=0,6\left(mol\right)\end{matrix}\right.\) \(\Rightarrow\left\{{}\begin{matrix}m_{H_2}=0,5\cdot2=1\left(g\right)\\m_{MgCl_2}=0,6\cdot95=57\left(g\right)\end{matrix}\right.\)
Mặt khác: \(m_{dd}=m_{hhA}+m_{ddHCl}-m_{H_2}=234\left(g\right)\) \(\Rightarrow C\%_{MgCl_2}=\dfrac{57}{234}\cdot100\%\approx24,36\%\)
Cho mình hỏi ở cái PTHH ấy! sao ta không tính số mol ở dưới??

a, mchất rắn = mCu = 12,8 (g)
=> mhh (Al, Zn) = 28,5 - 12,8 = 16,7 (g)
\(m_{H_2SO_4}=7,84\%.500=39,2\left(g\right)\\ n_{H_2SO_4}=\dfrac{39,2}{98}=0,4\left(mol\right)\)
Gọi \(\left\{{}\begin{matrix}n_{Al}=a\left(mol\right)\\n_{Zn}=b\left(mol\right)\end{matrix}\right.\left(a,b>0\right)\)
PTHH:
2Al + 3H2SO4 ---> Al2(SO4)3 + 3H2↑
a----->1,5a---------->0,5a-------->1,5a
Zn + H2SO4 ---> ZnSO4 + H2
b---->b------------>b--------->b
mdd (tăng) = mhh (Al, Zn) - mH2 = 27a + 65a - 2.(1,5a - b) = 24a - 63b = 515 - 500 = 15 (g)
=> Hệ pt \(\left\{{}\begin{matrix}27a+65b=15,7\\24a-63b=15\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}a=0,1\left(mol\right)\\b=0,2\left(mol\right)\end{matrix}\right.\left(TM\right)\)
\(\Rightarrow\left\{{}\begin{matrix}\%m_{Cu}=\dfrac{12,8}{28,5}.100\%=44,9\%\\\%m_{Al}=\dfrac{0,1.27}{28,5}.100\%=18,9\%\\\%m_{Zn}=100\%-44,9\%-18,9\%=36,2\%\end{matrix}\right.\)
b, \(n_{H_2SO_{4\left(dư\right)}}=0,4-0,1.1,5-0,2=0,05\left(mol\right)\)
\(\Rightarrow\left\{{}\begin{matrix}C\%_{Al_2\left(SO_4\right)_3}=\dfrac{0,05.342}{515}.100\%=3,32\%\\C\%_{ZnSO_4}=\dfrac{0,2.161}{515}.100\%=6,25\%\\C\%_{H_2SO_{4\left(dư\right)}}=\dfrac{0,05.98}{515}.100\%=0,95\%\end{matrix}\right.\)
anh ơi \(24a+63b=15\) mới đúng chứ anh:)
\(m_{dd\left(tăng\right)}=24a+63b\) nữa:)

Gọi số mol H2SO4 là a (mol)
Bảo toàn H: \(n_{H_2}=a\left(mol\right)\)
Có: \(m_{tăng}=m_{KL}-m_{H_2}\)
=> \(m_{KL}=48,6+2a\left(g\right)\)
Theo ĐLBTKL: \(m_{KL}+m_{H_2SO_4}=m_{Muối}+m_{H_2}\)
=> \(48,6+2a+98a=161,3+2a\)
=> a = 1,15 (mol)
=> \(a=\dfrac{1,15}{0,55}=\dfrac{23}{11}M\)

Giả sử có 1 mol khí ở 0oC, 2atm
Theo phương trình trạng thái khí lý tưởng:
\(P.V=n.R.T\)
=> \(V=\dfrac{n.R.T}{P}=\dfrac{1.0,082.273}{2}\approx11,2\left(l\right)\)
=> 1 mol khí chiếm thể tích 11,2 lít ở 0oC, 2atm nhé :)
\(n_{H_2}=\dfrac{P.V}{R.T}=\dfrac{2.6,72}{0,082.\left(0+273\right)}=0,6\left(mol\right)\\ n_{H_2SO_4}=n_{H_2}=n_{SO^{2-}_4}=0,6\left(mol\right)\\ \Rightarrow m_{muối}=m_{hhkimloai}+m_{SO^{2-}_4}=21+96.0,6=78,6\left(g\right)\\ V_{ddH_2SO_4}=\dfrac{0,6}{0,5}=1,2\left(l\right)\)
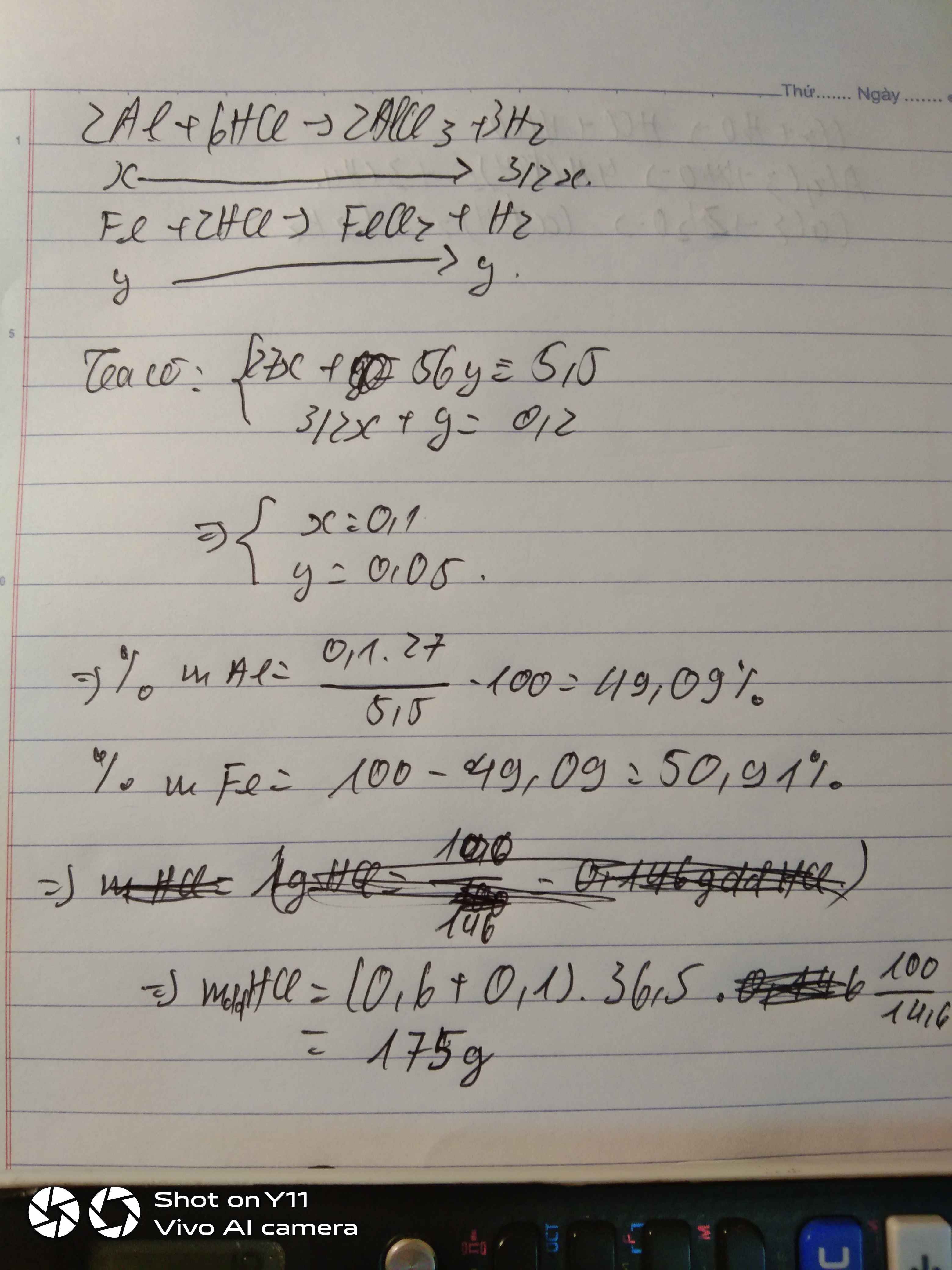

\(m_{HCl}=\dfrac{124,1\cdot25}{100}=31,025g\)
\(\Rightarrow n_{HCl}=0,85mol\)
\(2Al+6HCl\rightarrow2AlCl_3+3H_2\)
x 3x
\(Zn+2HCl\rightarrow ZnCl_2+H_2\)
y 2y
\(\Rightarrow\left\{{}\begin{matrix}27x+65y=17,05\\3x+2y=0,85\end{matrix}\right.\Rightarrow\left\{{}\begin{matrix}x=0,15\\y=0,2\end{matrix}\right.\)
\(\%m_{Zn}=\dfrac{0,2\cdot65}{17,05}\cdot100\%=75,25\%\)
76,2%