Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án B
Cho Al và Ag phản ứng với H 2 S O 4 loãng, dư chỉ có Al phản ứng.
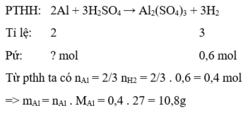
% m A l = 10,8 12 .100 % = 90 % .
% m A g = 100 % - 90 % = 10 %

\(n_{H_2}=\dfrac{13,44}{22,4}=0,6\left(mol\right)\)
PTHH: 2Al + 3H2SO4 --> Al2(SO4)3 + 3H2
_____0,4<-----------------------------------0,6
=> \(\%Al=\dfrac{0,4.27}{12}.100\%=90\%\)
%Ag = 100% - 90% = 10%

Theo bài ra, ta có: \(m_{Ag}=5,6\left(g\right)\)
PTHH: \(2Al+3H_2SO_4\rightarrow Al_2\left(SO_4\right)_3+3H_2\uparrow\)
a) Ta có: \(n_{H_2}=\dfrac{2,24}{22,4}=0,1\left(mol\right)\) \(\Rightarrow n_{Al}=\dfrac{1}{15}\left(mol\right)\) \(\Rightarrow m_{Al}=\dfrac{1}{15}\cdot27=1,8\left(g\right)\)
\(\Rightarrow\%m_{Al}=\dfrac{1,8}{1,8+5,6}\cdot100\%\approx24,32\%\) \(\Rightarrow\%m_{Ag}=75,68\%\)
b) Theo PTHH: \(n_{H_2SO_4}=n_{H_2}=0,1mol\) \(\Rightarrow C_{M_{H_2SO_4}}=\dfrac{0,1}{0,1}=1\left(M\right)\)
c) PTHH: \(H_2SO_4+Ba\left(OH\right)_2\rightarrow BaSO_4\downarrow+2H_2O\)
Theo PTHH: \(n_{Ba\left(OH\right)_2}=n_{H_2SO_4}=0,1mol\)
\(\Rightarrow V_{ddBa\left(OH\right)_2}=\dfrac{0,1}{0,2}=0,5\left(l\right)=500\left(ml\right)\)

Vì Ag không tác dụng với H2SO4 loãng
Pt : \(2Al+3H_2SO_4\rightarrow Al_2\left(SO_4\right)_3+3H_2|\)
2 3 1 3
0,3 0,45
\a) Chất rắn không tan là Ag nên :
\(m_{Ag}=5,4\left(g\right)\)
⇒ \(m_{Al}=13,5-5,4=8,1\left(g\right)\)
0/0Al = \(\dfrac{8,1.100}{13,5}=60\)0/0
0/0Ag = \(\dfrac{5,4.100}{13,5}=40\)0/0
b) Có : \(m_{Al}=8,1\left(g\right)\)
\(n_{Al}=\dfrac{8,1}{27}=0,3\left(mol\right)\)
\(n_{H2}=\dfrac{0,3.3}{2}=0,45\left(mol\right)\)
\(V_{H2\left(dktc\right)}=0,45.22,4=10,08\left(l\right)\)
Chúc bạn học tốt

\(n_{H2}=\dfrac{4,48}{22,4}=0,2\left(mol\right)\)
Pt : \(Zn+H_2SO_4\rightarrow ZnSO_4+H_2|\)
1 1 1 1
0,2 0,2
\(n_{Zn}=\dfrac{0,1.1}{1}=0,1\left(mol\right)\)
\(m_{Zn}=0,1.65=6,5\left(g\right)\)
\(m_{Ag}=15-6,5=8,5\left(g\right)\)
0/0Zn = \(\dfrac{6,5.100}{15}=43,33\)0/0
0/0Ag = \(\dfrac{8,5.100}{15}=56,67\)0/0
Chúc bạn học tốt

PTHH: \(Fe+H_2SO_4\rightarrow FeSO_4+H_2\uparrow\)
a) Ta có: \(n_{H_2}=\dfrac{5,6}{22,4}=0,25\left(mol\right)=n_{Fe}\)
\(\Rightarrow m_{Fe}=0,25\cdot56=14\left(g\right)\) \(\Rightarrow m_{Cu}=6\left(g\right)\)
b) Theo PTHH: \(n_{FeSO_4}=0,25mol\) \(\Rightarrow m_{FeSO_4}=0,25\cdot152=38\left(g\right)\)
Mặt khác: \(\left\{{}\begin{matrix}m_{ddH_2SO_4}=\dfrac{0,25\cdot98}{10\%}=245\left(g\right)\\m_{H_2}=0,25\cdot2=0,5\left(g\right)\end{matrix}\right.\)
\(\Rightarrow m_{dd}=m_{hh}+m_{H_2SO_4}-m_{Cu}-m_{H_2}=258,5\left(g\right)\)
\(\Rightarrow C\%_{FeSO_4}=\dfrac{38}{258,5}\cdot100\%\approx14,7\%\)
pthh : Fe +H2SO4 → FeSO4 +H2
theo bài ra số mol của h2 =0,15 (mol)
theo pt : nFe=nH2=0,15 (mol)
mFe=0,15 .56 =8,4 (g) ⇒mCu=20-8,4=11,6 (g)
