Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án : B
,nCO2 bđ = 0,4 mol
100 ml X + Ba(OH)2 -> nBaCO3 = nC(X) = 0,2 mol
=> Trong 400 ml X có 0,8 mol C => Bảo toàn C : nCO2 bđ + nK2CO3 = nC(X)
=> nK2CO3 = y = 0,4 mol
Giả sử trong 200 ml X có a mol K2CO3 và b mol KHCO3 ( a + b = 0,4 mol)
Cho từ từ X vào nHCl = 0,3 mol tạo nCO2 = 0,24 mol
=> K2CO3 và KHCO3 phản ứng đồng thời (vì HCl lúc đầu dư) theo tỉ lệ mol a : b
Gọi nK2CO3 pứ = ax và nKHCO3 pứ = bx
=> 2ax + bx = nHCl = 0,3 mol ; ax + bx = nCO2 = 0,24 mol
=> ax = 0,06 và bx = 0,18 mol
=> a : b = 1 : 3
=> a = 0,1 ; b = 0,3 mol
=> Bảo toàn K : x + 2y = 2.(2a + b)
=> x = 0,2 mol

Chọn đáp án A
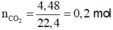
100 ml X + Ba(OH)2 dư → 0,2 mol BaCO3 ↓
![]()
100 ml X + HCl:
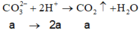
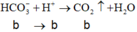
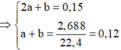
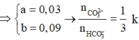
Trong 200 ml
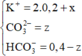
![]()
⇒ n C O 3 2 - = 0 , 1 m o l ; n H C O 3 - = 0 , 3 m o l
→ B T N T x = 0 , 1 . 2 + 0 , 3 - 0 , 2 . 2 = 0 , 1

Đáp án : C
Fe được hòa tan hoàn toàn bởi dd HNO3 thu được dd X, khi thêm HCl vào X có khí NO thoát ra → trong X có ion Fe2+ → HNO3 đã phản ứng hết
n(NO) = 1,12/22,4 = 0,05 mol
Fe + 4HNO3 → Fe(NO3)3 + NO + 4H2O
0,05 -> 0,2 -> 0,05
Fe + 2Fe(NO3)3 → 3Fe(NO3)2
x -> 3x
Theo ĐL bảo toàn nguyên tố, số mol NO3- có trong muối:
n(NO3- trong muối) = n(HNO3) - n(NO) = 0,15 mol
n(NaOH) = 0,115.2 = 0,23 mol
Sau khi NaOH pư hoàn toàn với các chất trong dd Y, dung dịch thu được có:
n(Na+) = n(NaOH) = 0,23 mol; n(Cl-) = n(HCl) = 0,1 mol → n(NO3-) = n(Na+) - n(Cl-) = 0,23 - 0,1 = 0,13 mol → Số mol NO3- bị Fe2+ khử: 0,15 - 0,13 = 0,02 mol
NO3- + 3Fe2+ + 4H+ → 3Fe3+ + NO + 2H2O
0,02 -> 0,06 -> 0,08
NO3- và H+ đều dư (H+ dư 0,02mol) → Fe2+ đã phản ứng hết
→ 3x = 0,06 → x = 0,02 mol
Tổng số mol Fe: n(Fe) = 0,05 + x = 0,07 mol
Khối lượng Fe đã sử dụng: m(Fe) = 0,07.56 = 3,92g





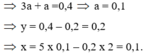



Đáp án B
n C O 2 = 0 , 2 m o l
Cho 100 ml dung dịch X vào dung dịch chứa 0,15 mol HCl thu được 0,12 mol CO2.
Do n C O 2 < n H C l < 2 n C O 2 nên dung dịch X chứa K2CO3 và KHCO3.
Gọi số mol K2CO3 và KHCO3 phản ứng lần lượt là a, b.
=> a+b= 0,12; 2a+b=0,15
Giải được a=0,03; b=0,09 vậy trong X tỉ lệ số mol K2CO3 và KHCO3 là 1:3.
Gọi số mol K2CO3 trong X là m suy ra KHCO3 là 3m.
Cho 100 ml dung dịch X tác dụng với Ba(OH)2 dư thu được 0,2 mol kết tủa BaCO3.
Do vậy 200 ml dung dịch X tác dụng thì thu được 0,4 mol kết tủa.
=> m+3m= 0,4=> m=0,1
Bảo toàn C: n K 2 C O 3 = 0 , 4 - 0 , 2 = 0 , 2
Bảo toàn K: n K O H = 0 , 1 . 2 + 0 , 3 - 0 , 2 . 2 = 0 , 1
Vậy x= 0,1