Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Nồng độ phần trăm của dung dịch:
C% = . 100% =
. 100% = 18%
nồng độ % của dung dịch \(CuSO_4\) là
\(\frac{3,6}{20}.100\%=18\%\)

Khối lượng dung dịch C u S O 4 ban đầu:
m d d = V.D = 165,84.1,206=200(g)
Nồng độ % của dung dịch C u S O 4 :
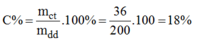

1)
\(m_{ddCuSO_4\left(bd\right)}=1,6.25=40\left(g\right)\)
\(n_{CuSO_4.5H_2O}=\dfrac{11,25}{250}=0,045\left(mol\right)\)
=> \(n_{CuSO_4}=0,045\left(mol\right)\)
\(C_M=\dfrac{0,045}{0,025}=1,8M\)
\(C\%=\dfrac{0,045.160}{40}.100\%=18\%\)
b)
\(m_{CuSO_4}=\dfrac{200.18}{100}=36\left(g\right)\)
\(n_{CuSO_4.5H_2O}=\dfrac{5,634}{250}=0,022536\left(mol\right)\)
nCuSO4 (tách ra) = 0,022536 (mol)
=> \(m_{CuSO_4\left(dd.ở.t^o\right)}=36-0,022536.160=32,39424\left(g\right)\)
\(m_{H_2O\left(bd\right)}=200-36=164\left(g\right)\)
nH2O (tách ra) = 0,022536.5 = 0,11268 (mol)
=> \(m_{H_2O\left(dd.ở.t^o\right)}=164-0,11268.18=161,97176\left(g\right)\)
\(S_{t^oC}=\dfrac{32,39424}{161,97176}.100=20\left(g\right)\)

Theo de bai ta co
mddCuSO4=D.V=1,206.165,84\(\approx\)200 g
\(\Rightarrow\)Nong do % cua dd CuSO4 da dung la
C%=\(\dfrac{mct}{mdd}.100\%=\dfrac{36}{200}.100\%=18\%\)

5 Nồng độ phần trăm là gì? Trong hóa học, nồng độ phần trăm của dung dịch được kí hiệu là C% cho ta biết số gam chất tan có trong 100 gam dung dịch là bao nhiêu
C%=\(\dfrac{20}{620}.100=3,22\%\)
CM=\(\dfrac{1,5}{0,75}\)=2M
6 ko giải thích lại
C%=\(\dfrac{30}{230}100=13\%\)
CM=\(\dfrac{1}{0,2}\)=5M

C% CuSO4 = \(\dfrac{32}{200}\).100% = 16%
Ta có ct:
CM = \(\dfrac{C\%.D.10}{M}\)=\(\dfrac{16.1,2.10}{160}\)= 1,2 M
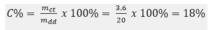
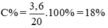

Nồng độ phần trăm của dung dịch:
C% =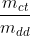 . 100% =
. 100% =  . 100% = 18%
. 100% = 18%
nồng độ % của dung dịch \(CuSO_4\) là
\(\frac{3,6}{20}.100\%=18\%\)