Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

\(n_{O_2}=\dfrac{3,36}{22,4}=0,15\left(mol\right)\)
PTHH: 2KMnO4 --to--> K2MnO4 + MnO2 + O2
0,3<------------------------------0,15
2KClO3 --to--> 2KCl + 3O2
0,1<-----------------0,15
=> \(\left\{{}\begin{matrix}m_{KMnO_4}=0,3.158=47,4\left(g\right)\\m_{KClO_3}=0,1.122,5=12,25\left(g\right)\end{matrix}\right.\)
=> Dùng KClO3 sẽ cần khối lượng nhỏ hơn

Dùng KClO3
PTHH: \(2KClO_3\xrightarrow[MnO_2]{t^o}2KCl+3O_2\uparrow\)
Ta có: \(n_{O_2}=\dfrac{4,48}{22,4}=0,2\left(mol\right)\) \(\Rightarrow n_{KClO_3}=\dfrac{2}{15}\left(mol\right)\)
\(\Rightarrow m_{KClO_3}=\dfrac{2}{15}\cdot122,5\approx16,33\left(g\right)\)

\(Coi\ n_{O_2} = 3(mol)\\ 2KMnO_4 \xrightarrow K_2MnO_4 + MnO_2+ O_2\\ n_{KMnO_4} = 2n_{O_2} = 6(mol)\\ 2KClO_3 \xrightarrow{t^o} 2KCl + 3O_2\\ n_{KClO_3} = \dfrac{2}{3}n_{O_2} = 2(mol)\\ \dfrac{m_{KMnO_4}}{m_{KClO_3}} = \dfrac{6.158}{2.122,5} = 3,869\)
\(2KMnO_4\underrightarrow{^{t^0}}K_2MnO_4+MnO_2+O_2\)
\(2a................................a\)
\(2KClO_3\underrightarrow{^{t^0}}2KCl+3O_2\)
\(\dfrac{2a}{3}..................a\)
\(m_{KMnO_4}=2a\cdot158=316a\left(g\right)\)
\(m_{KClO_3}=\dfrac{2}{3}a\cdot122.5=\dfrac{245a}{3}\left(g\right)\)
\(\dfrac{m_{KMnO_4}}{m_{KClO_3}}=\dfrac{316a}{\dfrac{245a}{3}}=\dfrac{948}{245}\)

-Gọi số mol của oxygen là a (mol) \(\left(a>0\right)\)
-PTHH (1): \(2KMnO_4\rightarrow^{t^0}K_2MnO_4+MnO_2+O_2\)
2a a (mol)
\(\Rightarrow m_{KMnO_4}=n.M=2a.158=316a\left(g\right)\)
-PTHH (2): \(2KClO_3\rightarrow^{t^0}2KCl+3O_2\)
\(\dfrac{2}{3}a\) a (mol)
\(\Rightarrow m_{KClO_3}=n.M=\dfrac{2}{3}a.122,5\approx81,67.a\left(g\right)\)
\(\dfrac{m_{KMnO_4}}{m_{KClO_3}}=\dfrac{316.a}{81,67.a}\approx3,87\)

PTHH: 3Fe + \(2O_2\) --->\(Fe_3O_4\)
theo pt: 3_____2_____________1
theo đề: x______y_____________0.01
nFe3O4 là: 0.01mol
\Rightarrow nO2= 0.01*2/1=0.02 mol
VO2= 0.02*22.4=0.448l
b, PTHH : 2KMnO4 ----> K2MnO4 + MnO2 + O2
theo pt: 2__________1________1______1
theo đề: x___________________________0.02
=> n KMnO4= 0.02*2/1= 0.04 mol
=>mKMnO4= 0.04*158=6.32g
a. số mol của là :
2.32 : 232 =0.01 mol
theo tỉ lệ mol ta có số mol của Fe là:
0.01 * 3 = 0.03 mol
khối lượng sắt là: 0.03*56=1.68g
số mol oxi là: 0.01*2=0.02mol
thể tích oxi là: 0.02*22.4= 0.448g
b. 2KMnO_4 ---> K2MnO4 + MnO2 + O2
---> nKMnO_4 = 2nO2 = 0,04 mol ---> mKMnO_4=0.04*158=6.32g

PTHH :
\(2KClO_3\underrightarrow{t^o}2KCl+3O_2\)
1/3 0,5
\(2MnO_4\underrightarrow{t^o}K_2MnO_4+MnO_2+O_2\uparrow\)
1 0,5
Vậy khi điều chế cùng lượng O2 ta dùng KClO3 lợi hơn vì với 1 mol KClO3 sẽ cho ra 1,5 mol O2 còn KMnO4 chỉ cho ra 0,5 mol O2
\(n_{O_2}=\dfrac{11,2}{22,4}=0,5\left(mol\right)\)
\(m_{KClO_3}=122,5.\dfrac{1}{3}=\dfrac{245}{6}\approx40,8\left(g\right)\)
\(m_{KMnO_4}=158.1=158\left(g\right)\)

\(2KMnO_4\underrightarrow{^{t^0}}K_2MnO_4+MnO_2+O_2\)
\(\dfrac{a}{158}.............................\dfrac{a}{79}\)
\(2KClO_3\underrightarrow{^{t^0}}2KCl+3O_2\)
\(\dfrac{a}{122.5}............\dfrac{3a}{245}\)
\(TC:\)
\(\dfrac{a}{79}>\dfrac{3a}{245}\)
=> Lượng Cl2 điều chế từ KMnO4 lớn nhất.

a) Phương trình hóa học của phản ứng:
3Fe + 2O2 → Fe3O4.
nFe3O4 = 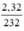 = 0,01 mol.
= 0,01 mol.
nFe = 3.nFe3O4 = 0,01 .3 = 0,03 mol.
nO2 = 2.nFe3O4 = 0,01 .2 = 0,02 mol.
mFe = 0,03.56 = 1,68g.
mO2 = 0,02.32 = 0,64g.
b) Phương trình phản ứng nhiệt phân KMnO4:
2KMnO4 → K2MnO4 + MnO2 + O2
nKMnO4 = 2.nO2 = 0,02.2 = 0,04 mol.
mKMnO4 = 0,04 .158 = 6,32g.

nO2 = \(\frac{4,48}{22,4}=0,2\) mol
Pt: 2KMnO4 --to--> K2MnO4 + MnO2 + O2
....0,4 mol<----------------------------------0,2 mol
mKMnO4 = 0,4 . 158 = 63,2 (g)
Pt: 2KClO3 --to--> 2KCl + 3O2
...0,13 mol<-----------------0,2 mol
mKClO3 = 0,13 . 122,5 = 15,9 (g)
Vậy nên chọn KClO3 để có khối lượng nhỏ nhất