Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Trường hợp 1:
Cả 2 muối cùng phản ứng
Gọi số mol
AgCl : x mol ; AgBr: y mol
\(\left\{{}\begin{matrix}74,5x+119y=87,4\\143,5x+188y=33,15\end{matrix}\right.\Rightarrow\left\{{}\begin{matrix}x=-4,07\\y=3,28\end{matrix}\right.\)
Có nghiệm âm, loại
Trường hợp 2
Chỉ có KCl tác dụng
\(n_{AgCl}=\frac{33,15}{143,5}=0,23\left(mol\right)\)
\(n_{AgCl}=n_{KCl}=0,23\left(mol\right)\)
\(m_{KCl}=0,23.74,5=17,135\left(g\right)\)
\(m_{KBr}=87,4-17,35=70,265\left(g\right)\)
Trường hợp 3:
Chỉ có KBr tác dụng:
\(n_{AgBr}=\frac{33,15}{188}=0,18\left(mol\right)\)
\(n_{AgBr}=n_{KBr}=0,18\left(mol\right)\)
\(m_{KBr}=0,18.119=21,42\left(g\right)\)
\(m_{KCl}=87,4-21,42=65,98\left(g\right)\)

Đáp án A
Các phương trình phản ứng :

Tính toán:
Gọi số mol các chất trong X là Fe: a mol; C: 2a mol. Ta có:

Sơ đồ phản ứng :
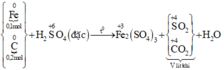
Các quá trình nhường, nhận electron:


\(Đặt:\)
\(n_{Fe}=x\left(mol\right)\\ n_{Fe\left(ỌH\right)_2}=y\left(mol\right)\\ n_{FeCO_3}=z\left(mol\right)\)
\(n_{hh}=x+y+z=0.06\left(mol\right)\left(1\right)\)
\(Fe+2HCl\rightarrow FeCl_2+H_2\\ Fe\left(OH\right)_2+2HCl\rightarrow FeCl_2+H_2O\\ FeCO_3+2HCl\rightarrow FeCl_2+CO_2+H_2O\)
\(n_{HCl}=2x+2y+2z=2\left(x+y+z\right)=2\cdot0.06=0.12\left(mol\right)\\ \Rightarrow n_{HCl\left(dư\right)}=0.16-0.12=0.04\left(mol\right)\)
\(n_{FeCl_2}=n_{Fe\left(hh\right)}=0.06\left(mol\right)\)
\(FeCl_2+2AgNO3\rightarrow Fe\left(NO3\right)_2+2AgCl\\ HCl+AgNO3\rightarrow HNO3+AgCl\)
\(n_{AgCl}=2n_{FeCl_2}+n_{HCl\left(dư\right)}=2\cdot0.06+0.04=0.16\left(mol\right)\)
\(m_{AgCl}=0.16\cdot143.5=22.96\left(g\right)\)

Đáp án C
Ta có:
Fe + 2HCl→ FeCl2 + H2
Fe3O4 + 8HCl → 2FeCl3 + FeCl2 + 4H2O
![]()
![]()
Bảo toàn Fe: nFe bđ = 0,2 + 0,2.3 = 0,8
2Fe → Fe2O3
0,8 → 0,4
=> m = 0,4.160 = 64 (g)





Gọi : \(\left\{{}\begin{matrix}n_{KF}=a\left(mol\right)\\n_{KCl}=a\left(mol\right)\\n_{KBr}=3a\left(mol\right)\\n_{KI}=3a\left(mol\right)\end{matrix}\right.\)⇒ 58a + 74,5a + 3a.119 + 3a.166=98,75
⇒ a = 0,1
KCl + AgNO3 → AgCl + KNO3
0,1........................0,1....................(mol)
KBr + AgNO3 → AgBr + KNO3
0,3.........................0,3......................(mol)
KI + AgNO3 → AgI + KNO3
0,3....................0,3.............................(mol)
Vậy :
a = 0,1.143,5 + 0,3.188 + 0,3.235 = 141,25(gam)