Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án A
- Xét quá trình phản ứng của Al với dung dịch X ta có:
![]()
![]()
![]()
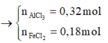
- Trong Y có
![]()
![]()
![]()
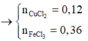
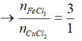

Ta có: \(n_{Al}=\dfrac{8,64}{27}=0,32\left(mol\right)\)
\(Al:0,32\left(mol\right)+74,7\left(g\right)\left\{{}\begin{matrix}CuCl_2:x\\FeCl_3:0,18+y\end{matrix}\right.\) \(\rightarrow\) \(17,76\left(g\right)\left\{{}\begin{matrix}Cu:x\\Fe:y\end{matrix}\right.\) + \(\left\{{}\begin{matrix}AlCl_3\\FeCl_2\end{matrix}\right.\)
Theo ĐLBT KL, có: mAlCl3 + mFeCl2 = 8,64 + 74,7 - 17,76 = 65,58 (g)
BTNT Al, có: nAlCl3 = nAl = 0,32 (mol)
⇒ nFeCl2 = 0,18 (mol)
Có: 64x + 56y = 17,76 (1)
BT e, có: 2x + 3y + 0,18.1 = 0,32.3 (2)
Từ (1) và (2) \(\Rightarrow\left\{{}\begin{matrix}x=0,12\left(mol\right)\\y=0,18\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow\dfrac{n_{FeCl_3}}{n_{CuCl_2}}=\dfrac{0,18+0,18}{0,12}=\dfrac{3}{1}\)

Đáp án B
Ở anot thu được hỗn hợp khí gồm Cl2 và O2, dựa vào tỉ khối ta có tỉ lệ số mol 2 khí này là 6:1.
Gọi số mol O2 là x mol suy ra số mol Cl2 là 6x.
Ở catot thu được Cu 8x mol.
Khối lượng dung dịch giảm là do O2, Cu, Cl2 thoát ra
![]()
Giải được: x=0,03
![]()
Khối lượng kim loại Cu bàm vào catot là 158,36 gam.
Cho Ba(OH)2 dư vào dung dịch sau điện phân kết tủa thu được gồm a mol BaSO4 và a-0,24 mol Cu(OH)2.
![]()
Giải được a=0,48.
Khối lượng chất tan trong X là 97,86 gam.
4,68 gam hỗn hợp Al và Mg có tỉ lệ số mol 2:1 gồm có 0,12 mol Al và 0,06 mol Mg.
Ta có: ![]()
nên lượng khí oxi hóa vừa đủ.
Điện phân X trong 20072 giây tức số mol e là 1,04 mol.
Ở catot thu được Cu 0,48 mol và H2 0,04 mol.
Ở anot thu được Cl2 0,18 mol và O2 0,17 mol.
Tổng số mol khí thoát ra là 0,39 mol

Đáp án A
- Phương trình điện phân
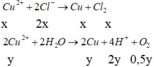
Có mdung dịch giảm = m Cu + m Cl 2 + m O 2 = 64 ( x + y ) + 71 x + 32 . 0 , 5 y = 20 , 815 gam
Cho (Mg, MgO) + dung dịch sau điện phân → 18,16g muối + 0,012mol khí Y
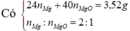
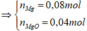
m muối = m Mg ( NO 3 ) 2 + m NH 4 NO 3 = 148 . ( 0 , 08 + 0 , 04 ) + 80 n NH 4 NO 3 = 18 , 16 g ⇒ n NH 4 NO 3 = 0 , 005 mol
+ Giả sử 1 mol N+5 nhận n mol e để chuyển thành N trong khí Y
Áp dụng bảo toàn electron có:
![]()
=> n = 10 => Khí Y là N2
m muối = m Mg ( NO 3 ) 2 + m NH 4 NO 3 = 148 . ( 0 , 08 + 0 , 04 ) + 80 n NH 4 NO 3 = 18 , 16 g ⇒ 2 y = 2 n Mg ( NO 3 ) 2 + 2 n NH 4 NO 3 + 2 n N 2 = 0 , 274 mol
=>Thời gian điện phân t = ( 0 , 137 + 0 , 073 ) . 2 . 96500 5 = 8016 s

Đáp án D
Cho hỗn hợp kim loại trên vào dung dịch chứa FeCl3 và CuCl2 sau phản ứng thu được dung dịch X và rắn Y. Cho AgNO3 dư vào X thấy AgNO3 phản ứng 0,54 mol và thu được kết tủa là AgCl và Ag.
Giải được số mol AgCl và Ag lần lượt là 0,48 và 0,06 mol.
Gọi số mol FeCl3 lần lượt là a thì số mol CuCl2 là 1,5a
Bảo toàn Cl: 3 a + 1 , 5 a . 2 = 0 , 48 → a = 0 , 08 m o l
Ta có số mol Ag là 0,06 nên số mol FeCl2 trong X phải là 0,06 mol.
Do vậy chỉ có Al phản ứng với dung dịch muối ban đầu vì số mol FeCl2 nhỏ hơn FeCl3.
→ n A l = 0 , 08 + 0 , 02 . 2 + 0 , 12 . 2 3 = 0 , 12 = n F e
Do vậy rắn Y chứa Fe 0,14 mol, Cu 0,12 mol
→ x = 15 , 52 g a m

Đáp án B
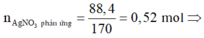
![]()
=> Chứng tỏ kết tủa gồm AgCl và Ag.
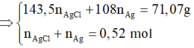
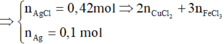
= 0,42 mol
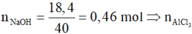
![]()
![]()
![]()
Chứng tỏ Fe và Al phản ứng hết.
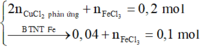
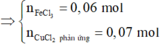
![]()