


Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.



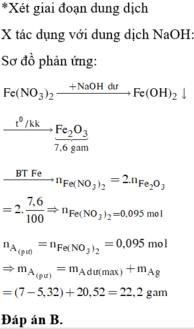

Đáp án D
M g S O 4 : : a F e S O 4 : b → M g O : a F e 2 O 3 : 0 , 5 b → → T G K L 40 a + 8 b = 6 , 9 - 5 , 1 40 a + 80 b = 4 , 5 → a = b = 0 , 0375 → n C u S O 4 = 0 , 075 → x = 0 , 3

Gọi a, b là số mol Mg, Fe phản ứng.
Mg+CuSO4→MgSO4+Cu
a_____a_______a____a
Fe+CuSO4→FeSO4+Cu
b____b_______b_____b
(Nếu giải ra b>0 thì Fe đã phản ứng. Nếu giải ra b=0 thì Fe chưa phản ứng)
MgSO4+2NaOH→Mg(OH)2+Na2SO4
a________________a
FeSO4+2NaOH→Fe(OH)2+Na2SO4
b________________b
Mg(OH)2→MgO+H2O
a_________a
4Fe(OH)2+O2→2Fe2O3+4H2O
b______________b/2
5,1-24a-56b+64(a+b)=6,9
=> 5a+b=0,225
40a+160b/2=4,5
Giải hệ, được a=b=0,0375
%mMg=24.0,0375/5,1.100%=17,65%
%mFe=100%-17,65%=82,35%
Số mol Fe có trong A bằng(5,1-24.0,0375)/56=0,075(mol)
Fe dư và CuSO4 phản ứng hết.
nCuSO4=a+b=0,0375+0,0375=0,075(mol)
CM(CuSO4) =0,075/0,25=0,3(M) → Đáp án D
Cho 5,1 gam hỗn hợp gồm Mg và Fe vào 250 ml dung dịch CuSO4. Sau khi các phản ứng xảy ra hoàn toàn, lọc, thu được 6,9 gam chất rắn X và dung dịch Y chứa hai muối. Thêm dung dịch NaOH dư vào dung dịch Y. Lọc lấy kết tủa đem nung ngoài không khí đến khối lượng không đổi được 4,5 gam chất rắn Z.
a) Tính thành phần phần trăm theo khối lượng của Mg trong hỗn hợp ban đầu.
b) Tính nồng độ mol của dung dịch CuSO4.
c) Tính thể tích khí SO2 (đo ở đktc) thu được khi hoà tan hoàn toàn 6,9 gam chất rắn X trong dung dịch H2SO4 đặc, nóng.
cho mình hỏi câu này với ạ

Chọn đáp án C
Giả sử KOH tác dụng với X thì KOH hết ⇒ n KNO 3 = n KOH = 0 , 5 mol.
⇒ m KNO 3 = 0 , 5 x 101 = 50 , 5 gam gam > 41,05 gam ⇒ vô lí ⇒ KOH dư.
Đặt n KOH dư = x mol; n KNO 3 = y mol
![]()
Phản ứng:
![]()
Giải hệ có: x = 0,05 mol; y = 0,45 mol
![]()
Đặt n Fe = a mol; n Cu = b mol ⇒ m A = 56 a + 64 b = 11 , 6 gam.
Do KOH dư ⇒ kết tủa hết ion kim loại ⇒ nung T thì rắn gồm Fe2O3 và CuO.
⇒ mrắn = 41,05 = 0,5a × 160 + 80b. Giải hệ có: a = 0,15 mol; b = 0,05 mol.
Quy hỗn hợp B về N và O. Bảo toàn nguyên tố nitơ có nN spk = 0,7 – 0,45 = 0,25 mol.
![]()
⇒ dung dịch chứa ion Fe2+, Fe3+ và H+ hết.!
Bảo toàn nguyên tố hidro có n H 2 O = 0 , 7 ÷ 2 = 0 , 35 mol.
⇒ bảo toàn nguyên tố oxi có nO sk = 0,7 × 3 – 0,45 × 3 – 0,35 = 0,4 mol.
⇒ BTKL mdung dịch sau phản ứng = 11,6 + 87,5 – 0,25 × 14 – 0,4 × 16 = 89,2 gam.
![]()

Đáp án A
Bài này có thể giải theo kinh nghiệm,
hoặc biện luận rào số mol hỗn hợp A.
Từ đó ⇒ giới hạn của chất rắn C
Trường hợp xả ra đó là:
Fe pứ hết và Cu chỉ pứ 1 phần
⇒ C gồm Ag và Cu chưa tan.
+ Sơ đồ ta có:
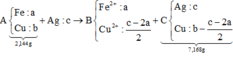

PT theo khối lượng oxit:
40c = 2,56 Û c = 0,064 mol
⇒ CM AgNO3 = 0,064 ÷ 0,2 = 0,32