Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

- Chất rắn không tan là Cu
\(\Rightarrow\) %Cu = \(\dfrac{0,04.100}{3}\) \(\approx\) 1,3%
\(\Rightarrow\) %Fe3O4 = \(\dfrac{\left(3-0,04\right).100}{3}\) \(\approx\) 98,7%

Bước 1: Tính khối lượng chất rắn có trong dd y ban đầu: Khối lượng chất rắn tan trong dd y = Khối lượng dd y - Khối lượng các muối tan = 15,4g + 2,56g = 17,96g
Bước 2: Tính số mol các chất trong dd y: Số mol Cu = Khối lượng Cu / Khối lượng mol Cu = 2,56g / 63,55g/mol Số mol Fe3O4 = Khối lượng Fe3O4 / Khối lượng mol Fe3O4 = (17,96g - 2,56g) / (55,85g/mol + 3 x 16g/mol) Số mol FeO = Số mol Fe3O4 / 3
Bước 3: Xác định phản ứng giữa dd y và AgNO3: Phản ứng xảy ra giữa Cu và AgNO3 theo phương trình: Cu + 2AgNO3 → Cu(NO3)2 + 2Ag
Bước 4: Tính số mol AgNO3 cần để phản ứng hoàn toàn với Cu: Số mol AgNO3 = 2 x Số mol Cu
Bước 5: Tính khối lượng chất rắn không tan thu được sau phản ứng với AgNO3: Khối lượng chất rắn không tan = Số mol AgNO3 x Khối lượng mol AgNO3
Bước 6: Tính m: m = Khối lượng chất rắn không tan sau phản ứng với AgNO3 - Khối lượng chất rắn không tan ban đầu
Lưu ý: Trong quá trình tính toán, cần sử dụng đúng các khối lượng mol của các chất và phương trình phản ứng để xác định số mol và chất rắn không tan thu được.

TN1: Fe3O4 + 8HCl → 2FeCl3 + FeCl2 + 4H2O
2FeCl3 + Cu → CuCl2 + 2FeCl2
Vì Cu còn dư 0,1 mol nên sau phản ứng chứa FeCl2 : 3a mol, CuCl2 : a mol
→ a. 232 + 64. ( a + 0,1)= 24,16 → a = 0,06 mol
Vậy X gồm Cu: 0,16 mol và Fe3O4 : 0,06 mol
+ Nhận thấy nếu chất rắn chỉ chứa NaNO2 : 0,12 mol thì mchất rắn = 0,12. 69 > 78,16 gam.
⇒ Chất rắn chứa đồng thời NaNO2 : x mol và NaOH : y mol
Giả sử sản phẩm khử chứa N và O
Bảo toàn nguyên tố N → nN = 1,2 - 1,04 = 0,16 mol
Bảo toàn electron → 2nCu + nFe3O4 = 5nN - 2nO → nO = 0,21 mol
Bảo toàn khối lượng → mdd = 24,16 + 240 - 0,16.14 - 0,21. 16 = 258,56 gam
%Cu(NO3)2 =0.16*188/258,56 . 100% = 11,63%

a) Zn+2HCl---.ZnCl2 +H2
x-----------------------------x
Fe+2HCl--->FeCl2 +H2
y---------------------------y
b) m\(_{Cu}=\)5,1(g)
=>m \(_{Fe+Zn}=20-5,1=14,9\left(g\right)\)
n\(_{H2}=\frac{5,6}{22,4}=0,25\left(mol\right)\)
Suy ra ta có hệ pt
\(\left\{{}\begin{matrix}65x+56y=14,9\\x+y=0,25\end{matrix}\right.\Rightarrow\left\{{}\begin{matrix}0,1\\0,15\end{matrix}\right.\)
%m\(_{Cu}=\frac{5,1}{20}.100\%=25,5\%\)
%m\(_{Zn}=\frac{0,1.65}{20}.100\%=32,5\%\)
%m\(_{Fe}=\frac{0,15.56}{20}.100\%=42\%\)

Đáp án B
Đặt
![]()
Khối lượng muối khan giảm là do đã xảy ra phản ứng thay thế các nguyên tử halogen trong muối.
Ta có hệ:
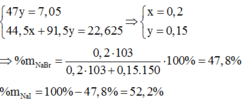

\(Đặt:\)
\(\left\{{}\begin{matrix}n_{Mg}=x\left(mol\right)\\\\n_{Fe}=y\left(mol\right)\end{matrix}\right.\)
\(n_{H_2}=\dfrac{6.72}{22.4}=0.3\left(mol\right)\)
\(Mg+2HCl\rightarrow MgCl_2+H_2\\ Fe+2HCl\rightarrow FeCl_2+H_2\)
\(m_{hh}=24x+56y=13.6\left(g\right)\\ n_{H_2}=x+y=0.3\left(mol\right)\)
\(\Rightarrow\left\{{}\begin{matrix}x=0.1\\y=0.2\end{matrix}\right.\)
\(\%Mg=\dfrac{0.1\cdot24}{13.6}\cdot100\%=17.64\%\\ \%Fe=100-17.64=82.36\%\)
\(n_{HCl}=2n_{H_2}=2\cdot0.3=0.6\left(mol\right)\)
\(V_{HCl}=\dfrac{0.6}{2}=0.3\left(l\right)\)
\(m_Y=m_{MgCl_2}+m_{FeCl_2}=0.1\cdot95+0.2\cdot127=34.9\left(g\right)\)

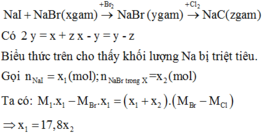
- Chất rắn không tan là Cu
\(\Rightarrow\) %Cu = \(\dfrac{0,04.100}{3}\) \(\approx\) 1,3%
\(\Rightarrow\) %Fe3O4 = \(\dfrac{\left(3-0,04\right).100}{3}\) \(\approx\) 98,7%