Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

nFe = 22.4/56 = 0.4 (mol)
nH2SO4 = 24.5/98 = 0.25 (mol)
Fe + H2SO4 => FeSO4 + H2
0.25.....0.25.....................0.25
mFe(dư) = ( 0.4 - 0.25 ) * 56 = 8.4 (g)
VH2 = 0.25 * 22.4 = 5.6 (l)
nFe=\(\dfrac{22,4}{56}\)= 0,4 ( mol)
nH2SO4=\(\dfrac{24,5}{98}\)=0,25 ( mol )
Fe + H2SO4 → FeSO4 + H2
Trước phản ứng: 0,4 0,25 ( mol )
Phản ứng: 0,25 0,25 0,25 ( mol )
Sau phản ứng: 0,15 0,25 0,25 ( mol )
a) m= n.M= 0,15.56=8,4 (g)
vậy Fe còn dư và dư 8,4 gam
b) VH2= n.22,4= 0,25.22,4=5,6 (l)

TIẾP BÀI 3
Fe+H2SO4->FeSO4+H2
nFe=28\56=0,5 mol
nH2SO4=39,2\98=0,4 mol
=>fe dư=>mFe dư=0,1.56=5,6g
=>VH2 0,4.22,4=8,96 l
Câu 1: -Phản ứng thế là phản ứng trong đó có nguyên tử hoặc nhóm nguyên tử trong phân tử chất hữu cơ bị thay thế bởi 1 nguyên tử hoặc nhóm nguyên tử khác
Vd: \(CH_4+Cl_2-ánhsáng->CH_3Cl+HCl\)
Câu 2: -Phản ứng phân hủy là phản ứng từ 1 chất tham gia tạo ra 2 hay nhiều chất sản phẩm.
VD:
2KNO3 --> 2KNO2 + O22Fe(OH)3 --> Fe2O3 + 3H2O Câu 3: mình chưa tính

a) \(Pt:Fe+H_2SO_4\rightarrow FeSO_4+H_2\)
\(n_{Fe}=\dfrac{22,4}{56}=0,4mol\)
\(n_{H_2SO_4}=\dfrac{24,5}{98}=0,25mol\)
Lập tỉ lệ
\(n_{Fe}:n_{H_2SO_4}=\dfrac{0,4}{1}:\dfrac{0,25}{1}=0,4:0,25\)
Do 0,4>0,25
=> Fe dư
Theo pt: \(n_{H_2}=n_{H_2SO_4}=0,25mol\)
=> \(V_{H_2}=0,25.22,4=5,6lít\)
b) Fe là chất dư sau phản ứng
\(n_{Fe}dư=0,4-0,25=0,15mol\)
\(m_{Fe}dư=0,15.56=8,4g\)
\(a) Fe + H_2SO_4 \to FeSO_4 + H_2\\ n_{Fe} = \dfrac{22,4}{56} = 0,4 > n_{H_2SO_4} = \dfrac{24,5}{98} = 0,25(mol) \to Fe\ dư\\ n_{H_2} = n_{H_2SO_4} = 0,25(mol)\\ V_{H_2} = 0,25.22,4 = 5,6(lít)\\ b) n_{Fe\ pư} = n_{H_2SO_4} = 0,25(mol)\\ \Rightarrow m_{Fe\ dư} = 22,4 - 0,25.56 = 8,4(gam)\)

\(n_{Fe}=\dfrac{22,4}{56}=0,4\left(mol\right);n_{H_2SO_4}=\dfrac{24,5}{98}=0,25\left(mol\right)\\ PTHH:Fe+H_2SO_4\rightarrow FeSO_4+H_2\\ Vì:\dfrac{0,4}{1}>\dfrac{0,25}{1}\Rightarrow Fe.dư\\ n_{H_2}=n_{Fe\left(p.ứ\right)}=n_{H_2SO_4}=0,25\left(mol\right)\\ a,V_{H_2\left(đktc\right)}=0,25.22,4=5,6\left(l\right)\\ b,n_{Fe\left(dư\right)}=0,4-0,25=0,15\left(g\right)\\ m_{Fe\left(dư\right)}=0,14.56=8,4\left(g\right)\)

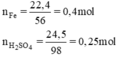
Phương trình hóa học của phản ứng:

So sánh tỉ lệ 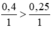 ⇒ Fe dư
⇒ Fe dư
Theo PT nFe (pư) = nH2SO4 = 0,25 mol ⇒ nFe dư = 0,4 – 0,25 = 0,15 mol
mFe dư = 0,15. 56 = 8,4g.
Do khối lượng Fe dư nên tính thể tích khí H2 theo số mol H2SO4.
nH2 = nH2SO4 = 0,25 mol
Vkhí = 0,25 . 22,4 = 5,6l.

\(n_{Al}=\dfrac{2,5}{27}=\dfrac{25}{270}=\dfrac{5}{54}\left(mol\right)\\ n_{H_2SO_4}=0,5\left(mol\right)\\ a,2Al+3H_2SO_4\rightarrow Al_2\left(SO_4\right)_3+3H_2\\ b,Vì:\dfrac{\dfrac{5}{54}}{2}< \dfrac{0,5}{4}\Rightarrow H_2SO_4dư\\ b,n_{H_2SO_4\left(dư\right)}=0,5-\dfrac{3}{2}.\dfrac{5}{54}=\dfrac{13}{36}\left(mol\right)\\ \Rightarrow m_{H_2SO_4}=\dfrac{13}{36}.98=\dfrac{637}{18}\left(g\right)\\ c,n_{H_2}=\dfrac{3}{2}.n_{Al}=\dfrac{3}{2}.\dfrac{5}{54}=\dfrac{5}{36}\left(mol\right)\\ \Rightarrow V_{H_2\left(đktc\right)}=\dfrac{5}{36}.22,4=\dfrac{28}{9}\left(l\right)\)

a: \(2Al+3H_2SO_4\rightarrow Al_2\left(SO_4\right)_3+3H_2\)
b: \(n_{Al}=\dfrac{2.5}{27}< \dfrac{1}{4}\)
=>H2SO4 dư, Al đủ
\(m_{H_2SO_4}=0.25\cdot98=24.5\left(g\right)\)
c: \(n_{Al_2\left(SO_4\right)_3}=\dfrac{2.5}{54}=\dfrac{5}{108}\left(mol\right)\)
\(\Leftrightarrow n_{H_2}=\dfrac{5}{36}\left(mol\right)\)
\(V_{H_2}=\dfrac{5}{36}\cdot22.4=\dfrac{28}{9}\left(lít\right)\)
Mình thấy bạn Thịnh tính lượng dư sai
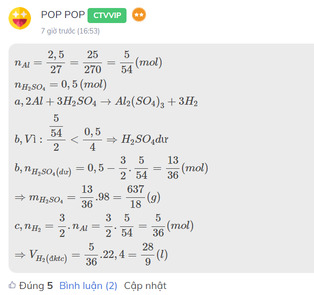
Đây là bài mình từng làm, bạn tham khảo nhé!

a) nFe=0,4(mol); nH2SO4=0,5(mol)
PTHH: Fe + H2SO4 -> FeSO4 + H2
Ta có: 0,4/1 < 0,5/1
=> Fe hết, H2SO4 dư. tính theo nFe.
=> nH2= nH2SO4(p.ứ)=nFe=0,4(mol)
=>nH2SO4(dư)=0,5-0,4=0,1(mol)
=>H2SO4(dư)=0,1.98=9,8(g)
b) V(H2,dktc)=0,4.22,4=8,96(l)