Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án : A
nCH4=10 mol
2CH4 --> C2H2 + 3H2 (1)
2x------->x-------->3x
CH4 -->C + 2H2 (2)
y------------->2y
sau phản ứng ta được:
x(mol) C2H2; 10-(2x+y) (mol) CH4 và 3x+2y (mol) H2
ta có các phương trính sau:
x/0,12 = [10 - (2x + y)]/0,1 = (3x + 2y)/0,78
Giải ra ta được:
x=24/11; y=42/11
Tổng số mol của các khí trong A là:
x+10-(2x+y)+3x+2y=2x+y+10=18,1818 mol
Vậy V=18,1818.22,4 = 407.2727 (l)

Đáp án : C
Ta có Cùng điều kiện -> Quy số lít về số mol.n(hh ban đầu) = 20 mol; n(hh sau) = 16 lít
=> H2 phản ứng mất 4 lít => C2H2 có 2 lít và CH4 có 8 lít

1. Giả sử trong 20,16 lít A có x mol C 2 H 2 và y mol H 2 .
Ta có: 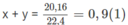
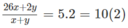
Giải hệ phương trình ta có x = 0,3 ; y = 0,6.
Thành phần hỗn hợp A:
C
2
H
2
chiếm 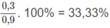
H 2 chiếm 100% - 33,33% = 66,67%
Khi A qua chất xúc tác Ni, xảy ra phản ứng cộng. C 2 H 2 hợp hiđro có thể tạo thành C 2 H 4 hoặc thành C 2 H 6 hoặc thành cả 2 chất đó :
C 2 H 2 + H 2 → C 2 H 4
C 2 H 2 + 2 H 2 → C 2 H 6
Số mol khí trong hỗn hợp B : 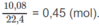
Trong hỗn hợp A có 0,3 mol C 2 H 2 thì trong hỗn hợp B cũng có 0,3 mol các hiđrocacbon.
Số mol H 2 trong B là: 0,45 - 0,3 = 0,15 (mol).
Số mol H 2 đã tham gia phản ứng: 0,6 - 0,15 = 0,45 (mol).
Khi B đi qua nước brom dư, những hiđrocacbon không no đều bị giữ lại hết (phản ứng hoàn toàn).
Vậy hỗn hợp C chỉ còn lại C 2 H 6 và H 2 với số mol tổng cộng là:

trong đó số mol H 2 là 0,15 mol, vậy số mol C 2 H 6 là : 0,33 - 0,15 = 0,18 (mol).
Thành phần hỗn hợp C:
C2H6 chiếm 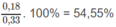
H2 chiếm 100% - 55,45% = 45,45%.
Trong hỗn hợp B cũng phải có 0,18 mol C 2 H 6 . Để tạo ra 0,18 mol C 2 H 6 cần 0,36 mol H 2 tác dụng với C 2 H 2 . Vậy lượng H 2 tác dụng với C 2 H 2 để tạo ra C 2 H 4 là : 0,45 - 0,36 = 9. 10 - 2 (mol).
Lượng C 2 H 4 trong hỗn hợp B là 9. 10 - 2 (mol) và lượng C 2 H 2 trong B là :
0,3 - 0,18 - 9. 10 - 2 = 3. 10 - 2 mol.
Thành phần hỗn hợp B:
C
2
H
6
chiếm 
C
2
H
4
chiếm 
C
2
H
2
chiếm 
H
2
chiếm 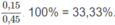
2. Khối lượng bình đựng nước brom tăng thêm :
9. 10 - 2 .28 + 3. 10 - 2 .26 = 3,3 (g).

a, PT: \(C_2H_2+AgNO_3+NH_3\rightarrow Ag_2C_{2\downarrow}+NH_4NO_3\)
\(C_2H_4+Br_2\rightarrow C_2H_4Br_2\)
b, Ta có: \(V_{CH_4}=V_Y=0,56\left(mol\right)\Rightarrow\%V_{CH_4}=\dfrac{0,56}{6,72}.100\%\approx8,33\%\)
\(V_{C_2H_4}=V_X-V_{CH_4}=3,92\left(l\right)\Rightarrow\%V_{C_2H_4}=\dfrac{3,92}{6,72}.100\%\approx58,34\left(\%\right)\)
\(\Rightarrow V_{C_2H_2}=6,72-4,48=2,24\left(l\right)\Rightarrow\%V_{C_2H_2}=\dfrac{2,24}{6,72}.100\%\approx33,33\%\)
c, \(n_{Ag_2C_2}=n_{C_2H_2}=\dfrac{2,24}{22,4}=0,1\left(mol\right)\)
\(\Rightarrow m_{Ag_2C_2}=0,1.240=24\left(g\right)\)

Đáp án : A
Do tỉ lệ thể tích bằng tỉ lệ số mol, coi 40l = 40mol, 56l = 56mol
Do cracking nên không thêm chất bên ngoài vào, vậy lượng chênh lệch trước và sau phản ứng chính là lượng butan phản ứng có số mol: 56 - 40 = 16 mol
=> H = 16/40 = 40%

Gọi nAl = x mol ; nSn = y mol → 27x + 119y = 14,6 (1) ; nH2 = 0,25 mol
- Khi X tác dụng với dung dịch HCl:
quá trình oxi hóa:
Al -> Al3 + +3e
x -> 3x
Sn -> Sn2+ +2e
y -> 2y
Qúa trình khử
2H+ + 2e -> H2
0,5<- 0,25
=> 3x+2y=0,5 (2)
(1)(2) => x=y=0,1mol
- Khi X tác dụng O2
quá trình oxi hóa
Al -> Al3 + +3e
x -> 3x
Sn -> Sn4+ +4e
y -> 4y
Qúa trình khử
O2 + 4e -> 2O2-
VO2 = ((3x +4y)/4).22,4 = ((3.0,1+4.0,1)/4).22,4 = 3,92l => D

a) \(n_X=\dfrac{33,6}{22,4}=1,5\left(mol\right);n_{C_2Ag_2}=\dfrac{144}{240}=0,4\left(mol\right);n_{CH_4}=\dfrac{11,2}{22,4}=0,5\left(mol\right)\)
PTHH:
\(C_2H_2+2AgNO_3+2NH_3\rightarrow C_2Ag_2\downarrow+2NH_4NO_3\)
0,4<---------------------------------0,4
\(C_2H_4+Br_2\rightarrow C_2H_4Br_2\)
b) \(n_{C_2H_4}=1,5-0,4-0,5=0,6\left(mol\right)\)
\(\Rightarrow\left\{{}\begin{matrix}m_{CH_4}=0,5.16=8\left(g\right)\\m_{C_2H_2}=0,4.26=10,4\left(g\right)\\m_{C_2H_4}=0,6.28=16,8\left(g\right)\end{matrix}\right.\)
c) \(2CH\equiv CH\xrightarrow[]{t^o,p,xt}CH\equiv C-CH=CH_2\)
0,4------------------>0,2
\(\Rightarrow m_{C_4H_4}=0,2.80\%.52=8,32\left(g\right)\)
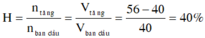
Đáp án A
Ta có:
24%VA 12%VA 36%V
21%Va 42%V