Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án B
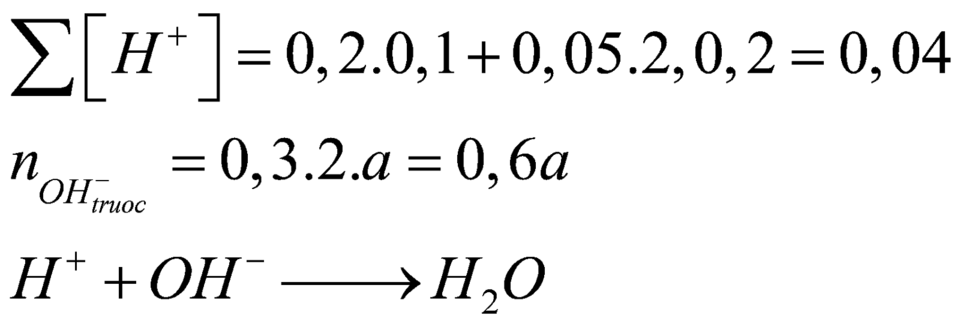
Mà sau phản ứng thu được dung dịch bazo có ph=13 (500ml)nên ta có
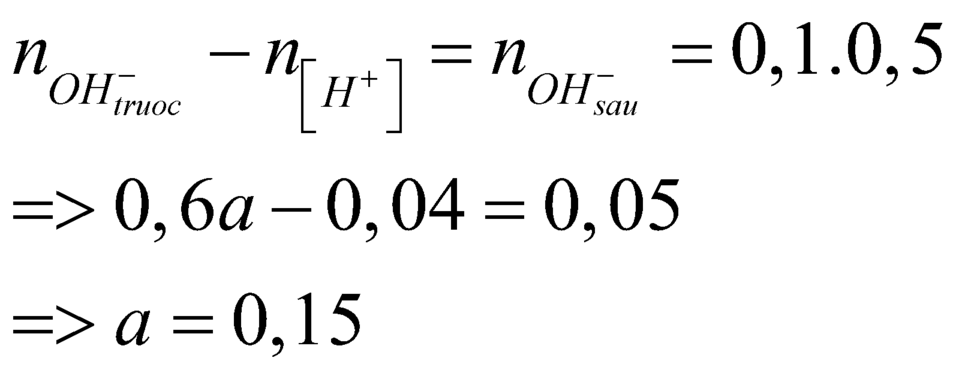
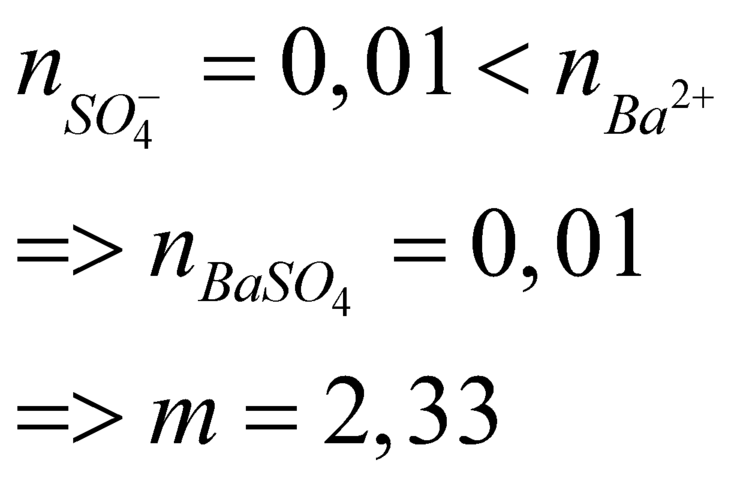

Đáp án B
Gọi số mol MgSO4 và Al2(SO4)3 lần lượt là x và y (mol) có trong 200ml dung dịch.
+ 400 ml dd X + NH3 dư => kết tủa thu được là Mg(OH)2 : 2x ( mol) và Al(OH)3: 4y (mol)
=> ∑ mkết tủa = 58.2x + 78.4y = 65,36 (1)
+ 200 ml dd X + Ba(OH)2 dư => kết tủa thu được là Mg(OH)2 : x (mol) và BaSO4 : x + 3y (mol) ( Vì Al(OH)3 tan được trong dd Ba(OH)2 dư)
=> ∑ mkết tủa = 58x + (x + 3y).233 = 151,41 (2)
Từ (1) và (2) => x = 0,16 ; y = 0,15
+ 500 ml dd X ( có 0,4 mol Mg2+, 0,75 mol Al3+) + NaOH→ 70gam kết tủa => lượng NaOH lớn nhất ứng với trường hợp tạo Mg(OH)2↓ và Al(OH)3↓ sau đó kết tủa bị hòa tan 1 phần
=> nAl(OH)3 = (70 – 0,4.58)/78 = 0,6 (mol)
Mg2+ + 2OH → 2Mg(OH)2↓
0,4 → 0,8 (mol)
Al3+ + 3OH-→ Al(OH)3↓
0,75→2,25 → 0,75 (mol)
Al(OH)3+ OH- → AlO2- + 2H2O
(0,75-0,6) → 0,15 (mol)
∑ nOH-= 0,8 + 2,25 + 0,15 = 3,2 (mol) =nNaOH
=> mNaOH = 3,2.40 = 128 (g)

Đáp án A
Có nCO32- = nHCO3- = 0,03 mol > nBa2+ = 0,02 mol (có 0,02 mol BaCO3)
⇒ dung dịch X có 0,01 mol CO32-
Và nOH- dư = 0,04 – 0,03 = 0,01 mol,
Để vừa bắt đầu xuất hiện bọt khí thì
nH+ = nOH- + n CO32- = 0,01 + 0,01 =0,02 =0,25V
V =80 ml

Đáp án B
Ta có:
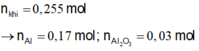
Dung dịch Y chứa 0,23 mol AlCl3.
Cho dung dịch chứa 0,3 mol Ba(OH)2 và 0,37 mol NaOH tác dụng với Y thu được dung dịch Z.
Z chứa Ba2+ 0,3 mol, Na+ 0,37 mol, AlO2- 0,23 mol, OH- dư 0,05 mol.
Cho H2SO4 vào Z.
Để kết tủa Al(OH)3 lớn nhất thì :
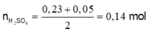
Để kết tủa BaSO4 lớn nhất thì : n H 2 S O 4 = 0 , 3 m o l
Lúc kết tủa BaSO4 tối đa thì Al(OH)3 bị hòa tan nhưng lượng BaSO4tạo thành lớn hơn Al(OH)3 bị hòa tan nên kết tủa vẫn tăng


Đáp án B
Ta có: n k h i = 0 , 255 m o l
![]()
Dung dịch Y chứa 0,23 mol AlCl3.
Cho dung dịch chứa 0,3 mol Ba(OH)2 và 0,37 mol NaOH tác dụng với Y thu được dung dịch Z.
Z chứa Ba2+ 0,3 mol, Na+ 0,37 mol, AlO2- 0,23 mol, OH- dư 0,05 mol.
Cho H2SO4 vào Z.
Để kết tủa Al(OH)3 lớn nhất thì :
n H 2 S O 4 = 0 , 23 + 0 , 05 2 = 0 , 14 m o l
Để kết tủa BaSO4 lớn nhất thì : n H 2 S O 4 = 0 , 3
Lúc kết tủa BaSO4 tối đa thì Al(OH)3 bị hòa tan nhưng lượng BaSO4tạo thành lớn hơn Al(OH)3 bị hòa tan nên kết tủa vẫn tăng
→ V = 0 , 3 2 = 150 m l

Đáp án A
Khi thêm 0,85 mol NaOH vào X thì thu được dung dịch chứa NaCl: 0,52 mol và Na2SO4 : 0,14mol;
Vì n N a O H > n N a C l + 2 n N a 2 S O 4 nên còn N a A l O 2
Bảo toàn Na có n N a O H = n N a C l + 2 n N a 2 S O 4 + n N a A l O 2 → 0 , 85 = 0 , 52 + 2 . 0 , 14 + n N a A l O 2
→ n N a A l O 2 = 0,05 mol
Kết tủa thu được là M g ( O H ) 2 : x mol và A l ( O H ) 3 : y mol
Ta có hệ sau
→ dd X có A l + 3 : 0 , 15 m o l ; M g + 2 : 0 , 15 m o l ; C l - : 0 , 52 m o l ; S O 4 2 - : 0 , 14 m o l
Ta thấy X có 3 n A l + 2 n M g < n C l + 2 n S O 4 nên X có dư H + → n H + = 0,52 + 0,14.2 -0,15.3 -0,15.2 = 0,05 mol
OH- + H + → H2O
OH- + M g + 2 → M g ( O H ) 2
3OH- + A l + 3 → A l ( O H ) 3
B a 2 + + S O 4 2 - → B a S O 4
A l ( O H ) 3 + O H - → A l O 2 - + 2 H 2 O
Khi thêm 8x mol KOH và x mol B a ( O H ) 2 vào dung dịch X thì để thu được lượng kết tủa lớn nhất ta xét các TH sau
TH1 : kết tủa có B a S O 4 : 0,14 mol và M g ( O H ) 2 : 0,15 mol và có thể có A l ( O H ) 3
Bảo toàn Ba có x = 0,14 mol → n O H =8x + 2x =10x =1,4 mol > 2 n M g + 4 n A l + n H + = 0,95
→ phản ứng có kết tủa A l ( O H ) 3 bị hòa tan hết → kết tủa thu được là B a S O 4 và M g ( O H ) 2
→ đem nung thu được B a S O 4 : 0,14 mol và MgO : 0,15 mol → m = 38,62g
TH2: Kết tủa có A l ( O H ) 3 : 0,15 mol và Mg(OH)2: 0,15 mol; B a S O 4
Ta có n O H = 10x = 0,15.3 + 0,15.2 +0,05=0,8 → x = 0,08 mol→ có 0,08 mol B a S O 4
→ Đem nhiệt phân thu được 0,08 mol B a S O 4 ; 0,075 mol Al2O3 và 0,15mol MgO
→ m = 0,08.233 + 0,075.102 +0,15.40 =32,29g
Nên TH1 khối lượng kết tủa lớn nhất là 38,62 g gần nhất với 38,6 nhất

Đáp án B
Xét NaOH +X
tạo 0,52 mol NaCl và 0,14 mol N a 2 S O 4 và dư 0,05 mol N a +
Ghép với A l O 2 - ⇒ tạo 0,05 mol N a A l O 2
Đặt n A l = x ; n M g = y
![]()
![]()
Giải hệ có: ![]()
![]()
TH1: B a S O 4 đạt cực đại
⇒ n B a ( O H ) 2 = n S O 4 = 0 , 14 m o l
⇒ n K O H = 0 , 14 . 8 = 1 , 12 m o l
Ghép tương tự NaOH, ta thấy B a 2 + , K + , S O 4 2 - , C l - còn dư 0,6 mol điện tích
Ghép với A l O 2 - ⇒ ghép được 0,15 mol
⇒ vẫn chưa đủ ⇒ còn O H - dư
Rắn gồm 0,14 mol B a S O 4 ; 0 , 15 m o l M g O ⇒ mrắn =38,62g
TH2: A l ( O H ) 3 đạt cực đại
⇒ các ion trong dung dịch gồm B a 2 + , K + , S O 4 2 - , C l -
(ta đang giả sử B a 2 + , S O 4 2 - cùng tồn tại trong cùng 1 dung dịch)
Đặt n B a 2 + = a ⇒ n K + = 8 a
Bảo toàn điện tích:
![]()
n B a S O 4 = n B a 2 + = 0 , 08 m o l
![]()
![]()
⇒ mrắn tối đa =38,62 (g)

Đáp án B
• ![]()
• Đặt số mol Mg, Al lần lượt là a, b => 24a + 27b = 7,65 g (1)
Có n NaOH = 0 , 85 > 0 , 52 + 2 . 0 , 14 = 0 , 8
=> Chứng tỏ Al(OH)3 bị hòa tan một phần: n AlO 2 - = 0 , 85 - 0 , 8 = 0 , 05 mol
⇒ m ↓ = m Mg ( OH ) 2 + m Al ( OH ) 3 = 58 a + 78 . ( b - 0 , 05 ) = 16 , 5 g (2)
• Từ (1) và (2) suy ra a = b = 0,15
• Đặt V (lít) là thể tích dung dịch kiềm thêm vào.
⇒ n B a 2 + = 0 , 1 V , n OH - = ( 0 , 8 + 2 . 0 , 1 ) V = V
P Lượng hiđroxit thu được cực đại khi: n OH - = n H + ⇒ V = 0 , 8 ( l )
Khi đó: n B a 2 + = 0 , 08 mol < n SO 4 2 - = 0 , 14 mol
⇒ m ↓ = 58 . 0 , 15 + 78 . 0 , 15 + 233 . 0 , 08 = 39 , 04 g
P Lượng BaSO4 thu được cực đại khi: n Ba 2 + = n SO 2 - = 0 , 14 mol ⇒ n OH - = 1 , 4 mol
Khi đó: n OH - > n H + + n Al ⇒ Al ( OH ) 3 tan hết
⇒ m ↓ = 58 . 0 , 15 + 233 . 0 , 14 = 41 , 32 g > 39 , 04 g
=> Lượng kết tủa đạt cực đại khi V = 1,4 lít
⇒ m ↓ = m MgO + m B a S O 4 = 40 . 0 , 15 + 233 . 0 , 14 = 38 , 62 g
Gần nhất với giá trị 38,6
nOH- = 0,04 mol
Vì nAlO2- = 0,02 mol mà chỉ thu được 0,01 mol kết tủa nên nHCl = 4n kết tủa + nAlO2- dư = 0,05 mol
=> tổng nH+ = 0,09 mol => V = 45ml
Vậy : B đúng
H+ + OH- => H2O 1
0,02......0,02
H+ + AlO2 - + H2O => Al(OH)3 2
0,02.....0,02.........................0,02
3H+ + Al(OH)3 => Al3+ +3H2O 3
0,03.........0,01
do cần V lớn nhất nên xét TH tạo kết tủa xong hòa tan 1 phần kết tủa
n Al(OH)3 =0,01 => nAl(OH)3 ở 3 =0,01
=> nHCl= 0,03 +0,02 +0,02 =0,07 => V=0,035 => C