Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

\(1.m_{CaCO_3}=400.85\%=340\left(g\right)\\ \rightarrow n_{CaCO_3}=\frac{340}{100}=3,4\left(mol\right)\\ PTHH:CaCO_3+2HCl\rightarrow CaCl_2+H_2O+CO_2\uparrow\\ V_{CO_2}=3,4.22,4=76,16\left(l\right)\\ m_{HCl}=3,4.2.36,5=248,2\left(g\right)\\ m_{CaCl_2}=3,4.111=377,4\left(g\right)\)
\(2.\\ PTHH:C+O_2\underrightarrow{t^o}CO_2\\ PTHH:S+O_2\underrightarrow{t^o}SO_2\\ n_{SO_2}=\frac{4,48}{22,4}=0,2\left(mol\right)\\ \rightarrow m_S=0,2.32=6,4\left(g\right)\\ m_C=\sum_m-m_S=10-6,4=3,6\left(g\right)\\ \%_C=\frac{3,6}{10}.100=36\left(\%\right)\\ n_C=\frac{3,6}{12}=0,3\left(mol\right)\\ \sum n_{O_2}=0,3+0,2=0,5\left(mol\right)\\ \rightarrow V_{O_2}=0,5.22,4=11,2\left(l\right)\\ \rightarrow V_{KK}=5.11,2=56\left(l\right)\\ V_{CO_2}=0,3.22,4=6,72\left(l\right)\)

1.a) n O2=\(\frac{4,5.10^{23}}{6.10^{23}}\)=0,75 (mol)
---> V O2 =0,75 . 22,4=16,8(l)
b)m O2= 0,75 . 32=24(g)
2.
m C= 1. 96%=0,96(g) --->n C=\(\frac{0,96}{12}\)=0,08(mol)
m S= 1 . 4%=0,04(g) ---> n S=\(\frac{0,04}{32}\)=0,00125(mol)
PTHH
C + O2 --t*--> CO2
0,08---> 0,08 ---->0,08 (mol)
S + O2 ---t*---> SO2
0,00125 --------> 0,00125
Tổng n O2= 0,08 + 0,00125= 0,08125 (mol)
V O2= 0,08125 . 22,4=1,82 (l)
m CO2= 0,08 . 44=3,52(g)
3) m C= 0,5 . 90%= 0,45 (g) ==> n C =\(\frac{0,45}{12}\)=0,0375(mol)
C + O2 ----> CO2
0,0375 ----> 0,0375 (mol)
V O2 = 0,0375 . 22,4=0,84 (l)
==>V kk= 5 . 0,84=4,2 (l)

\(n_{N_2}=\dfrac{3,36}{22,4}=0,15mol\)
\(n_{O_2}=\dfrac{4,48}{22,4}=0,2mol\)
\(N_2+O_2\underrightarrow{t^o}2NO\)
0,15 0,2 0
0,15 0,15 0,3
0 0,05 0,3
Sau phản ứng oxi còn dư và dư \(m=0,05\cdot32=1,6g\)
\(m_{NO}=0,3\cdot30=9g\)

a, \(4Al+3O_2\underrightarrow{t^o}2Al_2O_3\)
b, Ta có: \(n_{Al}=\dfrac{10,8}{27}=0,4\left(mol\right)\)
\(n_{O_2}=\dfrac{8,96}{22,4}=0,4\left(mol\right)\)
Xét tỉ lệ: \(\dfrac{0,4}{4}< \dfrac{0,4}{3}\), ta được O2 dư.
Theo PT: \(n_{O_2\left(pư\right)}=\dfrac{3}{4}n_{Al}=0,3\left(mol\right)\Rightarrow n_{O_2\left(dư\right)}=0,4-0,3=0,1\left(mol\right)\)
\(\Rightarrow V_{O_2\left(dư\right)}=0,1.22,4=2,24\left(l\right)\)
Lập phương trình hóa học:
Al+O2---->Al2O3
4Al+3O2---->2AlO3
Áp dụng đinh luật bảo toàn khối lượng ta có:
mAl + mO2=mAl2O3
=>mO2=mAl2O3 - mAl
=>mO2=20,4 - 10,8=9,6(g)
Số mol của 9,6g khí oxi là:
ADCT: n=m\M=>nO2=9,6\32=>nO2=0,3(mol)
n=V\22,4=>VO2=nO2 . 22,4=0,3 . 22,4=6,72(l)

a, \(4P+5O_2\underrightarrow{t^o}2P_2O_5\)
b, \(n_P=\dfrac{1,55}{31}=0,05\left(mol\right)\)
\(n_{O_2}=\dfrac{1,12}{22,4}=0,05\left(mol\right)\)
Xét tỉ lệ: \(\dfrac{0,05}{4}>\dfrac{0,05}{5}\), ta được P dư.
c, Theo PT: \(n_{P\left(pư\right)}=\dfrac{4}{5}n_{O_2}=0,04\left(mol\right)\Rightarrow n_{P\left(dư\right)}=0,05-0,04=0,01\left(mol\right)\)
\(\Rightarrow m_{P\left(dư\right)}=0,01.31=0,31\left(g\right)\)

2Zn+O2-to>2ZnO
0,1---0,05----0,1
n Zn=0,1 mol
nO2=0,025 mol
=>VO2=0,05.22,4=1,12l
=>mZnO=0,1.81=8,1g
c)Zn dư
=>m ZnO=0,05.81=4,05g
2Zn+O2-to>2ZnO
0,1---0,05----0,1
n Zn=6,5/65=0,1 mol
n O2=0,8/32=0,025 mol
=>VO2=0,05.22,4=1,12l
=>mZnO=0,1.81=8,1g
c)Zn dư
=>m ZnO=0,05.81=4,05g

a/ Ta có: \(n_{Mg}=\dfrac{4.8}{24}=0.2\left(mol\right)\)
PTHH:
\(2Mg+O_2\underrightarrow{t^o}2MgO\)
2 1
0.2 x
\(=>x=\dfrac{0.2\cdot1}{2}=0.1=n_{O_2}\)
\(=>V_{O_2\left(đktc\right)}=0.1\cdot22.4=2.24\left(l\right)\)
b/ \(2Mg+O_2\underrightarrow{t^o}2MgO\)
2 2
0.2 y
\(=>y=\left(0.2\cdot2\right):2=0.2=n_{MgO}\)
\(=>m_{MgO}=0.2\cdot\left(24+16\right)=8\left(g\right)\)

\(n_{Zn}=\dfrac{m_{Zn}}{M_{Zn}}=\dfrac{19,5}{65}=0,3mol\)
\(Zn+\dfrac{1}{2}O_2\rightarrow\left(t^o\right)ZnO\)
1 1/2 1 (mol)
0,3 0,15 0,3 ( mol )
PƯ trên thuộc loại phản ứng hóa hợp
\(m_{ZnO}=n_{ZnO}.M_{ZnO}=0,3.81=24,3g\)
\(V_{O_2}=n_{O_2}.22,4=0,15.22,4=3,36l\)

\(a) 4P+ 5O_2 \xrightarrow{t^o} 2P_2O_5\\ b) n_{O_2} = \dfrac{1,12}{22,4} = 0,05(mol)\\ n_{P_2O_5} = \dfrac{2}{5}n_{O_2} = 0,02(mol)\\ m_{P_2O_5} = 0,02.142 = 2,84(gam) c) 2KClO_3 \xrightarrow{t^o} 2KCl + 3O_2\\ n_{KClO_3} = \dfrac{2}{3}n_{O_2} = \dfrac{0,1}{3}(mol)\\ m_{KClO_3} = \dfrac{0,1}{3}122,5 = 4,083(gam)\)
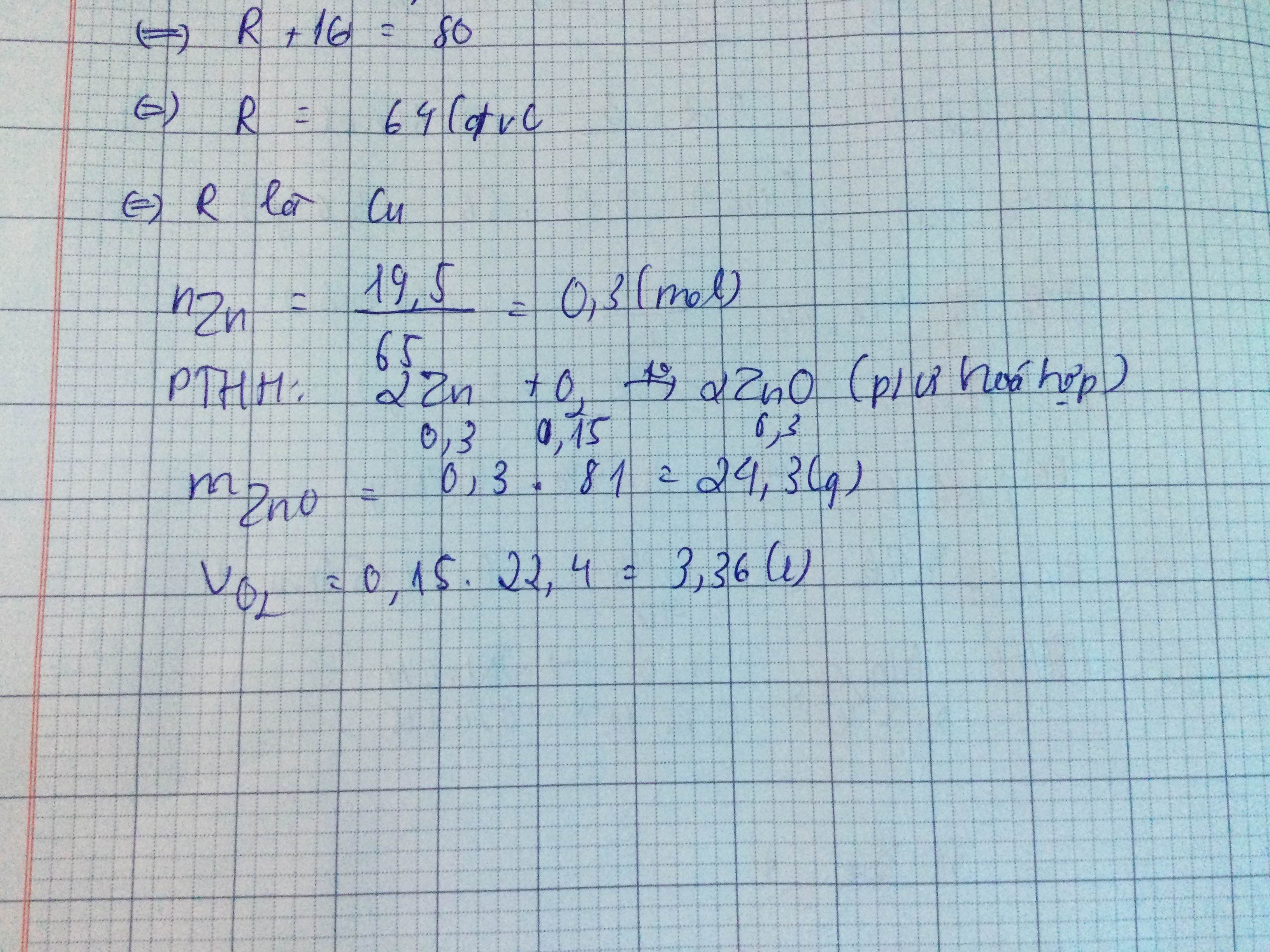
?