Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

\(n_{H_2}=\dfrac{1,12}{22,4}=0,05\left(mol\right)\)
PTHH: Fe + H2SO4 --> FeSO4 + H2
____0,05<------------------------0,05
=> mFe = 0,05.56 = 2,8 (g)
=> mCu = 6 - 2,8 = 3,2 (g)
=> D

Chọn B
Cho hỗn hợp chất rắn phản ứng với HCl dư có Cu không phản ứng.
Phương trình hóa học:
F e + 2 H C l → F e C l 2 + H 2 F e O + 2 H C l → F e C l 2 + H 2 O


\(n_{H_2}=\dfrac{1,12}{22,4}=0,05\left(mol\right)\)
PTHH: Fe + H2SO4 --> FeSO4 + H2
_____0,05<--------------------0,05
=> mFe = 0,05.56 = 2,8 (g)
=> mCu = 6-2,8 = 3,2 (g)
=> A

Có V1 < V2 => khi X tác dụng với H2O thì Al còn dư.
Giả sử số mol 3 kim loại là: x, y, z.
K + H2O → KOH + ½ H2↑
x → x 0,5x
Al + KOH + H2O → KAlO2 + 1,5H2↑
x ← x→ 1,5x
→ 0,5x + 1,5x = 0,2 → x = 0,1
X tác dụng với KOH: 0,1 . 0,5 + 1,5y = 0,35 => y = 0,2
Khi cho X tác dụng với H2O còn dư Al => Y chứa Al dư và Fe
nAl dư = nAl ban đầu – nAl phản ứng = 0,2 – 0,1 = 0,1mol
=> 0,1 . 1,5 + z = 0,4 => z = 0,25mol
=> m = 23,3g





BTKL
mX + mdd HNO3 = mdd X + mH2O + m↑
=> mdd X = 11,6 + 87,5 – 30 . 0,1 – 46 . 0,15 = 89,2g
=> C%Fe(NO3)3 = 13,565%





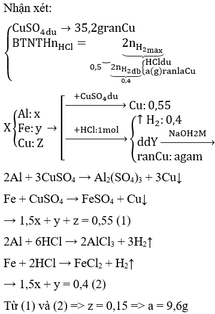

Câu 48:
\(n_{Al}=x(mol);n_{Fe}=y(mol)\\ \Rightarrow 27x+56y=11(1)\\ 2Al+6HCl\to 2AlCl_3+3H_2\\ Fe+2HCl\to FeCl_2+H_2\\ \Rightarrow 1,5x+y=\dfrac{8,96}{22,4}=0,4(2)\\ (1)(2)\Rightarrow x=0,2(mol);y=0,1(mol)\\ \Rightarrow n_{AlCl_3}=0,2(mol);n_{FeCl_2}=0,1(mol)\\ \Rightarrow m_{muối}=0,2.133,5+0,1.127=39,4(g)(B)\)
Câu 49:
\(n_{Al}=x(mol);n_{Fe}=y(mol)\\ \Rightarrow 27x+56y=4,15(1)\\ 2Al+3H_2SO_4\to Al_2(SO_4)_3+3H_2\\ Fe+H_2SO_4\to FeSO_4+H_2\\ \Rightarrow 1,5x+y=\dfrac{2,8}{22,4}=0,125(2)\\ (1)(2)\Rightarrow x=y=0,05(mol)\\ \Rightarrow \%_{Fe}=\dfrac{0,05.56}{4,15}.100\%=67,5\%\\ \Rightarrow \%_{Al}=100\%-67,5\%=32,5\%\\ \Rightarrow B\)
Câu 50:
\(Fe+H_2SO_4\to FeSO_4+H_2\\ Mg+H_2SO_4\to MgSO_4+H_2\\ FeSO_4+2NaOH\to Fe(OH)_2\downarrow+Na_2SO_4\\ MgSO_4+2NaOH\to Mg(OH)_2\downarrow+Na_2SO_4\\ 4Fe(OH)_2+O_2\xrightarrow{t^o}2Fe_2O_3+4H_2O\\ Mg(OH)_2\xrightarrow{t^o}MgO+H_2O\\ \Rightarrow n_{Fe_2O_3}=\dfrac{1}{2}n_{Fe}=\dfrac{11,2}{56}=0,1(mol)\\ n_{MgO}=n_{Mg}=\dfrac{2,4}{24}=0,1(mol)\\ \Rightarrow \Sigma m_{\text{chất rắn}}=0,1.160+0,1.40=20(g)\)
Chọn B