
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


nFe = 16,8\56 = 0,3(mol)
mO trong sắt oxit là: 23,2 - 16,8 = 6,4(g) => nO = 6,4\16 = 0,4(mol)
Đặt CT dạng chung là FexOy (x,y∈∈N*)
=> x:y = nFe:nO = 0,3:0,4 = 3:4
Vậy CTHH là Fe3O4


Câu 1 : $n_{Na} = \dfrac{m}{M} = \dfrac{2,3}{23} = 0,1(mol)$
Câu 2 : $V_{O_2} = n.22,4 = 0,05.22,4 = 1,12(lít)$
Câu 3 : $d_{SO_2/H_2} = \dfrac{64}{2} = 32 > 1$
Vậy khí $SO_2$ nặng hơn $H_2$ 32 lần


\(Cu\left(OH\right)_2+2HNO_3\rightarrow Cu\left(NO_3\right)_2+2H_2O\\ MgO+2HCl\rightarrow MgCl_2+H_2O\\ Fe\left(OH\right)_3+3HCl\rightarrow FeCl_3+3H_2O\\ Fe_2\left(SO_4\right)_3+3BaCl_2\rightarrow3BaSO_4\downarrow+2FeCl_3\)

\(a,2KMnO_4\rightarrow\left(t^o\right)K_2MnO_2+MnO_2+O_2\\ b,n_{KMnO_4}=\dfrac{31,6}{158}=0,2\left(mol\right)\\ \Rightarrow n_{O_2}=\dfrac{0,2}{2}=0,1\left(mol\right)\\ \Rightarrow V_{O_2\left(đktc\right)}=0,1.22,4=2,24\left(l\right)\\ c,n_{Fe}=\dfrac{11,2}{56}=0,2\left(mol\right)\\ 3Fe+2O_2\rightarrow\left(t^o\right)Fe_3O_4\\ Vì:\dfrac{0,2}{3}< \dfrac{0,1}{2}\Rightarrow Fedư\\ \Rightarrow n_{Fe_3O_4}=n_{O_2}:2=0,1 :2=0,05\left(mol\right)\\ \Rightarrow m_{Fe_3O_4}=232.0,05=11,6\left(g\right)\)

Bài 2 : (1) liên kết ; (2) electron ; (3) liên kết ; (4) : electron ; (5) sắp xếp electron
Bài 4 :
$\dfrac{M_X}{4} = \dfrac{M_K}{3} \Rightarrow M_X = 52$
Vậy X là crom,KHHH : Cr
Bài 5 :
$M_X = 3,5M_O = 3,5.16 = 56$ đvC
Tên : Sắt
KHHH : Fe
Bài 9 :
$M_Z = \dfrac{5,312.10^{-23}}{1,66.10^{-24}} = 32(đvC)$
Vậy Z là lưu huỳnh, KHHH : S
Bài 10 :
a) $PTK = 22M_{H_2} = 22.2 = 44(đvC)$
b) $M_{hợp\ chất} = X + 16.2 = 44 \Rightarrow X = 12$
Vậy X là cacbon, KHHH : C
Bài 11 :
a) $PTK = 32.5 = 160(đvC)$
b) $M_{hợp\ chất} = 2A + 16.3 = 160 \Rightarrow A = 56$
Vậy A là sắt
c) $\%Fe = \dfrac{56.2}{160}.100\% = 70\%$

\(n_{K_2SO_3}=\dfrac{39,5}{158}=0,25\left(mol\right)\) ; \(n_{HCl}=\dfrac{14,6}{36,5}=0,4\left(mol\right)\)
\(K_2SO_3+HCl\rightarrow KCl+H_2O+SO_2\)
\(0,25\) \(0,4\)
→ HCl dư
\(K_2SO_3+HCl\rightarrow KCl+H_2O+SO_2\)
\(0,25\rightarrow0,25\rightarrow0,25\rightarrow0,25\rightarrow0,25\)
a) m dư = m K2SO3 = 0,25 . 158 = 39,5 (g)
b) m KCl = 0,25 . 74,5 = 18,625 (g)
c) V SO2 = 0,25 . 22,4 = 5,6 (lít)

a) \(m_O=\dfrac{20.20}{100}=4\left(g\right)\)
=> \(n_{CaO}=n_O=\dfrac{4}{16}=0,25\left(mol\right)\)
\(\left\{{}\begin{matrix}\%m_{CaO}=\dfrac{0,25.56}{20}.100\%=70\%\\\%m_{Ca}=100\%-70\%=30\%\end{matrix}\right.\)
b) \(n_{Ca}=\dfrac{20.30\%}{40}=0,15\left(mol\right)\)
PTHH: Ca+ 2H2O --> Ca(OH)2 + H2
0,15-------------------->0,15
=> V = 0,15.22,4 = 3,36 (l)
\(n_{Fe_3O_4}=\dfrac{23,2}{232}=0,1\left(mol\right)\)
=> nFe = 0,3 (mol)
=> mFe = 0,3.56 = 16,8 (g)
=> \(m=\dfrac{16,8.100}{78,9474}=21,28\left(g\right)\)
c) Giả sử Fe3O4 bị khử thành Fe
Gọi số mol Fe3O4 pư là a (mol)
PTHH: Fe3O4 + 4H2 --> 3Fe + 4H2O
a--->4a----->3a
Xét tỉ lệ: \(\dfrac{0,1}{1}>\dfrac{0,15}{4}\) => Hiệu suất tính theo H2
m = 23,2 - 232a + 168a = 21,28
=> a = 0,03 (mol)
=> \(\left\{{}\begin{matrix}n_{Fe_3O_4\left(pư\right)}=0,03\left(mol\right)\\n_{H_2\left(pư\right)}=0,12\left(mol\right)\end{matrix}\right.\)
\(H=\dfrac{n_{H_2\left(pư\right)}}{n_{H_2\left(bđ\right)}}=\dfrac{0,12}{0,15}.100\%=80\%\)
 Câu 3 ạ
Câu 3 ạ






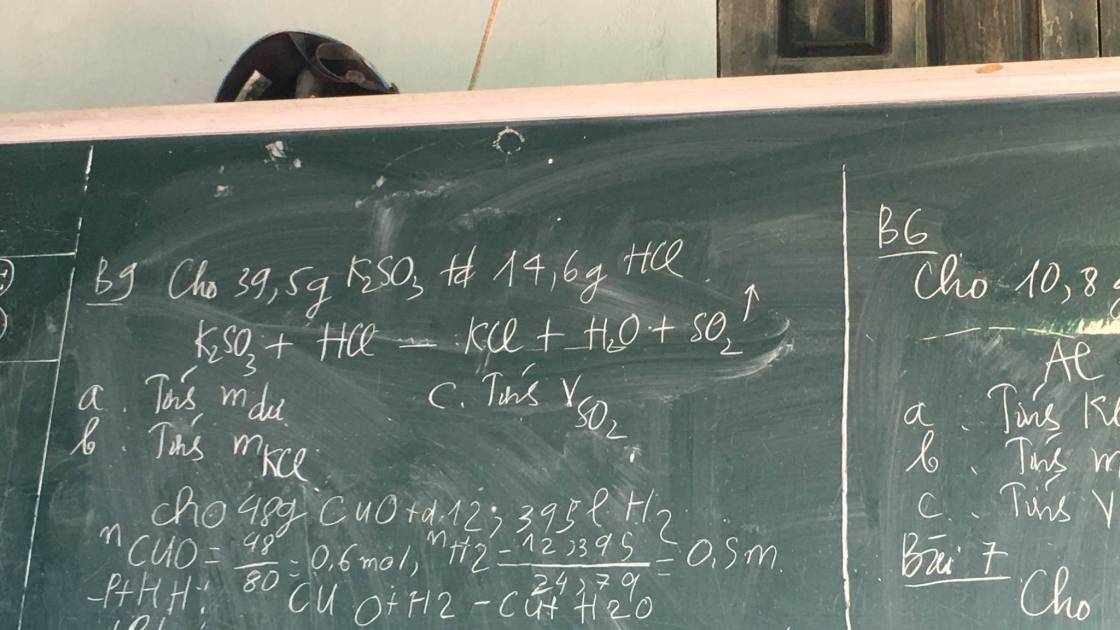

3Fe+2O2-to>Fe3O4
0,45----0,3-----------0,15
n Fe=28\56=0,5 mol
n Fe3O4=34,8\232=0,15 mol
=>m Fe pứ =0,45.56=25,2g
=>m Fe dư = 28 -25,2=2,8g
=>VO2=0,3.22,4=6,72l
( đây là dạng hóa cơ bản em nên tập làm nhé )
à e nhầm