Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án A
Cách 1: Theo giả thiết ta có:
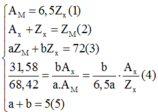
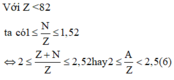
Từ (4) và (6) ta suy ra: 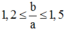
Chỉ có cặp a = 2 và b = 3 thỏa mãn
hợp chất là MaXb là M2X3
Thay vào ngược lại ta có:
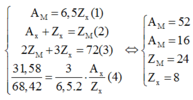
=> Hợp chất cần tìm là Cr2O3
Cách 2: X chiếm 31,58% về khối lượng:
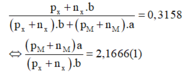
Theo giải thiết ta có
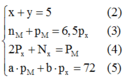
Quan sát – phân tích: Để tìm câu trả lời cho bài toán ta chỉ cần xác định được 4 ẩn x ; y; pM; pR. Vì vậy ta sẽ tìm cách khử các ẩn không cần thiết bằng cách thế phương trình (3) và (4) phương trình (1):
Thế (3) và (4) vào phương trình (1) ta được:
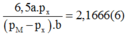
Phương án 1: Biện luận nghiệm theo giá trị của a và b:
Ta còn lại 3 phương trình với 4 ẩn số
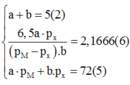
Nhận xét: Ở phương trình (6) chứa ẩn apX và bpM nhưng phương trình 5 lại không chứa 2 ẩn đó. Vì vậy ta không thể đưa ba phương trình trên về phương trình hai ẩn để biện luận. Điều duy nhất chúng ta có thể làm là phải biện luận cùng lúc 2 giá trị của a và b
Vậy M là Crom và X là Oxi.
Phương án 2:
Biện luận tìm giá trị của a và b từ đó tìm M và X.
Từ phương trình (4) ta có
![]()
Mặt khác ta có với một nguyên tố có Z < 82 ta có:
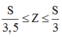
![]()
Từ (6); (7) và (8) ta suy ra: ![]()
=> chỉ có a = 2 và b = 3 là thỏa mãn
Ta tìm được M là Crom và X là Oxi.
Vậy hợp chất cần tìm là Cr2O3.
=> Tổng số hạt cơ bản là 224
Nhận xét: Đây là một trong những bài tập khó đòi hỏi tư duy và kĩ năng tính toán cao nhưng đối với những bạn có nhiều kinh nghiệm thì với bài tập này hoàn toàn có thể đoán được. Khi đề cho a + b = 5 thì với kinh nghiệm tích lũy trong quá trình học thì chúng ta sẽ đoán cặp số ở đây sẽ là 2 và 3 hợp chất đó sẽ là M2X3 thông thường thì đây sẽ là oxit của kim loại hóa trị 3 thay ngay Oxi vào tìm ra được M một cách nhanh chóng. Vì vậy kinh nghiệm đoán và bắt bài là một trong những kĩ năng rất cần thiết giúp ta giải quyết nhanh những bài toán hóa học khó.

Đáp án A
Cách 1: Theo giả thiết ta có:
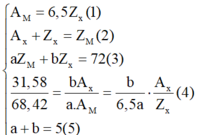
Với Z <82 ta có
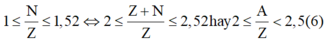
Từ (4) và (6) ta suy ra:
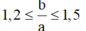
Chỉ có cặp a = 2 và b = 3 thỏa mãn
⇒ hợp chất là MaXb là M2X3
Thay vào ngược lại ta có:
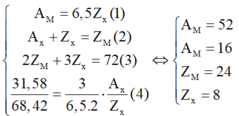
⇒ Hợp chất cần tìm là Cr2O3
Cách 2: X chiếm 31,58% về khối lượng:
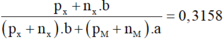
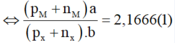
Theo giải thiết ta có
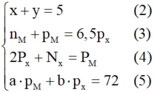
Quan sát – phân tích: Để tìm câu trả lời cho bài toán ta chỉ cần xác định được 4 ẩn x ; y; pM; pR. Vì vậy ta sẽ tìm cách khử các ẩn không cần thiết bằng cách thế phương trình (3) và (4) phương trình (1):
Thế (3) và (4) vào phương trình (1) ta được:
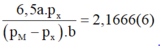
Phương án 1: Biện luận nghiệm theo giá trị của a và b:
Ta còn lại 3 phương trình với 4 ẩn số
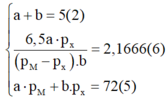
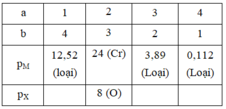
Nhận xét: Ở phương trình (6) chứa ẩn apX và bpM nhưng phương trình 5 lại không chứa 2 ẩn đó. Vì vậy ta không thể đưa ba phương trình trên về phương trình hai ẩn để biện luận. Điều duy nhất chúng ta có thể làm là phải biện luận cùng lúc 2 giá trị của a và b
| a |
1 |
2 |
3 |
4 |
| b |
4 |
3 |
2 |
1 |
| pM |
12,52 (loại) |
24 (Cr) |
3,89 (Loại) |
0,112 (Loại) |
| pX |
|
8 (O) |
|
|
Vậy M là Crom và X là Oxi.
Phương án 2:
Biện luận tìm giá trị của a và b từ đó tìm M và X.
Từ phương trình (4) ta có
![]()
Mặt khác ta có với một nguyên tố có Z < 82 ta có:
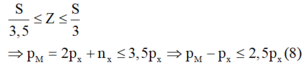
Từ (6); (7) và (8) ta suy ra:
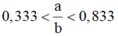
⇒ chỉ có a = 2 và b = 3 là thỏa mãn
Ta tìm được M là Crom và X là Oxi.
Vậy hợp chất cần tìm là Cr2O3.
⇒ Tổng số hạt cơ bản là 224
Nhận xét: Đây là một trong những bài tập khó đòi hỏi tư duy và kĩ năng tính toán cao nhưng đối với những bạn có nhiều kinh nghiệm thì với bài tập này hoàn toàn có thể đoán được. Khi đề cho a + b = 5 thì với kinh nghiệm tích lũy trong quá trình học thì chúng ta sẽ đoán cặp số ở đây sẽ là 2 và 3 ⇒ hợp chất đó sẽ là M2X3 thông thường thì đây sẽ là oxit của kim loại hóa trị 3 thay ngay Oxi vào tìm ra được M một cách nhanh chóng. Vì vậy kinh nghiệm đoán và bắt bài là một trong những kĩ năng rất cần thiết giúp ta giải quyết nhanh những bài toán hóa học khó.

3. Khối lượng mol của hợp chất đó là :
2.28 = 56 (g/mol)
mC = \(\frac{56.85,7}{100}\approx48\left(g\right)\)
mH = 56 - 48 = 8 (g)
nC = \(\frac{48}{12}=4\left(mol\right)\)
nH = \(\frac{8}{1}=8\left(mol\right)\)
Vậy công thức hóa học là C4H8.

a) Vì 2 nguyên tố có tổng số proton là 32
=> 2 nguyên tố thuộc chu kì nhỏ
Gọi 2 nguyên tố cần tìm trong A là X, Y
Vì hợp chất A tạo bởi 3 nguyên tử của 2 nguyên tố thuộc cùng 1 nhóm, ở 2 chu kì liên tiếp => CT của A : XY2
Ta có : \(\left\{{}\begin{matrix}Z_X+2Z_Y=32\\\left|Z_X-Z_Y\right|=8\end{matrix}\right.\)
=> \(\left\{{}\begin{matrix}Z_X=16\left(S\right)\\Z_Y=8\left(O\right)\end{matrix}\right.\)
=> CTPT của hợp chất : SO2
CT cấu tạo :
SO2 là liên kết cộng hóa trị có cực
b) Lưu huỳnh đioxit (SO2) mang đầy đủ tính chất hóa học của một oxit axit.
Tính chất hóa học của SO2:
- Tác dụng với nước tạo thành dung dịch axit.
Ví dụ: SO2 + H2O → H2SO3
- Tác dụng với dung dịch bazơ tạo thành muối và nước.
Ví dụ: SO2 + 2NaOH → Na2SO3 + H2O
- Tác dụng với oxit bazơ tạo thành muối.
Ví dụ: SO2 + Na2O → Na2SO3
Bài 6:
1. Fe2(SO4)3
- sắt III sunfat được cấu tạo từ 3 nguyên tố: Fe, S và O
- 1 phân tử sắt III sunfat gồm: 2 nguyên tố Fe, 3 nguyên tố S và 12 nguyên tố O
- \(PTK_{Fe_2\left(SO_4\right)_3}=56\times2+3\times\left(32+16\times4\right)=400\left(đvC\right)\)
2. Fe(NO3)2
- sắt II nitrat được cấu tạo từ 3 nguyên tố: Fe, N, và O
-1 phân tử sắt II nitrat gồm: 1 nguyên tử Fe, 2 nguyên tử N và 6 nguyên tử O
- \(PTK_{Fe\left(NO_3\right)_2}=56+2\times\left(14+16\times3\right)=180\left(đvC\right)\)
3. Zn(NO3)2
- kẽm nitrat được cấu tạo từ 3 nguyên tô: Zn, N và O
- 1 phân tử kẽm nitrat gồm: 1 nguyên tử Zn, 2 nguyên tử N và 6 nguyên tử O
- \(PTK_{Zn\left(NO_3\right)_2}=65+2\times\left(14+16\times3\right)=189\left(đvC\right)\)
4. CaCO3
- canxi cacbonat được cấu tạo từ 3 nguyên tố: Ca, C và O
- 1 phân tử canxi cacbonat gồm: 1 nguyen tử Ca, 1 nguyên tử C và 3 nguyên tử O
- \(PTK_{CaCO_3}=40+12+16\times3=100\left(đvC\right)\)
5. Al2(SO4)3
- nhôm sunfat được cấu tạo từ 3 nguyên tố: Al, S và O
- 1 phân tử nhôm sufat gồm: 2 nguyên tử Al, 3 nguyên tử S và 12 nguyên tử O
- \(PTK_{Al_2\left(SO_4\right)_3}=27\times2+3\times\left(32+16\times4\right)=342\left(đvC\right)\)
6. Mg(HCO3)2
- magie hydro cacbonat được cấu tạo từ 4 nguyên tố: Mg, H, C và O
- 1 phân tử magie hydro cacbonat gồm: 1 nguyên tử Mg, 2 nguyên tử H, 2 nguyên tử C và 6 nguyên tử O
- \(PTK_{Mg\left(HCO_3\right)_2}=24+2\times\left(1+12+16\times3\right)=146\left(đvC\right)\)
bài tương đối dài