Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

a.\(n_{H_2}=\dfrac{6,72}{22,4}=0,3mol\)
\(Fe+2HCl\rightarrow FeCl_2+H_2\)
0,3 0,3 ( mol )
\(m_{Fe}=0,3.56=16,8g\)
\(\%m_{Fe}=\dfrac{16,8}{20}.100=84\%\)
\(\%m_{Cu}=100\%-84\%=16\%\)
b.\(m_{Cu}=20-16,8=3,2g\)
\(n_{Cu}=\dfrac{3,2}{64}=0,05mol\)
\(CuO+H_2\rightarrow\left(t^o\right)Cu+H_2O\)
0,05 0,05 ( mol )
\(m_{CuO}=0,05.80=4g\)
\(n_{H_2}=\dfrac{6,72}{22,4}=0,3\left(mol\right)\\ PTHH:Fe+2HCl\rightarrow FeCl_2+H_2\uparrow\\ Theo.pt:n_{Fe}=n_{H_2}=0,3\left(mol\right)\\ m_{Fe}=0,3.56=16,8\left(g\right)\\ m_{Cu}=20-16,8=3,2\left(g\right)\\ n_{Cu}=\dfrac{3,2}{64}=0,06\left(mol\right)\\ PTHH:CuO+H_2\underrightarrow{t^o}Cu+H_2O\\ Mol:0,05\leftarrow0,05\leftarrow0,05\\ m_{CuO}=0,05.80=4\left(g\right)\)

Đặt XO là các oxit (giả sử X hóa trị II)
\(nO\left(oxit\right)=n_{XO}=\dfrac{40-32}{16}=0,5\left(mol\right)\)
\(H_2SO_4\left(0,5\right)+XO\left(0,5\right)\rightarrow XSO_4+H_2O\)
\(\Rightarrow V_{H_2SO_4}=0,25\left(l\right)=250\left(ml\right)\)
Ta thấy muối là phân tử mà trong đó gồm 1 hay nhiều nguyên tử kim loại liên kết với gốc axit \(\left(SO_4^{2-}\right)\). mÀ trong quá trình phản ứng SO4(2-) trong phân tử H2SO4 chuyển về muối hết => nSO4(2-) trong muối = nH2SO4 = 0,5 (mol)
\(m_{muoi}=m_{KL}+m_{SO_4^{2-}}=32+0,5.96=80\left(g\right)\)

2Al + 3H2SO4 →Al2(SO4)3 + 3H2 (1)
Zn + H2SO4 →ZnSO4 + H2 (2)
a;nH2=\(\dfrac{8,96}{22,4}\)=0,4(mol)
Đặt nAl=a
nZn=b
Ta có:
\(\left\{{}\begin{matrix}27x+65y=11,9\\1,5x+y=0,4\end{matrix}\right.\)
=>a=0,2;b=0,1
mAl=27.0,2=5,4(g)
%mAl=\(\dfrac{5,4}{11,9}.100\)=54,4%
%mZn=54,6%
Ta có kim loại + H2SO4 → muối + H2
nH2 = 0,4 mol
Bảo toàn nguyên tố H có nH2 = nH2SO4 = 0,4 mol
Bảo toàn khối lượng có mkim loại + mH2SO4 = mH2 + mmuối → 11,9 + 0,4.98 = 0,4.2 + m → m = 50,3

Phần 1 :
$m_{Cu} = 0,4(gam)$
Gọi $n_{Fe} = a ; n_{Al} = b \Rightarrow 56a + 27b + 0,4 = 1,5 : 2 = 0,75(1)$
$Fe + 2HCl \to FeCl_2 + H_2$
$2Al + 6HCl \to 2AlCl_3 + 3H_2$
$n_{H_2} = a + 1,5b = \dfrac{896}{1000.22,4} = 0,04(2)$
Từ (1)(2) suy ra a = -0,025 < 0$
$\to$ Sai đề

Ta có: mCu = 1,86 (g)
PT: \(2Al+6HCl\rightarrow2AlCl_3+3H_2\)
\(Fe+2HCl\rightarrow FeCl_2+H_2\)
Có: mAl + mFe = 6 - 1,86 = 4,14 (g)
Giả sử: \(\left\{{}\begin{matrix}n_{Al}=x\left(mol\right)\\n_{Fe}=y\left(mol\right)\end{matrix}\right.\)
⇒ 27x + 56y = 4,14 (1)
Ta có: \(n_{H_2}=\dfrac{3,024}{22,4}=0,135\left(mol\right)\)
Theo PT: \(n_{H_2}=\dfrac{3}{2}n_{Al}+n_{Fe}=\dfrac{3}{2}x+y\left(mol\right)\)
\(\Rightarrow\dfrac{3}{2}x+y=0,135\left(2\right)\)
Từ (1) và (2) \(\Rightarrow\left\{{}\begin{matrix}x=0,06\left(mol\right)\\y=0,045\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}\%m_{Cu}=\dfrac{1,86}{6}.100\%=31\%\\\%m_{Al}=\dfrac{0,06.27}{6}.100\%=27\%\\\%m_{Fe}=42\text{%}\end{matrix}\right.\)
Bạn tham khảo nhé!
Chất rắn không tan sau phản ứng là Cu
=> m Cu = 1,86(gam)
Gọi n Al =a (mol) ; n Fe = b(mol) => 27a + 56b = 6 -1,86 = 4,14(1)
$2Al + 6HCl \to 2AlCl_3 + 3H_2$
$Fe + 2HCl \to FeCl_2 + H_2$
n H2 = 1,5a + b = 3,024/22,4 = 0,135(2)
Từ (1)(2) suy ra a = 0,06 ; b = 0,045
Vậy :
%m Cu = 1,86/6 .100% = 31%
%m Al = 0,06.27/6 .100% = 27%
%m Fe = 100% -31% -27% = 42%

PTHH:
\(CuO+H_2\) \(\underrightarrow{t^o}\) \(Cu+H_2O\) \(\left(1\right)\)
\(Fe_2O_3+3H_2\) \(\underrightarrow{t^o}\) \(2Fe+3H_2O\) \(\left(2\right)\)
Số mol H2 là 0,6 mol
Gọi số mol H2 tham gia pư 1 là x mol \(\left(0,6>x>0\right)\)
Số mol H2 tham gia pư 2 là \(\left(0,6-x\right)mol\)
Theo PTHH 1:
\(n_{CuO}=n_{H_2}=x\left(mol\right)\)
Theo PTHH 2:
\(n_{Fe_2O_3}=\frac{1}{3}n_{H_2}=\left(0,6-x\right):3\left(mol\right)\)
Theo bài khối lượng hh là 40g
Ta có pt: \(80x+\left(0,6-x\right)160:3=40\)
Giải pt ta được \(x=0,3\)
Vậy \(n_{CuO}=0,3\left(mol\right);n_{Fe_2O_3}=0,1\left(mol\right)\)
\(\%m_{CuO}=\left(0,3.80.100\right):40=60\%\)
\(\%m_{Fe_2O_3}=\left(0,1.160.100\right):40=40\%\)
1)
PTHH: \(2Cu+O_2\) \(\underrightarrow{t^o}\) \(2CuO\)
x x
Gọi số mol Cu phản ứng là x mol ( x >0)
Chất rắn X gồm CuO và Cu
Ta có PT: 80x + 25,6 – 64x = 28,8
Giải PT ta được x = 0,2
Vậy khối lượng các chất trong X là:
\(m_{Cu}\) = 12,8 gam
\(m_{CuO}\) = 16 gam
2)
Gọi kim loại hoá trị II là A.
PTHH: \(A+2HCl\rightarrow ACl_2+H_2\)
Số mol \(H_2\)= 0,1 mol
Theo PTHH: \(n_A=n_{H_2}\)= 0,1 (mol)
Theo bài \(m_A\) = 2,4 gam \(\Rightarrow\) \(M_A\) = 2,4 : 0,1 = 24 gam
Vậy kim loại hoá trị II là Mg

Bài 7.4:
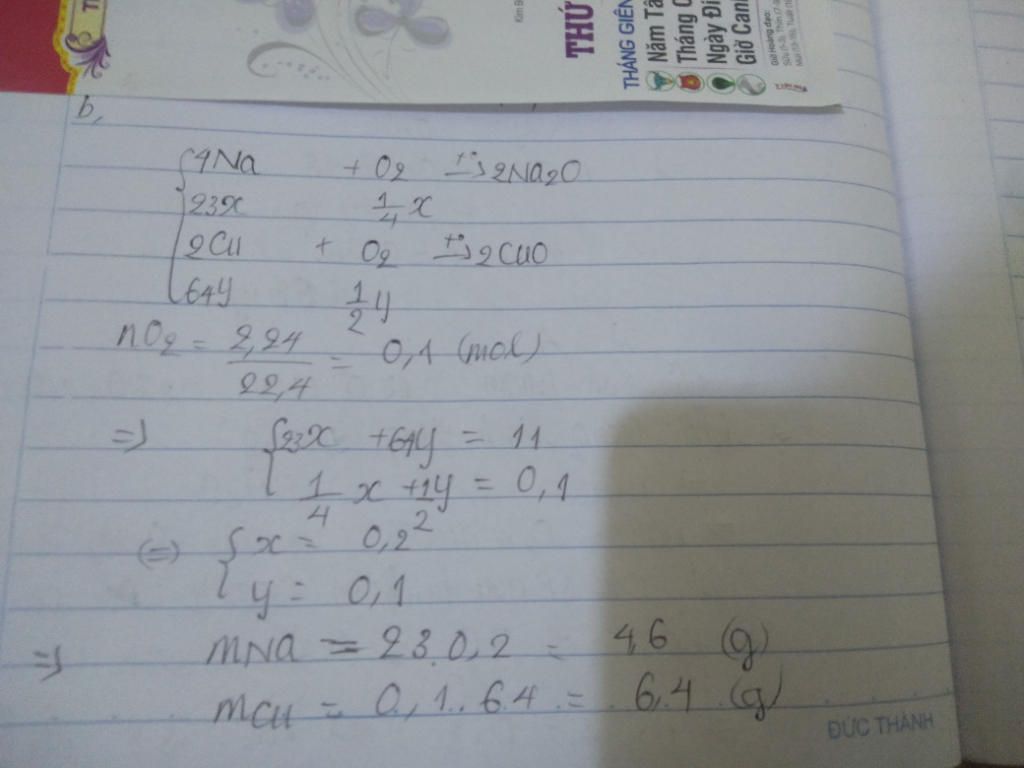
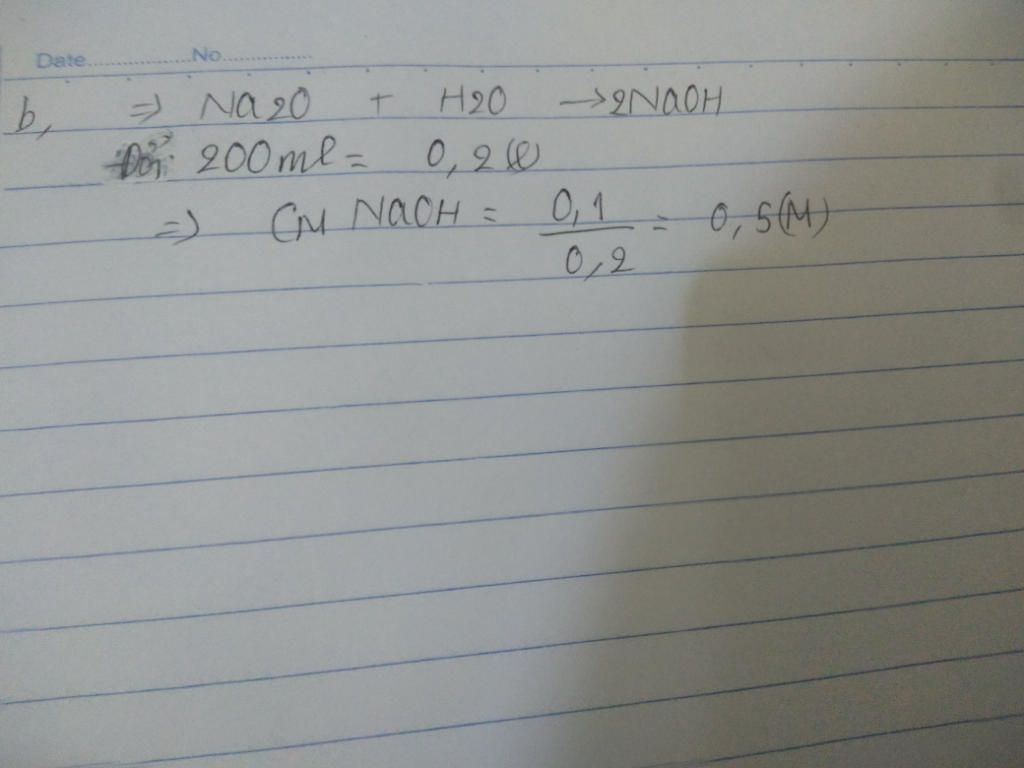
a) Fe + H 2 SO 4 → FeSO 4 + H 2
Mg + H 2 SO 4 → MgSO 4 + H 2
2Cu + O2 -----to------>2 CuO
\(n_{Cu}=n_{CuO}=\dfrac{5}{80}=0,0625\left(mol\right)\)
Gọi x, y lần lượt là số mol Fe,Mg
\(\left\{{}\begin{matrix}56x+24y=20-0,0625.64\\x+y=\dfrac{8,96}{22,4}=0,4\left(mol\right)\end{matrix}\right.\)
=> x= 0,2; y=0,2
\(\%m_{Fe}=\dfrac{0,2.56}{20}.100=56\%\)
\(\%m_{Mg}=\dfrac{24.0,2}{20}.100=24\%\)
\(\%m_{Cu}=\dfrac{0,0625.64}{20}.100=20\%\)
\(Mg+\dfrac{1}{2}O_2\rightarrow MgO\)
\(Cu+\dfrac{1}{2}O_2\rightarrow CuO\)
\(3Fe+2O_2\rightarrow Fe_3O_4\)
\(n_{O_2}=0,2.\dfrac{1}{2}+0,0625.\dfrac{1}{2}+0,2.\dfrac{2}{3}=\dfrac{127}{480}\left(mol\right)\)
Trong không khí chứa khoảng 20% khí oxi
=>Vkk= \(\dfrac{127}{480}.\dfrac{100}{20}.22,4=29,63\left(l\right)\)