Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.



Qui đổi ½ hh B gồm Al (x mol), Fe (y mol), O (z mol)

=> mB = 2 (mAl + mFe + mO) = 102,78g
Gọi công thức của oxit sắt là FeaOb

=> Fe2O3

Câu 1
a)
Khí sinh ra là CO2 :
CO+ O→CO2
nBa(OH)2= 0,1 mol
\(n_{BaCO3}=\frac{9,85}{197}=0,05\left(mol\right)\)
Ta có 2 trường hợp:
TH1: Tạo 1 muối trung hòa
Ba(OH)2+ CO2→ BaCO3↓+H2O
_________0,05____0,05
⇒nCO2= 0,05 ⇒nO(FexOy)= 0,05 (1)
TH2: Tạo 2 muối
Ba(OH)2+ CO2→ BaCO3↓+H2O
0,1_____0,1______0,1
CO2+ BaCO3+H2O→ Ba(HCO3)2
0,05___0,05
⇒nCO2= 0,1+0,05= 0,15 mol ⇒nO(FexOy)= 0,15 (2)
PTHH:
Fe+ 2HCl→ FeCl2+H2↑
\(n_{FeCl2}=\frac{12,7}{127}=0,1\left(mol\right)\)
⇒ nFe= 0,1 mol
Vậy với nO= 0.05; nFe= 0,1⇒ x : y= 2:1 (loại)
với nO=0,15; nFe= 0,1⇒ x: y= 2:3 hay CTHC: Fe2O3
b)
m= 0,1.56+0,15.16=8 g
\(V=\frac{0,1.120}{2.100}=0,06l=60l\)
Câu 2:
nCO2= nBaCO3= \(\frac{27,58}{197}\)= 0,14 mol
CO+ O= CO2
\(\rightarrow\) nO (oxit)= nCO2= 0,14 mol
\(\rightarrow\)mO= 0,14.16= 2,24g
Coi oxit kim loại M gồm M và O
\(\rightarrow\) mM= 8,12-2,24= 5,88g
2M+ 2xHCl\(\rightarrow\) 2MClx+ xH2
nH2=\(\frac{2,352}{22,4}\)= 0,105 mol
\(\rightarrow\) nM= \(\frac{0,21}{x}\) mol
\(\rightarrow\)MM= \(\frac{5,88x}{0,21}\)= 28x
x=2 \(\rightarrow\) M=56. Vậy M là sắt (Fe)
FexOy+ yCO\(\underrightarrow{^{to}}\) xFe+ yCO2
nCO2= 0,14 mol \(\rightarrow\)nFexOy= 0,14/y mol
\(\rightarrow\)M FexOy= \(\frac{8,12y}{0,14}\)= 58y
Ta có pt: 56x+16y=58y
\(\Leftrightarrow\) 56x-42y=0
x=3\(\rightarrow\) y=4. Vậy CTHH oxit sắt laf Fe3O4

Dung dịch Ca(OH)2 không hấp thụ khí CO nên 6,72 lít khí thoát ra chính là khí CO dư.


m rắn giảm = mO (oxit) => nO (oxit) = (1,6 – 1,408) : 16 = 0,012mol
Dễ thấy n = nO (oxit) = 0,012mol
=> nH2 ban đầu = 0,012 : 80% = 0,015
=> nFe = nH2= 0,015 → x = 0,015
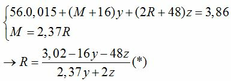
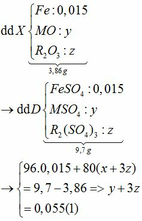
Ta có: CO + O(Oxit) → CO2
Vì: m(Rắn giảm) = mO(Oxit) → nO(Oxit) = (3,86 – 3,46) : 16 = 0,025
TH1: cả 2 oxit đều bị khử bởi CO
→ nO(Oxit) = y + 3z = 0,025 kết hợp với (1) loại
TH2: chỉ có MO bị khử bởi CO
→ nO(Oxit) = nMO = 0,025 → y = 0,025 kết hợp với (1) => z = 0,01
Kết hợp với (*) => M = 64 (Cu)
TH3: chỉ có R2O3 bị khử bởi CO
→ nO(Oxit) = 3.nR2O3 → z = 0,025/3 kết hợp với (1) => y = 0,03
Kết hợp với (*) y => M lẻ => loại
Vậy %m các chất trong X là: 21,76%; 51,81%; 26,43%

3. CuO +H2SO4 -->CuSO4 +H2O
nCuO=64/80=0,8(mol)
theo PTHH :nCuO =nH2SO4=nCuSO4=0,8(mol)
=>mddH2SO4 20%=0,8.98.100/20=392(g)
mCuSO4=0,8.160=128(g)
mdd sau phản ứng =64 +392=456(g)
mH2O=456 -128=328(g)
giả sử có a g CuSO4.5H2O tách ra
trong 250g CuSO4 tách ra có 160g CuSO4 và 90g H2O tách ra
=> trong a g CuSO4.5H2O tách ra có : 160a/250 g CuSO4 và 90a/250 g H2O tách ra
=>mCuSO4(còn lại)=128 -160a/250 (g)
mH2O (còn lại)=328 -90a/250 (g)
=>\(\dfrac{128-\dfrac{160a}{250}}{328-\dfrac{90a}{250}}.100=25\)
=>a=83,63(g)
Bài 1 :
Theo đề bài ta có : nHCl = 2.0,06 = 0,12 (mol)
Ta có PTHH :
\(\left(1\right)2Fe\left(OH\right)3-^{t0}->Fe2O3+3H2O\)
\(\left(2\right)Fe2O3+6HCl->2FeCl3+3H2O\)
0,02mol............0,06mol
m(cr) thu được sau khi nung là : mFe2O3 = 0,02.160 = 3,2(g)
Ta có :
(m - 0,81) = 3,2 <=> m = 3,2+ 0,81 = 4,01(g)
Theo PTHH 1 ta có : nFe(OH)3 = 2nFe2O3 = 0,04 (mol)
Hiệu suất phản ứng nung Fe(OH)3 là :
H = \(\dfrac{m\left(th\text{ực}-t\text{ế}\right)}{m\left(l\text{ý}-thuy\text{ết}\right)}.100\%=\dfrac{4,01}{0,04.107}.100\%\approx93,69\%\)
Tham khảo ở đây : index