Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

2 khí không màu, không hóa nâu trong không khí và là sản phẩm khử của N+5 chỉ có thể là N2 và N2O
-TH1: 21,19 gam muối không có muối NH4NO3
Theo bảo toàn nguyên tố M ta có: nM= nM(NO3)2
→ m M m M ( N O 3 ) 2 = M M M M ( N O 3 ) 2 → 7 , 15 21 , 19 = M M + 62 , 2
→M= 63,148 Loại
Do đó trường hợp này loại
-TH2: 21,19 gam muối có muối NH4NO3
QT cho e:
M → M2++ ne (1)
7,15/M 7,15.2/M
QT nhận e : nkhí= 0,02 mol. Mà số mol hai khí bằng nhau nên n N 2 O = n N 2 =0,01mol
2NO3-+ 8e+ 10H+ → N2O + 5H2O (2)
0,08 0,1 ← 0,01 mol
2NO3-+ 10e+12H+→ N2+ 6H2O (3)
0,1 0,12← 0,01 mol
NO3-+ 8e + 10H+ → NH4+ + 3H2O (4)
8x xmol
Đặt số mol muối NH4+ là x mol
Theo ĐL BT e: ne cho= ne nhận nên 7,15.2/M= 0,08 + 0,1+8x (*1)
Mặt khác : mmuối= mM(NO3)2+ mNH4NO3= 7,15/M. (M+124)+80x= 21,19 (*2)
Từ (*1) và (*2) ta có: x= 5.10-3 và M=65. M là Zn
Đáp án D

a, Ta có: \(n_{NO}=\dfrac{0,448}{22,4}=0,02\left(mol\right)\)
Theo ĐLBT e, có: 2nR = 0,02.3 ⇒ nR = 0,03 (mol)
\(\Rightarrow M_R=\dfrac{1,92}{0,03}=64\left(g/mol\right)\)
Vậy: R là Cu.
b, Ta có: nHNO3 (pư) = 4nNO = 0,08 (mol)
Mà: HNO3 dùng dư 10% so với lượng cần pư.
⇒ nHNO3 = 0,08 + 0,08.10% = 0,088 (mol)
\(\Rightarrow C_{M_{HNO_3}}=\dfrac{0,088}{0,1}=0,88\left(M\right)\)

Ta có: \(n_{NO}+n_{N_2}=\dfrac{1,12}{22,4}=0,05\left(mol\right)\left(1\right)\)
\(30n_{NO}+28n_{N_2}=1,44\left(g\right)\left(2\right)\)
Từ (1) và (2) \(\Rightarrow\left\{{}\begin{matrix}n_{NO}=0,02\left(mol\right)\\n_{N_2}=0,03\left(mol\right)\end{matrix}\right.\)
Gọi nNH4NO3 = a (mol)
⇒ nNO3- (trong muối) = 3nNO + 10nN2 + 8nNH4NO3 = 0,36 + 8a (mol)
Ta có: m muối = mKL + mNO3- (trong muối) + mNH4NO3
⇒ 66,88 = 10 + 62.(0,36 + 8a) + 80a
⇒ a = 0,06 (mol)
⇒ nHNO3 = 4nNO + 12nN2 + 10nNH4NO3 = 1,04 (mol)

X gồm 2 khí không màu, không hóa nâu ngoài không khí và là sản phẩm khử của N nên X là N2, N2O
Đặt nN2= x mol; nN2O= y mol
Ta có nX= x+ y= 0,075 mol
mX= nX.MX= 0,075.17,2.2= 28x+ 44y
Giải hệ trên có : x= 0,045 ; y=0,03
QT nhận e :
2NO3-+ 8e+ 10H+ → N2O + 5H2O (1)
0,24 0,3 ← 0,03 mol
2NO3-+ 10e+12H+→ N2+ 6H2O (2)
0,45 0,54← 0,045
Theo PT (1), (2): nH+= 0,3+0, 54= 0,84 mol= nHNO3→ Vdd HNO3= 4,2 lít
QT cho e:
M → Mn++ ne
0,69/n 0,69 mol
Theo ĐL bảo toàn e : ne cho = ne nhận= 0,24+0,45= 0,69 mol
MM= mM/nM= 6,21 : 0,69/n=9n
Xét n=1, 2, 3 thì thấy chỉ có n=3, M=27 (Al) thỏa mãn
Đáp án D

Ta đặt nMg= 3x, nAl= 2x mol → mhh= 24.3x+ 27.2x=126x= 5,04 →x=0,04 mol→ nMg= 0,12 mol; nAl= 0,08 mol
Sản phẩm khử gồm 2 khí không màu, không hóa nâu ngoài không khí. Đó là N2 (a mol) và N2O (b mol)
Ta có a+b= 0,896/22,4= 0,04
Và mhh= 28a+ 44b= 18.2.0,04
Giải hệ trên có a= 0,02, b=0,02
QT cho e:
Mg→ Mg2++ 2e
0,12 0,24
Al→ Al3++ 3e
0,08 0,24
Tổng số mol e cho ne cho= 0,24+ 0,24= 0,48 mol
Quá trình nhận e:
2NO3-+ 10e+ 12H+ → N2 + 6H2O (2)
0,2 ← 0,02 mol
2NO3-+ 8e+ 10H+ → N2O + 5H2O (3)
0,16 ← 0,02mol
Tổng số mol e nhận ở (2) và (3) là ne nhận= 0,2+ 0,16= 0,36mol <0,48 mol
Do đó còn xảy ra quá trình nhận e: ne nhận ở (4)= 0,48- 0,36= 0,12 mol
NO3-+ 8e+ 10H+ → NH4++ 3H2O (4)
0,12 → 0, 015 mol
Theo các bán phản ứng (2), (3), (4) thì
nNO3-bị khử= 2.nN2+ 2. nN2O+nNH4+= 2.0,02+2.0,02+0,015= 0,095 mol
=nHNO3 bị khử
Đáp án A

Chọn D

Vì có khí H 2 thoát ra và Zn dư → H + và NO 3 - hết → Muối thu được là muối clorua.
Do n NO 3 - ban đầu = 0,15 mol > n NO = 0,09 mol→ X chứa NH 4 + .
Bảo toàn nguyên tố N → n NH 4 + = 0,15- 0,09= 0,06(mol)
Bảo toàn electron: 2. n Zn pứ = 3. n NO + 8 n NH 4 + + 2 n H 2 → n Zn pứ = n Zn 2 + = 0,405 mol
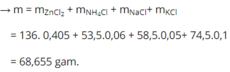

\(n_{Mg}=a\left(mol\right),n_{Al}=b\left(mol\right)\)
\(24a+27b=15\left(1\right)\)
Bảo toàn e :
\(2a+3b=0.1\cdot\left(2+3+1+8\right)\left(2\right)\)
\(\left(1\right),\left(2\right):\)
\(a=0.4,b=0.2\)
\(\%Mg=64\%,\%Al=36\%\)
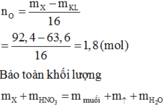

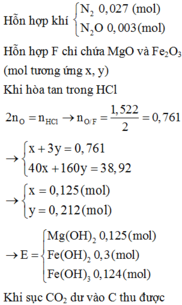

\(\overset{0}{R}\rightarrow\overset{+3}{R}+3e\)
\(\frac{5,94}{M}\rightarrow\frac{17,82}{M}\)mol
\(n_{khi}=0,12mol\)
\(a:n_{NO}\)
\(b:n_{N_2O}\)
\(\left\{{}\begin{matrix}a+b=0,12\\\frac{30a+44b}{0,12}=18,5.2\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}a=0,06\\b=0,06\end{matrix}\right.\)
\(\overset{+5}{N}+3e\rightarrow\overset{+2}{N}\)
\(0,18\leftarrow0,06mol\)
\(\overset{+5}{2N}+8e\rightarrow\overset{+1}{N_2}\)
\(0,48\leftarrow0,06mol\)
Bảo toàn e: \(\frac{17,82}{M}=0,18+0,48\Rightarrow M=27\)
Vậy R là Al
Bài 1:
\(T=\frac{0,2}{0,1}=2\)
=> Tạo 2 muối Na2HPO4
\(PTHH:2NaOH+H3PO4\rightarrow Na2HPO4+2H2O+HP+\)