Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

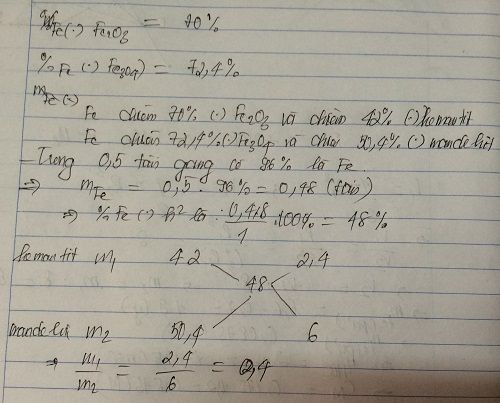
đề sai sai nha !
X là quặng hematit chứa 60% Fe2O3, Y là quặng manhetit chứa 69,6% Fe3O4. Cần trộn X, Y theo tỉ lệ khối lượng như thế nào để được quặng Z mà từ 1 tấn quặng Z có thể điều chế được 0,5 tấn gang chứa 96% sắt?OK!

mFe3O4 = \(\dfrac{69,6}{100}\).10 = 6,96 ( tấn)
nFe3O4 = \(\dfrac{6,96}{232}\) = 0,03 mol
Fe3O4 + 4CO \(^{to}\rightarrow\)3Fe + 4CO2 \(\uparrow\)
0,03---------------->0,09
\(\Rightarrow\)mFe= 0,09 . 56 = 5,04 ( tấn)
\(\Rightarrow\)mgang(LT) = 5,04 . \(\dfrac{100}{95,2}\) = 5,3 ( tấn)
mà hiệu suất phản ứng là 93%
\(\Rightarrow\)mgang(TT) = 5,3 . \(\dfrac{93}{100}\) = 4,77 ( tấn)

\(m_{Fe}=0.95\left(tấn\right)=0.95\cdot10^3\left(kg\right)\)
\(\Rightarrow n_{Fe}=\dfrac{0.95\cdot10^3}{56}=\dfrac{19}{1120}\cdot10^3\left(kmol\right)\)
\(\Rightarrow n_{Fe_2O_3}=\dfrac{1}{2}\cdot\dfrac{19}{1120}\cdot10^3\left(kmol\right)\)
\(m_{Fe_2O_3}=\dfrac{19}{2240}\cdot10^3\cdot160=1357.1\left(kg\right)\)
\(\Rightarrow m_{quặng}=\dfrac{1357.1}{60\%}=2261.9\left(kg\right)\)
\(A\)

\(m_{Fe_2O_3}=1000000.60\%=600000(g)\\ \Rightarrow n_{Fe_2O_3}=\dfrac{600000}{160}=3750(mol)\\ PTHH:Fe_2O_3+3CO\xrightarrow{t^o}2Fe+3CO_2\\ \Rightarrow n_{Fe}=2n_{Fe_2O_3}=7500(mol)\\ \Rightarrow m_{Fe(\text {Phản ứng})}=7500.56=420000(g)\\ \Rightarrow m_{Fe(\text {Thực tế)}}=420000.80\%=336000(g)\\ \Rightarrow m_{gang}=\dfrac{336000}{95\%}\approx353684(g)=353,684(kg)\)

Câu 1:
Ta có: 1 tấn = 1000 kg
⇒ mFe = 1000.95% = 950 (kg)
\(\Rightarrow n_{Fe}=\dfrac{950}{56}\left(kmol\right)\)
BTNT Fe, có: \(n_{Fe_2O_3\left(LT\right)}=\dfrac{1}{2}n_{Fe}=\dfrac{475}{56}\left(kmol\right)\)
Mà: H = 80% \(\Rightarrow n_{Fe_2O_3\left(TT\right)}=\dfrac{475}{56}:80\%=\dfrac{2375}{224}\left(kmol\right)\)
\(\Rightarrow m_{Fe_2O_3\left(TT\right)}=\dfrac{2375}{224}.160=\dfrac{11875}{7}\left(kg\right)\)
⇒ m quặng \(=\dfrac{m_{Fe_2O_3}}{60\%}\approx2827,38\left(kg\right)\)
Câu 2:
Ta có: 65nZn + 27nAl = 3,79 (1)
PT: \(Zn+H_2SO_4\rightarrow ZnSO_4+H_2\)
\(2Al+3H_2SO_4\rightarrow Al_2\left(SO_4\right)_3+3H_2\)
Theo PT: \(n_{H_2}=n_{Zn}+\dfrac{3}{2}n_{Al}=\dfrac{1,792}{22,4}=0,08\left(mol\right)\left(2\right)\)
Từ (1) và (2) \(\Rightarrow\left\{{}\begin{matrix}n_{Zn}=0,05\left(mol\right)\\n_{Al}=0,02\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}m_{Zn}=0,05.65=3,25\left(g\right)\\m_{Al}=0,02.27=0,54\left(g\right)\end{matrix}\right.\)

trong gang:nFe =3/350
BT ng tu ngto:2nFe2O3+3nFe3O4=3/350
=>2*0.6*m1/160+3*0.696*m2/232=3/350
m1+m2=1
=>m1=2/7;m2=5/7
=>m1:m2=2/5