Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Gọi CTTQ của oxit là RxOy
Moxit=Rx+16y=232
=>16y/(Rx+16y)=1-0,7241
=>y=4
=>Rx=232-64=168
Chọn các giá trị nguyên của x thấy x=3 tm=>R=56 Fe

Bài 1:
Gọi công thức oxit là XaOb
% khối lượng O chiếm là 27,59%
\(\Rightarrow\dfrac{16b}{232}.100=27,59\)
Vì kim loại chỉ có các hóa trị I, II, III nên xét các trường hợp b=1,2,3,4 (Trong trường hợp là oxit Fe3O4 thì n=4) .
Kiểm tra thì thấy b=4 thỏa mãn => MX=56.
Công thức chất cần tìm là Fe3O4

a)Gọi CTHH của oxit là \(R_xO_y\).
Trong phân tử có 5 nguyên tử tạo thành.
\(\Rightarrow x+y=5\left(1\right)\)
Theo bài: \(\%m_O=\dfrac{16y}{R\cdot a+16y}\cdot100\%=47,06\%\)
\(\Rightarrow\left\{{}\begin{matrix}a=2\\b=3\\R=27\Rightarrow Al\end{matrix}\right.\)
Vậy CTHH là \(Al_2O_3\) có tên nhôm oxit.
b)\(n_{Al_2O_3}=\dfrac{5,1}{102}=0,05mol\)
\(2Al\left(OH\right)_3\underrightarrow{t^o}Al_2O_3+3H_2O\)
0,1 0,05
\(m_{Al\left(OH\right)_3}=0,1\cdot78=7,8g\)
\(H=80\%\Rightarrow m_{Al\left(OH\right)_3}=7,8\cdot80\%=6,24g\)
a) Đặt CTHH của oxit là NxOy
Theo đề bài ta có : x + y = 5(1)
Mà : %O=\(\dfrac{16y}{Nx+16y}100=47,06\%\)=47,06%(2)
Giai hệ phương trình (1) và (2) ta có :
x=2,y=3,N=27g\mol
⇒CTHH:Al2O3.
Gọi tên : Nhôm oxit .
b)
PT 2Al(0H)3-to>Al2O3+3H2O
nAl2O3=0,05mol
=> nAl(OH)3 =0,1mol
mà H = 80% nên nAl(OH)3=0,125mol
=> mAl(OH)3 cần dùng = 0,125.78=9,75g

1)
PTKR2Ox = 2.NTKR + 16x = 102 (đvC)
| x | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 |
| NTKR | 43(Loại) | 35(Loại) | 27(Al) | 19(Loại) | 11(Loại) | 3(Loại) | Loại | Loại |
=> R là Al
2)
CTHH: RxOy
\(\%R=\dfrac{x.NTK_R}{160}.100\%=70\%\)
=> \(NTK_R=\dfrac{112}{x}\left(đvC\right)\)
Chỉ có x = 2 thỏa mãn \(NTK_R=\dfrac{112}{2}=56\left(đvC\right)\)
=> R là Fe
PTKFe2Oy = 160 (đvC)
=> y = 3
CTHH: Fe2O3

a) Câu hỏi của Trần Thị Thùy Trang - Hóa học lớp 8 | Học trực tuyến
b) Ta có: Hiệu suất 80% thì tạo thành 5,1g Al2O3
.....Vậy: Hiệu suất 100% thì tạo thành m (g) Al2O3
=> m = \(\dfrac{100\times5,1}{80}=6,375\left(g\right)\)
=> nAl2O3 = \(\dfrac{6,375}{102}=0,0625\) mol
Pt: 2Al(OH)3 --to--> Al2O3 + 3H2O
....0,125 mol<-------0,0625 mol
mAl(OH)3 = 0,125 . 78 = 9,75 (g)
Vậy .........................

Đặt công thức của oxit kim loại là MxOy
%mO = 100% - 70% = 30%
⇒ mO = 12y = 160.30% = 48
⇒ y = 3
mM = 160.70% = 112g = M.x (với M là phân tử khối của kim loại M)
Áp dụng quy tắc hóa trị ta có:
a.x = 2.3 = 6 (với a là hóa trị của M; a = 1; 2; 3)
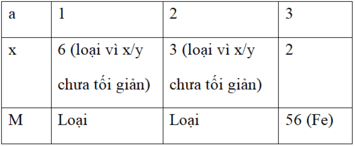
⇒ M là kim loại Sắt.
Vậy công thức hóa học của oxit kim loại là Fe2O3 (Sắt (III) oxit).

a) Đặt CTHH: AxOy
\(m_A=\frac{232.72,41}{100}=168\left(g\right)\)
\(m_O=232-168=64\left(g\right)\)
\(n_O=\frac{64}{16}=4\left(mol\right)\)
Ta có: A.x=168
Lập bảng ta có: x=3; A=56 là thích hợp
CTHH: Fe3O4
b) \(Fe_3O_4+4CO\underrightarrow{t^o}3Fe+4CO_2\)
\(n_{Fe_3O_4}=\frac{2,32}{232}=0,01\left(mol\right)\)
Vì hiệu suất là 30% nên chỉ có 30% lượng oxit sắt từ phản ứng
\(n_{Fe_3O_4}=\frac{0,01.30}{100}=0,003\left(mol\right)\)
\(n_{CO}=3.n_{Fe_3O_4}=3.0,003=0,009\left(mol\right)\)
\(m_{CO}=0,009.28=0,252\left(g\right)\)
a;
Fe3O4:oxit sắt từ
b; ko rõ đề