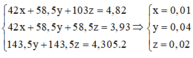Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

MnO 2 + HCl → MnCl 2 + Cl 2 + 2 H 2 O
Cl 2 + 2NaOH → NaCl + NaClO + H 2 O
n MnO 2 = 0,2 mol; n NaOH = 0,729 mol
Theo phương trình (1) ta có: n Cl 2 = n MnO 2 = 0,2 mol
Theo phương trình (2) ta có: 2 n Cl 2 < n NaOH ⇒ NaOH dư
Dung dịch A gồm: n NaCl = n NaClO = n Cl 2 = 0,2 mol
n NaOH dư = 0,729 – 2.0,2 = 0,329 mol
m dd A = m Cl 2 + m dd NaOH = 0,2.71 + 145,8 = 160g
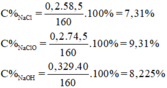

1) Ptpư:
2Al + 6HCl \(\rightarrow\) 2AlCl3 + 3H2
Fe + 2HCl \(\rightarrow\) FeCl2 + H2
Cu + HCl \(\rightarrow\) không phản ứng
=> 0,6 gam chất rắn còn lại chính là Cu:
Gọi x, y lần lượt là số mol Al, Fe
Ta có:
3x + 2y = 2.0,06 = 0,12
27x + 56 y = 2,25 – 0,6 = 1,65
=> x = 0,03 (mol) ; y = 0,015 (mol)
=> \(\%Cu=\frac{0,6}{2,25}.100\%=26,67\%\); \(\%Fe=\frac{56.0,015}{2,25}.100\%=37,33\%\); %Al = 36%
2) \(n_{SO_2}=\frac{1,344}{22,4}=0,06mol\); m (dd KOH) = 13,95.1,147 = 16 (gam)
=> mKOH = 0,28.16 = 4,48 (gam)=> nKOH = 0,08 (mol)=> \(1<\)\(\frac{n_{KOH}}{n_{SO_2}}<2\)
=> tạo ra hỗn hợp 2 muối: KHSO3: 0,04 (mol) và K2SO3: 0,02 (mol)
Khối lượng dung dịch sau pu = 16 + 0,06.64 = 19,84 gam
=> \(C\%\left(KHSO_3\right)=\frac{0,04.120}{19,84}.100\%\)\(=24,19\%\)
\(C\%\left(K_2SO_3\right)=\frac{0,02.158}{19,84}.100\%\)\(=15,93\%\)

\(Đặt:n_{MnO_2}=a\left(mol\right),n_{KMnO_4}=b\left(mol\right)\)
\(m_{hh}=87a+158b=37.96\left(g\right)\left(1\right)\)
\(n_{Cl_2}=\dfrac{10.08}{22.4}=0.45\left(mol\right)\)
\(2KMnO_4+16HCl\rightarrow2KCl+2MnCl_2+5Cl_2+8H_2O\)
\(MnO_2+4HCl\rightarrow MnCl_2+Cl_2+2H_2O\)
\(n_{Cl_2}=a+2.5b=0.45\left(mol\right)\left(2\right)\)
\(\left(1\right),\left(2\right):a=0.4,b=0.02\)
\(\%MnO_2=\dfrac{0.4\cdot87}{37.96}\cdot100\%=91.68\%\\\%KMnO_4=100-91.68=8.32\% \)
\(m_M=m_{KCl}+m_{MnCl_2}=0.02\cdot74.5+\left(0.4+0.02\right)\cdot126=54.41g\)

Câu 1:
2Al+ 6HCl---->2AlCl3+3H2
x-----3x----------------x----1,5x
Zn+2HCl----->ZnCl2+H2
y------2y------------y-----y
n HCl=0,4.2=0,8(mol)
Theo bài ta có hpt
\(\left\{{}\begin{matrix}27x+65y=11,9\\3x+2y=0,8\end{matrix}\right.\Rightarrow\left\{{}\begin{matrix}x=0,2\\y=0,1\end{matrix}\right.\)
m AlCl3=0,2.133,5=26,7(g)
m ZnCl2=0,1.136=13,6(g)
b) Theo pthh
n H2=1/2n HCl=0,4(mol)
V H2=0,4.22,4=8,96(l)
c) m muối=26,7+13,6=40,3(g)
2)
a) MnO2+4HCl---->Cl2+2H2O+MnCl2
Cl2+ 2NaOH---->H2O+NaCl+NaClO
b)
nNaOH = 0,5 x 4 = 2 mol
a) Phương trình hóa học của phản ứng mk ghi lại cho dễ nhìn nha
MnO2 + 4 HCl → MnCl2 + Cl2 +2H2O
0,8 mol 0,8mol 0,8 mol
Cl2 + 2NaOH → NaCl + NaClO + H2O
0,8 mol → 1,6 mol 0,8mol 0,8mol
b) Nồng độ mol/l của các chất trong dung dịch sau phản ứng:
CM(NaCl) = = CM(NaClO) =\(\frac{0,8}{0,5}\)= 1,6 mol/l
CM(NaOH)dư = = 0,8 mol/l
3) 
Chúc bạn học tốt

Câu 3:
Thứ tự các phản ứng như sau:
\(Cl_2+2KI\rightarrow2KCl+I_2\left(1\right)\)
\(Cl_2+2NaBr\rightarrow2NaCl+Br_2\left(2\right)\)
Ta có:
\(n_{Cl2}=\frac{8,064}{22,4}=0,36\left(mol\right)\)
\(n_{KI}=\frac{83}{39+127}=0,5\left(mol\right)\)
\(n_{NaBr}=\frac{15,45}{23+80}=0,15\left(mol\right)\)
Nhận thấy: \(2n_{Cl2}>n_{NaBr}+n_{KI}\) nên clo dư.
\(n_{KCl}=n_{KI}=0,5\left(mol\right);n_{NaCl}=n_{NaBr}=0,15\left(mol\right)\)
\(\Rightarrow m=m_{KCl}+m_{NaCl}=0,5.\left(39+35,5\right)+0,15.\left(23+35,5\right)=46,025\left(g\right)\)