Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Gọi số hạt proton = Số hạt electron = p
Gọi số hạt notron = n
Hạt mang điện là proton, electron
Hạt không mang điện là notron
Bài 1 :
Ta có :
$2p + n = 40$ và $2p - n = 12$
Suy ra p = 13 ; n = 14
Bài 2 :
Ta có :
$2p + n = 58$ và $n - p = 1$
Suy ra p = 19 ; n = 20
Bài 3 :
Ta có :
$2p + n = 48$ và $2p = 2n$
Suy ra p = n = 16

\(Tacó:\left\{{}\begin{matrix}2Z+N=40\\N-Z=1\end{matrix}\right.\\ \Rightarrow\left\{{}\begin{matrix}Z=13=P=E\\N=14\end{matrix}\right.\)

a,
Ta có: \(\left\{{}\begin{matrix}p+e+n=40\\p=e\\n-p=1\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}3p=39\\n=p+1\\p=e\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}p=e=13\\n=14\end{matrix}\right.\)
b,
Ta có: \(\left\{{}\begin{matrix}p+e+n=21\\p=e\\p+e-n=7\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}2n=14\\p=e\\p+e+n=21\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}p=e=7\\n=7\end{matrix}\right.\)
c,
Ta có: \(\left\{{}\begin{matrix}p+n=16\\p=e\\\dfrac{p}{n}=\dfrac{1}{1}\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}2p=16\\p=e\\p=n\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}p=e=8\\n=8\end{matrix}\right.\)

1. Ta có tổng số hạt cơ bản của nguyên tố X là 36 , suy ra
p + e + n = 36 => 2p + n = 36
Số hạt mang điện gấp đôi số hạt không mang điện : 2p = 2n => p = n
Vậy : 3p = 36 => p = 12 => số p = số e = số z = 12
Số khối : A = p + n = 12 + 12 = 24
2.
a, Ta có tổng số hạt cơ bản là 54 hạt.
=> p+e+n=54 => 2p+n=54(1)
Vì số hạt mang điện nhiều hơn số hạt không mang điện là 14
=> 2p-n=14(2)
Từ (1) và (2) ta có hệ pt:
2p-n=14
2p+n=54
<=> p=17
n=20
Vậy e=17, p=17, n=20
b, số hiệu nguyên tử Z=17
c, kí hiệu: Cl

Đáp án A
Ion X2- có cấu trúc electron: 1s22s22p63s23p6
X + 2e → X2-
Vậy cấu hình electron của X là 1s22s22p63s23p4
X có 3 lớp electron → X thuộc chu kì 3.
X có số electron = 16 → X thuộc ô 16.
X có 6 electron hóa trị, electron cuối cùng điền vào phân lớp 3p → X thuộc nhóm VIA.
• Nguyên tố Y có tổng số hạt cơ bản trong nguyên tử là 40. Trong đó số hạt mang điện nhiều hơn số hạt không mang điện là 12.
Giả sử số hiệu nguyên tử, số nơtron của Y lần lượt là Z, N
Ta có hpt: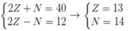
Cấu hình electron của Y là 13Y: 1s22s22p63s23p1
Y có 3 lớp electron → X thuộc chu kì 3.
Y có số electron = 13 → X thuộc ô số 13.
Y có 3 electron hóa trị, electron cuối cùng điền vào phân lớp 3p → Y thuộc nhóm IIIA.
• Ion Z2+ có tổng số hạt mang điện tích dương trong hạt nhân bằng 29.
Z có số hạt mang điện tích dương bằng ion Z2+
Cấu hình electron của Z là 29Z: 1s22s22p63s23p63d104s1
Z thuộc ô số 29.
Z có 4 lớp electron → X thuộc chu kì 4.
Z có electron cuối cùng điền vào phân lớp 3d, có 1 electron hóa trị → Z thuộc nhóm IB.
→ Chọn A.

a) \(\left\{{}\begin{matrix}2Z+N=52\\2Z-N=16\end{matrix}\right.\) \(\Leftrightarrow\left\{{}\begin{matrix}Z=17\\N=18\end{matrix}\right.\)
b) \(\left\{{}\begin{matrix}2Z+N=95\\2Z-N=25\end{matrix}\right.\) \(\Leftrightarrow\left\{{}\begin{matrix}Z=30\\N=35\end{matrix}\right.\)

Ta có: \(\left\{{}\begin{matrix}p+e+n=58\\p=e\\p+e-n=18\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}2n=40\\2p+n=58\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}p=e=19\\n=20\end{matrix}\right.\)


1.
Trong nguyên tử Y có: số p = số e = Z
số n = N
Theo đề bài ta có: \(\left\{{}\begin{matrix}2Z+N=40\\2Z-N=12\end{matrix}\right.\)
<=> \(\left\{{}\begin{matrix}4Z=52\\2Z-N=12\end{matrix}\right.\)
<=> \(\left\{{}\begin{matrix}Z=13\\N=14\end{matrix}\right.\)
=> Nguyên tố Y là Al
Bài 1 :
2Z + N = 40
2Z - N = 12
=> Z = 13
N = 14
Bài 2 :
Z + N = 58
-Z + N = 1
=> Z = 28.5
N = 29.5
Xem lại đề