Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Chọn A.
Khí duy nhất thoát ra tại anot là Cl2 (0,14 mol) Þ ne = 0,28 mol Þ nCu = 0,14 mol
Dung dịch sau điện phân chứa Cu2+ dư và H+ (chưa điện phân)
⇒ C u N O 3 2 0 , 02 m o l H C l 0 , 04 m o l
Dung dịch X (tính cho P2) chứa HCl (0,8 mol) và Cu(NO3)2 (0,32 mol)
Khi cho Fe tác dụng với dung dịch trên thì:

Hỗn hợp rắn gồm: 64.0,32 + m – 56.0,62 = 0,75m Þ m = 56,96 (g)

Thí nghiệm 1 :
\(n_{Mg} = a(mol) ; n_{Fe} = b(mol) \\ \Rightarrow 24a + 56b = 15,6(1)\\ Mg + H_2SO_4 \to MgSO_4 + H_2\\ Fe + H_2SO_4 \to FeSO_4 + H_2\\ n_{H_2} =a + b = 0,3(2)\\ (1)(2) \Rightarrow a = 0,0375 ; b = 0,2625\)
Thí nghiệm 2 : Vì khối lượng thí nghiệm 1 bằng 3 lần khối lượng thí nghiệm 2 nên ở thì nghiệm 2 : \(n_{Mg} = \dfrac{0,0375}{3}=0,0125(mol)\\ n_{Fe} = \dfrac{0,2625}{3} = 0,0875(mol)\\ \text{Bảo toàn electron : }\\ n_{SO_2} = \dfrac{0,0125.2 + 0,0875.3}{2} = 0,14375(mol)\\ m_X - m_{SO_2} = 5,2 - 0,14375.64 = -4\)
Vậy khối lượng dung dịch Z giảm 4 gam so với H2SO4 ban đầu.

Đáp án C
Tương tự các bài trước, theo định luật bào toàn mol electron, ta có:
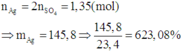
Mà đề bài hỏi khối lượng chất rắn tăng bao nhiêu phần trăm so với khối lượng G
Nên m = 623,08 – 100 = 523,08
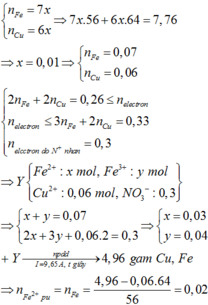
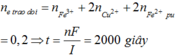



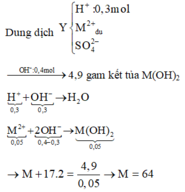
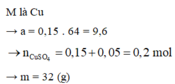


2/
áp dụng định luật Fa ra đây về điện phân
m = \(\dfrac{1}{F}\)\(\dfrac{A}{n}\).I.t trong đó
m khối lượng kim loại giải phóng
F = 96500
A khối lượng mol của kim loại
n hóa trị của kim loại
I cường độ dòng điện
t thời gian tính theo giây
⇒ 3,456 = \(\dfrac{1}{96500}\).\(\dfrac{A}{n}\)6.28,95.60
⇒\(\dfrac{A}{n}\)= 32
n = 2⇒ A = 64 (chọn A)