Tính C% của dung dịch thu được khi hòa tan 25 gam CuSO4 .5H2O vào 375 gam nước
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Khi đọc axit thì mình đọc gốc axit chứ không đọc nguyên tố em hi!
VD: HCl - Axit clohidric (Cl- là gốc clorua)
H2S - Axit sunfuhidric (S2- là gốc sunfua)
Với axit không có oxy cách đọc tên là: Axit + Tên gốc-hidric

Đáp án: vì Axit có 2 góc SO là H2SO3 và H2SO4 mà H2SO4 có nhiều oxi hơn H2SO3 (O4>O3)=> đuôi H2SO3 đọc là ơ. Còn axit có gốc NO chỉ có mỗi HNO3 thôi nên đuôi đọc là it

a, - Trích mẫu thử.
- Dẫn từng mẫu thử qua CuO (đen) nung nóng.
+ Chất rắn từ đen chuyển đỏ: H2.
PT: \(CuO+H_2\underrightarrow{t^o}Cu+H_2O\)
+ Không hiện tượng: O2, không khí. (1)
- Cho que đóm đang cháy vào mẫu thử nhóm (1)
+ Que đóm tiếp tục cháy: O2.
+ Que đóm cháy 1 lúc rồi tắt: không khí.
- Dán nhãn.
b, - Trích mẫu thử.
- Dẫn từng mẫu thử qua Ca(OH)2 dư.
+ Xuất hiện kết tủa trắng: CO2.
PT: \(CO_2+Ca\left(OH\right)_2\rightarrow CaCO_{3\downarrow}+H_2O\)
+ Không hiện tượng: H2, O2. (1)
- Dẫn mẫu thử nhóm (1) qua CuO (đen) nung nóng.
+ Chất rắn từ đen chuyển đỏ: H2.
PT: \(CuO+H_2\underrightarrow{t^o}Cu+H_2O\)
+ Không hiện tượng: O2.
- Dán nhãn.


a. PHHH: 4P + 5O2 ---> 2P2O5
\(n_P=\dfrac{6,2}{31}=0,2\left(mol\right)\)
Theo PTHH: \(n_{O_2}=\dfrac{0,2x5}{4}=0,25\left(mol\right)\)
Thể tích khí O2 (đktc) là: 0,25 x 22, 4 = 5,6 (l)
b. Số mol P2O5 thu được là: \(n_{P_2O_5}=\dfrac{n_P}{2}=\dfrac{0,2}{2}=0,1\left(mol\right)\)
Khối lượng P2O5 thu được là:
0,1 x 142 = 14,2 (gam)

TL:
Tham khảo nhé:

@@@@@@@@@@@@@@@@@@@@
@tuantuthan
HT
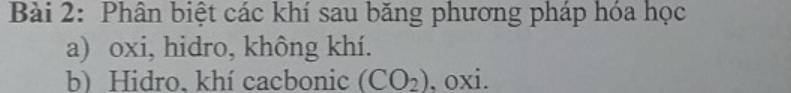
Ta có: \(n_{CuSO_4}=n_{CuSO_4.5H_2O}=\dfrac{25}{250}=0,1\left(mol\right)\)
m dd sau hòa tan = 25 + 375 = 400 (g)
\(\Rightarrow C\%_{CuSO_4}=\dfrac{0,1.160}{400}.100\%=4\%\)