Cho hỗn hợp X gồm 16,8 gam Fe và 12,8 gam Cu vào dung dịch HNO3 sau khi x tan hết thu được dung dịch y và 8,96 lít(dktc) khí NO(sản phảm khử duy nhất của N+5) cô cạn dd y của a gam muối.tính a
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Đáp án A
► Y hòa tan được Cu mà không thoát khí ⇒ Y chứa Fe3+ và H+ hết.
Cu + 2Fe3+ → Cu2+ + 2Fe2+ ⇒ nFe3+ = 2nCu = 0,4 mol.
● Đặt nFe2+ = x; nO = y ⇒ mX = 56.(x + 0,4) + 16y = 32(g).
nHNO3 = 4nNO + 2nO ⇒ nNO = (0,425 – 0,5y) mol || Bảo toàn electron:
2x + 3 × 0,4 = 2y + 3.(0,425 – 0,5y) ||⇒ giải hệ có: x = 0,1 mol; y = 0,25 mol.
||⇒ nNO = 0,425 – 0,5 × 0,25 = 0,3 mol ⇒ V = 6,72 lít

m muối = m KL + m NO 3 - = 27,5 + 0,4.3.62 = 101,9 gam.
Chọn đáp án C

Chọn C
∑ n e n h ư ờ n g = ∑ n e n h ậ n = n N O 3 - ( m u ố i ) = 3 . n k h í = 1 , 2 ( m o l ) m ố i m u ố i = m K L + m N O 3 - ( m u ố i ) = 27 , 5 + 1 , 2 . 62 = 101 , 9 g a m .

Đáp án A.
![]()
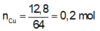
Quy hỗn hợp X về Fe và O
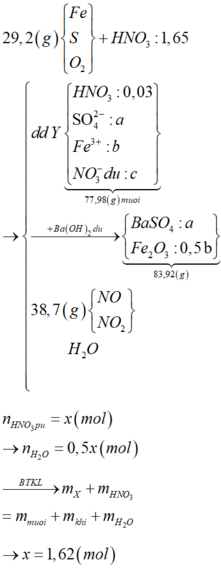
Sơ đồ phản ứng:
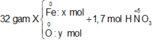
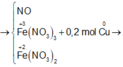

Quá trình cho nhận e:
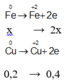
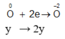
4 H + + N O 3 - + 3 e → N O + H 2 O
1,7 - 2y → 3 4 ( 1 , 7 - 2 y ) → 1 , 7 - 2 y 4
![]()
2y → y
m X = 32 g a m => 56x + 16y = 32 (1)
Bảo toàn electron
![]()
=> 2x - 0,5y = 0,875 (2)
Từ (1) và (2) => x = 0,5; y = 0,25
![]()
= 0,3 mol
=> V N O = 0,3.22,4 = 6,72 lit
=> Dung dịch Y chứa chất tan là FeCl2 và HCl

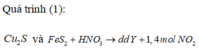
Vì thế Cu và Y vẫn có NO thoát ra
→ chứng tỏ H N O 3 dư
→ chứng tỏ phản úng oxi hóa – khử (1) xảy ra hoàn toàn.
→ khối lượng 12,8 kết hợp bảo toàn electron:
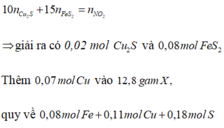
Phản ứng
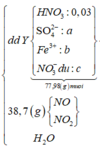
a m o l H N O 3 → m u ố i F e 2 + ; C u 2 + ; S O 4 2 - ; N O 3 - + 1 , 4 m o l N O 2 + ? m o l N O

Đáp án là B
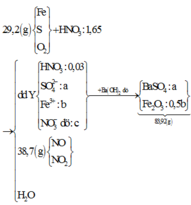
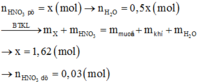
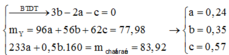
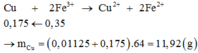
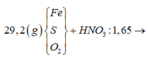
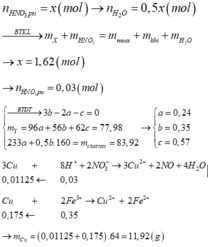
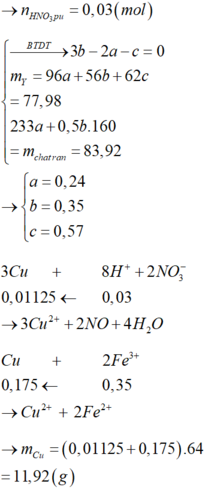
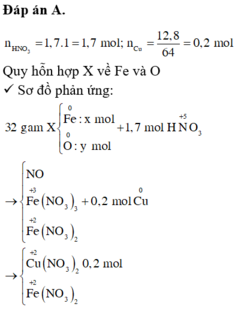

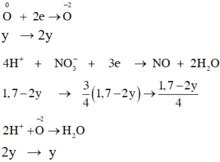

Ta có: nFe = 0,3 (mol)
nCu = 0,2 (mol) = nCu(NO3)2
nNO = 0,4 (mol)
BTNT Fe: nFe(NO3)2 + nFe(NO3)3 = nFe = 0,3 (1)
BT e, có: 2nFe(NO3)2 + 3nFe(NO3)3 + 2nCu = 3nNO = 1,2 (2)
Từ (1) và (2) \(\Rightarrow\left\{{}\begin{matrix}n_{Fe\left(NO_3\right)_2}=0,1\left(mol\right)\\n_{Fe\left(NO_3\right)_3}=0,2\left(mol\right)\end{matrix}\right.\)
⇒ a = 0,1.180 + 0,2.242 + 0,2.188 = 104 (g)