Giải chi tiết giúp em với ạ Bài 2. Cho 5,6 gam Fe tác dụng với dung dịch HNO3 (dư). Sau khi phản ứng xảy ra hoàn toàn thu được khí NO (ở đktc) . Tính khối lượng muối thu ? và Thể tích NO đktc
K
Khách
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Những câu hỏi liên quan

12 tháng 1 2018
Đáp án C
Bảo toàn electron : 2nMg = 3nNO + 8nNH4NO3
=> nNH4NO3 = 0,0075 mol
mmuối khan = mMg(NO3)2 + mNH4NO3 = 13,92g

18 tháng 10 2019
Đáp án : C
nMg = 0,09 mol ; nNO = 0,04 mol
Bảo toàn e : 2nMg = 3nNO + 8nNH4NO3 nếu có
=> nNH4NO3 = 0,0075 mol
=> Chất rắn gồm : 0,0075 mol NH4NO3 ; 0,09 mol Mg(NO3)2
=> mmuối khan = 13,92g

25 tháng 1 2018
Đáp án B
![]()
Vì sau phản ứng còn dư kim loại nên trong dung dịch B tồn tại Fe(NO3)2. Các phản láng xảy ra:
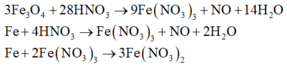
Như vậy trong toàn bộ các quá trình, số oxi hóa của sắt trong Fe và Fe3O4 đều về số oxi hóa +2.

Theo định luật bảo toàn mol electron, ta có:
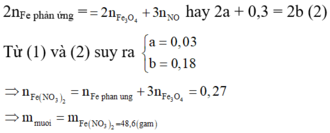



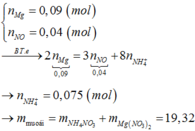
\(n_{Fe}=\dfrac{5,6}{56}=0,1mol\\ 3Fe+8HNO_3\rightarrow3Fe\left(NO_3\right)_2+2NO+4H_2O\\ n_{Fe\left(NO_3\right)_2}=n_{Fe}=0,1mol\\ m_{Fe\left(NO_3\right)_2}=0,1.180=18g\\ n_{NO}=0,1\cdot\dfrac{2}{3}=\dfrac{1}{15}mol\\ V_{NO}=\dfrac{1}{15}\cdot22,4=\dfrac{112}{75}\approx1,49l\)