Những nguyên tử nào trong cation ammonium thỏa mãn quy tắc octet?
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


- Nguyên tử C có 4 electron ở lớp vỏ ngoài cùng => Khi tham gia liên kết sẽ góp chung 4 electron
- Nguyên tử H có 1 electron ở lớp vỏ ngoài cùng => Khi tham gia liên kết sẽ góp chung 1 electron
a)
- Xét hydrocarbon: \(H - C \equiv C - H\)
+ Mỗi nguyên tử C có 4 (-), như vậy xung quanh mỗi nguyên tử C có 4 đôi electron chung => Có 8 electron ở lớp vỏ ngoài cùng => Đạt cấu hình khí hiếm Ne
+ Mỗi nguyên tử H có 1 (-), như vậy xung quanh mỗi nguyên tử H có 1 đôi electron chung => Có 2 electron ở lớp vỏ ngoài cùng => Đạt cấu hình khí hiếm He
=> Thỏa mãn quy tắc octet
- Xét hydrocarbon: \({H_2}C = C{H_2}\)
+ Mỗi nguyên tử C có 4 (-) 2 gạch giữa 2 C và 2 gạch với H, như vậy xung quanh mỗi nguyên tử C có 4 đôi electron chung => Có 8 electron ở lớp vỏ ngoài cùng => Đạt cấu hình khí hiếm Ne
+ Mỗi nguyên tử H có 1 (-) giữa C và H, như vậy xung quanh mỗi nguyên tử H có 1 đôi electron chung => Có 2 electron ở lớp vỏ ngoài cùng => Đạt cấu hình khí hiếm He
=> Thỏa mãn quy tắc octet
- Xét hydrocarbon: \({H_3}C - C{H_3}\)
+ Mỗi nguyên tử C có 4 (-) 1 gạch giữa 2 C và 3 gạch với H, như vậy xung quanh mỗi nguyên tử C có 4 đôi electron chung => Có 8 electron ở lớp vỏ ngoài cùng => Đạt cấu hình khí hiếm Ne
+ Mỗi nguyên tử H có 1 (-) giữa C và H, như vậy xung quanh mỗi nguyên tử H có 1 đôi electron chung => Có 2 electron ở lớp vỏ ngoài cùng => Đạt cấu hình khí hiếm He
=> Thỏa mãn quy tắc octet
b)
- Nguyên tử C tham gia 4 liên kết, nguyên tử H tham gia 1 liên kết để đạt cấu hình electron bền vững của khí hiếm
- Trong phân tử hydrocarbon, để x lớn nhất thì liên kết giữa C-H phải nhiều nhất
=> Liên kết giữa C và C phải là 1 (-)
Ta được công thức như sau: \({H_3}C - C{H_2} - C{H_3}\)
=> Có 8 nguyên tử H
=> Giá trị x lớn nhất có thể là 8.

- Cấu hình electron của F (Z = 9): 1s22s22p5
- Đề xuất của bạn học sinh không hợp lí trong thực tế vì:
+ Fluorine là nguyên tử có độ âm điện lớn nên khả năng nhận 1 electron dễ hơn nhường 7 electron.
+ Hai nlguyên tử F có độ âm điện bằng nhau nên không hình thành được liên kết ion như công thức (F7+)(F-)7 mà chỉ tạo được liên kết cộng hóa trị không cực.
- Sự hình thành liên kết trong phân tử F2:
Để đạt cấu hình của khí hiếm gần nhất, mỗi nguyên tử F đều cần thêm 1 electron. Vì vậy mỗi nguyên tử N cùng góp 1 electron để tạo nên 1 cặp electron chung cho 2 nguyên tử N.

⟹ Hai nguyên tử F liên kết với nhau bằng liên kết cộng hóa trị không cực tạo phân tử F2:
F - F

Quy tắc octet: Khi hình thành liên kết hoá học, các nguyên tử có xu hướng nhường, nhận hoặc góp chung electron để đạt tới cấu hình electron bền vững của nguyên tử khí hiếm.
Ví dụ:
- Phân tử O2
Khi hình thành liên kết hoá học trong phân tử O2, nguyên tử oxygen có 6 electron hoá trị, mỗi nguyên tử oxygen cần thêm 2 electron để đạt cấu hình electron bão hoà theo quy tắc octet nên mỗi nguyên tử oxygen góp chung 2 electron.
Phân tử O2 được biểu diễn như sau:


Các chất không thỏa mãn quy tắc bát tử là NO2 và PCl5:
NO2: cáu hình N:
1
s
2
2
s
2
2
p
3
, ở đây, N có lai hóa sp2 (cặp e ở 2s cho lai hóa với 2 e ở 2p tạo ra 4 e lai hóa sp2). Sử dụng 2 e để tạo liên kết đôi với 1 O, với O còn lại thì sẽ tạo liên kết cho nhận. Như vậy, trong N vẫn còn 1 e chưa liên kết. Do đó không thỏa mãn quy tắc bát tử
PCl5: P ở trạng thái kích thích (1 e ở 3s chuyển lên 3d làm cho P có 5 e độc thân), 5e này liên kết với 5 Cl, như vậy, xung quanh P có tổng cộng 10e nên cũng không thỏa mãn quy tắc bát tử.
=> Đáp án D

tham khảo
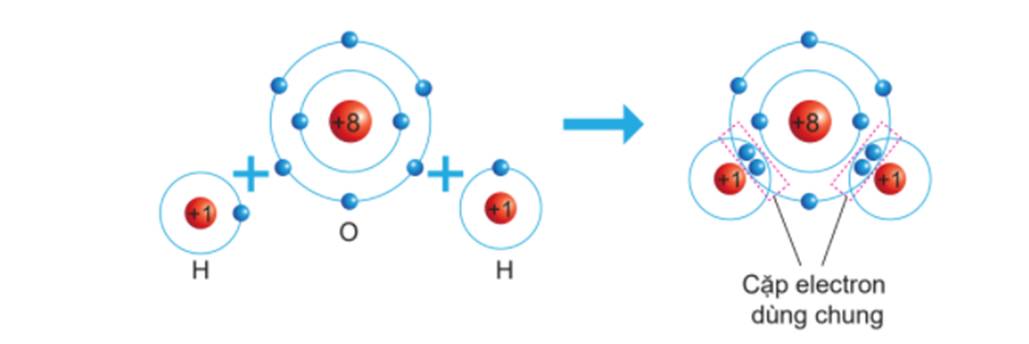
- Nguyên tử O (Z = 8): 1s22s22p4 ⇒ Có 6 electron lớp ngoài cùng ⇒ Có xu hướng nhận 2 electron để đạt được cấu hình electron giống khí hiếm.
- Nguyên tử H (Z = 1): 1s1 ⇒ Có xu hướng nhận 1 electron để đạt được cấu hình electron giống khí hiếm.
⇒ Mỗi nguyên tử H sẽ góp chung 1 electron với nguyên tử O (góp chung 2 electron) tạo thành 2 cặp electron dùng chung


- Ta thấy các nguyên tử H và N trong phân tử NH3 đều góp chung 1 electron để đạt cấu hình khí hiếm bền vững và tạo các liên kết đơn giữa mỗi nguyên tử.
- Trên nguyên tử N còn 1 cặp electron riêng, khi hình thành NH4+ cặp electron này trở thành cặp electron dùng chung cho cả N và H.
⟹ Cả N và các nguyên tử H đều thỏa mãn quy tắc octet.