pH của dung dịch nào sau đây có giá trị nhỏ nhất?
A. Dung dịch HCl 0,1 M.
B. Dung dịch CH3COOH 0,1 M.
C. Dung dịch NaCl 0,1 M.
D. Dung dịch NaOH 0,01 M.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

\(a,pH=-log\left[H^+\right]=1\\ b,pH=-log\left[H^+\right]=-log\left[0,1\right]=1\\ c,pH=7\\ d,pH=14-\left(-log\left[OH^-\right]\right)=14-\left(log\left[0,01\right]\right)=12\)
Chọn A và B
Đáp án: A
a, pH = -log[H+] = 1 (HNO3 là axit mạnh nên phân li hoàn toàn)
b, HF là axit yếu, phân ly không hoàn toàn ⇒ [H+] < 0,1 ⇒ pH > 1
c, KCl là muối trung hòa ⇒ pH = 7
d, KOH là bazo mạnh, phân ly hoàn toàn ⇒ pH = 14 - (-log[0,01]) = 12

Chọn B.
Tại V = 3b (kết tủa đạt cực đại) Þ 
Kết tủa bị hoà tan hết thì dung dịch thu được là Al3+ (0,03), Na+ (0,105), Cl- (y + 0,03) và SO42- (0,03)
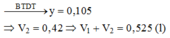

Đáp án D
C2H5OH ko là chất điện li nên khả năng dẫn điện kém nhất
CH3COOH là chất điện li yếu nên tổng nồng độ các ion < 0,2 mol
NaCl → Na++ Cl-
0,1 0,1 0,1
Tổng nồng độ các ion là 0,2M
K2SO4→ 2K++ SO42-
0,1 0,2 0,1
Tổng nồng độ các ion là 0,3M
Do đó độ dẫn điện C2H5OH<CH3COOH< NaCl < K2SO4

Vì muối CH3COONa là chất điện li mạnh nên ta có
![]()
Do đó sau quá trình trên trong dung dịch có nồng độ của ion CH3COO- là 0,1.
Xét cân bằng điện li: CH3COOH + H2O ⇌ CH3COO- + H3O+
Nồng độ ban đầu: 0,1 0,1 0
Nồng độ phân li: x(M) → x x
Nồng độ cân bằng: 0,1 – x 0,1 + x x
Thay các giá trị ở trạng thái cân bằng vào công thức tính hằng số điện li thì ta có
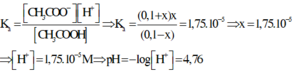
Đáp án D.
A. Dung dịch HCl 0,1 M.