Các nguyên tố chu kì 2 có bao nhiêu lớp electron? Vẽ mô hình nguyên tử theo Rutherford – Bohr của Li và F để giải thích về sự khác biệt bán kính nguyên tử.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Theo mô hình Rutherford – Bohr: Electron ở càng xa hạt nhân thì có năng lượng càng cao.
⇒ Lớp L ở xa hạt nhân hơn nên electron ở lớp L có năng lượng cao hơn.

Tham khảo:
Lực giữ cho electron chuyển động tròn quanh hạt nhân là lực tương tác tĩnh điện giữa electron và proton (lực hút). Lực này có phương nằm trên bán kính quỹ đạo và luôn có chiều hướng vào tâm quỹ đạo. Do đó, lực này đóng vai trò như lực hướng tâm, giữ cho electron chuyển động trên quỹ đạo tròn quanh hạt nhân.

a) Mô hình Rutherford – Bohr còn gọi là mô hình hành tinh nguyên tử vì trong mô hình Rutherford – Bohr electron quay xung quanh hạt nhân theo các quỹ đạo giống như các hành tinh quay xung quanh Mặt Trời.
b) Theo mô hình hiện đại, xác suất tìm thấy electron ở mỗi thùy trong AO p là khoảng 90%.
c)


Theo mô hình Rutherford – Bohr Electron ở càng xa hạt nhân thì có năng lượng càng cao.
Vì thế nên khi electron của nguyên tử H hấp thụ một năng lượng phù hợp, electron đó sẽ chuyển ra xa hạt nhân hơn.

1. Nguyên tử nguyên tố H , nguyên tử nguyên tố He có 1 lớp e
Nguyên tử nguyên tố Li, Be, C, N có 2 lớp e.
2. STT chu kì của nguyên tử nguyên tố H, He (1) < STT chu kì của nguyên tử nguyên tố Li, Be, C, N (2)


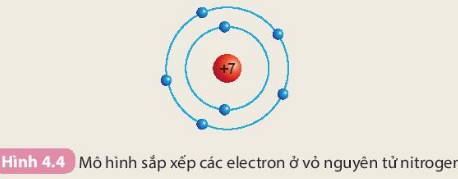
- Các nguyên tố chu kì 2 có 2 lớp electron.
- Mô hình nguyên tử của Li (Z = 3) và F (Z = 9) theo Rutherford – Bohr như sau:
- Nguyên tố Li và F đều có 2 lớp electron nên cùng chu kì 2, số đơn vị điện tích hạt nhân của Li nhỏ hơn F. Vì vậy bán kính nguyên tử Li lớn hơn nguyên tử F.