Cho 5,6 lít khí CO2 tác dụng với NaOH sau phản ứng thu được hỗn hợp 2 muối.Tính số mol NaOH đã dùng?
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Ta có: \(n_{Fe}=\dfrac{5,6}{56}=0,1\left(mol\right)\)
PT: \(Fe+2HCl\rightarrow FeCl_2+H_2\)
____0,1______0,2_____0,1____0,1 (mol)
a, \(C_{M_{HCl}}=\dfrac{0,2}{0,15}=\dfrac{4}{3}\left(M\right)\)
\(V_{H_2}=0,1.22,4=2,24\left(l\right)\)
b, \(FeCl_2+2NaOH\rightarrow2NaCl+Fe\left(OH\right)_2\)
Theo PT: \(n_{NaOH}=2n_{FeCl_2}=0,2\left(mol\right)\)
\(\Rightarrow V_{NaOH}=\dfrac{0,2}{2}=0,1\left(l\right)\)

Đáp án A
► Quy X và Y về CH2, COO và NH3 ⇒ nNH3 = 2nN2 = 0,4 mol.
COO ⇌ CO2 ⇒ không bị đốt ⇒ nO2 = 1,5nCH2 + 0,75nNH3 ⇒ nCH2 = 1,55 mol.
⇒ nCOO = 2,05 – 1,55 = 0,5 mol ⇒ m = 0,5 × 40 = 20(g)

1. Gọi chung hh 2 KL trên là A.
BT e, có: nA = 2nH2 ⇒ nH2 = 0,05 (mol)
⇒ VH2 = 0,05.22,4 = 1,12 (l)
2. Ta có: \(n_{H_2}=\dfrac{3,36}{22,4}=0,15\left(mol\right)\)
BT e, có: 3nAl = 2nH2 ⇒ nAl = 0,1 (mol)
\(\Rightarrow m_{Al_2O_3}=7,8-m_{Al}=5,1\left(g\right)\)
\(\Rightarrow\%m_{Al_2O_3}=\dfrac{5,1}{7,8}.100\%\approx65,38\%\)
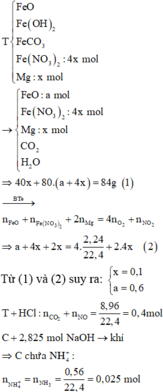



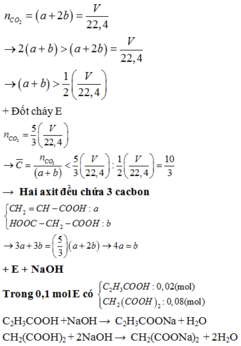

\(n_{CO_2}=0,25mol\)
Để tạo ra 2 muối thì \(1< \dfrac{n_{OH^-}}{n_{CO_2}}< 2\)
Vậy số mol NaOH nằm trong khoảng từ \(0,25< n_{NaOH}< 0,5\).
Vì đề bài của em cung cấp đang thiếu nên mình chỉ làm được đến bước này em nhé!