(Đề bị mờ Ko chụp được thông cảm) hai chất khí A,B có công thức dạng chung lần lượt là XY2 và XâY. Nếu trộn hai khí A,B theo tỉ lệ 2:3 thì được 1 hỗn hợp khí C có tỉ khối so với khí Hiđro là 22,4. Mặt khác , tỉ khối của A so với B xấp xỉ bằng 1,0455 a,Xác định CTHH của A và B b,Tính khối lượng nguyên tố Y có trong 25,3gam mỗi chất A,B nói trên c,Để thu mỗi khí A,B vào lọ bằng phương pháp đẩy không khí thì đặt ngược hay đặt đứng lọ ? Vì sao?
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

a) Giả sử có 2 mol A, 3 mol B
=> \(\dfrac{2.M_A+3.M_B}{2+3}=22,4.2=44,8\)
=> 2.MA + 3.MB = 224
Mà \(\dfrac{M_A}{M_B}=1,0455\)
=> MA = 46, MB = 44
=> \(\left\{{}\begin{matrix}M_X+2M_Y=46\\2M_X+M_y=44\end{matrix}\right.=>\left\{{}\begin{matrix}M_X=14\\M_Y=16\end{matrix}\right.\) => X là N, Y là O
CTHH của A là NO2, của B là N2O
b)- \(n_{NO_2}=\dfrac{25,3}{46}=0,55\left(mol\right)=>n_O=0,55.2=1,1\left(mol\right)\)
=> \(m_O=1,1.16=17,6\left(g\right)\)
- \(n_{N_2O}=\dfrac{25,3}{44}=0,575\left(mol\right)=>n_O=0,575\left(mol\right)\)
=> mO = 0,575.16 = 9,2(g)
c) \(d_{NO_2/kk}=\dfrac{46}{29}=1,586\)
=> NO2 nặng hơn kk nên đặt đứng lọ
\(d_{N_2O/kk}=\dfrac{44}{29}=1,517\)
=> N2O nặng hơn kk nên đặt đứng lọ

\(a,\text{Đ}\text{ặt}:S_xO_y\left(x,y:nguy\text{ê}n,d\text{ươ}ng\right)\\ \%m_S=\%m_O=50\%\\ \Leftrightarrow32.x=16.y\\ \Leftrightarrow\dfrac{x}{y}=\dfrac{16}{32}=\dfrac{1}{2}\Rightarrow x=1;y=2\\ \Rightarrow CTHH:SO_2\)
b) Phản hỏi tỉ lệ hoặc cho thể tích hh khí mới hợp lí chứ nhỉ?

vẫn như đề trước, câu b nếu đề hỏi tỉ lệ hoặc cho số lít hh thì có lẽ sẽ ổn hơn.

a) \(M_X=19.2=38\left(g/mol\right)\)
`=>` \(d_{X/kk}=\dfrac{38}{29}=1,310345\)
b) \(m_X=0,4.38=15,2\left(g\right)\)
Gọi \(\left\{{}\begin{matrix}n_{O_2}=x\left(mol\right)\\n_{CO_2}=y\left(mol\right)\end{matrix}\right.\)
`=>` \(\left\{{}\begin{matrix}32x+44y=15,2\\x+y=0,4\end{matrix}\right.\Leftrightarrow x=y=0,2\)
\(m_Y=0,1.28+15,2=18\left(g\right)\)
`=>` \(\left\{{}\begin{matrix}\%m_{N_2}=\dfrac{0,1.28}{18}.100\%=15,56\%\\\%m_{O_2}=\dfrac{0,2.32}{18}.100\%=35,56\%\\\%m_{CO_2}=100\%-15,56\%-35,56\%=48,88\%\end{matrix}\right.\)
b) \(M_{hh}=4.10=40\left(g/mol\right)\)
Gọi \(n_{NO_2}=a\left(mol\right)\)
`=>` \(\left\{{}\begin{matrix}m_{hh}=18+46a\left(g\right)\\n_{hh}=0,5+0,1+a=0,6+a\left(mol\right)\end{matrix}\right.\)
`=>` \(M_{hh}=\dfrac{m_{hh}}{n_{hh}}=\dfrac{18+46a}{0,6+a}=40\)
`=> a = 1`
`=> V_{NO_2(đktc)} = 1.22,4 = 22,4 (l)`

Giả sử trong 1 mol A có X mol C n H 2 n - 2 và (1 - x) mol H 2 . Khối lượng của 1 mol A là :
M A = (14n - 2)x + 2(1 - x) = 4,8.2 = 9,6 (g/mol) (1)
Khi đun nóng 1 mol A có mặt Ni, tất cả ankin đã biến hết thành ankan (vì B không tác dụng với nước brom) :
C n H 2 n - 2 + 2 H 2 → C n H 2 n + 2
x mol 2x mol x mol
Số mol khí còn lại trong B là (1 - 2x) mol nhưng khối lượng hỗn hợp B vẫn bằng khối lượng hỗn hợp A tức là bằng 9,6 g. Khối lượng của 1 mol B:
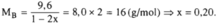
Thay x = 0,2 vào (1), tìm được n = 3.
Hỗn hợp A: C 3 H 4 chiếm 20%, H2 chiếm 80%.
Hỗn hợp B:
C
3
H
8
chiếm 
Vậy H 2 chiếm 67%.

Giả sử trong 1 mol A có x mol C n H 2 n và (1 - x) mol H 2 .
M A = 14nx + 2(1 - x) = 2.6 = 12 (g/mol) (1)
Khi đun nóng 1 mol A có mặt chất xúc tác Ni, tất cả anken đã chuyển hết thành ankan (vì B không làm mất màu nước brom).
C n H 2 n + H 2 → C n H 2 n + 2
x mol x mol x mol
Số mol khí trong hỗn hợp B là (1 - x)
Khối lượng hỗn hợp B = khối lượng hỗn hợp A = 12 (g). Do đó :

Thay x = 0,25 vào (1), tìm được n = 3.
Hỗn hợp A: C 3 H 6 25%; H2: 75%.
Hỗn hơp B:
C
3
H
8
: 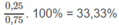
H 2 : 66,67%.