Khi lấy 6,66g muối clorua của Kim loại M (hoá tri 2) và một lượng muối nitrat của Kim loại đó có cùng số mol với muối clorua trên thấy khác 3,18g. Xác đinhj công thức phân tử của các muối
Plssss help me!!!.__.Thén ciù
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Gọi kim loại cần tìm là M, có hóa trị là n
Công thức muối clorua là MCln
Công thức muối nitrat là M(NO3)n. Có số mol là x
Theo bài ra ta có hệ phương trình :
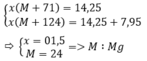

gọi Cthuc Oxit X là M2On : Y là : M2Om
Ta có Pt; M2On + 2nHNO3-> 2M(NO3)n+ nH2O
M2On + 2nHCl2-> 2MCln+ nH2O
- Tự chọn lượng chất: Gọi số gam oxit X là (2M+16n)gam hay 1 mol
ta có 2(M+62n)-2(M+35,5n)= 99,38( 2M+16n)/100
Gia ra:
M=18,7n
biện luân với n= 1,2,3
Nhận n=3 =>M =56
Vậy X là Fe2O3
Từ Phân tử khối của oxit Y bằng 45% phân tử khối của oxit X
=> Y: FeO

gọi Cthuc Oxit X là M2On : Y là : M2Om
Ta có Pt; M2On + 2nHNO3-> 2M(NO3)n+ nH2O
M2On + 2nHCl2-> 2MCln+ nH2O
- Tự chọn lượng chất: Gọi số gam oxit X là (2M+16n)gam hay 1 mol
ta có 2(M+62n)-2(M+35,5n)= 99,38( 2M+16n)/100
Gia ra:
M=18,7n
biện luân với n= 1,2,3
Nhận n=3 =>M =56
Vậy X là Fe2O3
Từ Phân tử khối của oxit Y bằng 45% phân tử khối của oxit X
Suy ra nốt Y: FeO

TK
CT muối clorua của KL kiềm là MCl
2MCl -dpnc→ 2M + Cl2
Khí ở anot là Cl2. Số mol Cl2:
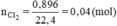
Số mol M là: nM = 0,04. 2 = 0,08 (mol)
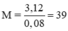

Giả sử M có hóa trị n không đổi.
PT: \(2M+2nHCl\rightarrow2MCl_n+nH_2\)
\(M+2nHNO_{3\left(đ\right)}\underrightarrow{t^o}M\left(NO_3\right)_n+nNO_2+nH_2O\)
Ta có: \(n_M=\dfrac{3,6}{M_M}\left(mol\right)\)
Theo PT: \(n_{MCl_n}=n_M=\dfrac{3,6}{M_M}\left(mol\right)\) \(\Rightarrow m_{MCl_n}=\dfrac{3,6.\left(M_M+35,5n\right)}{M_M}\left(g\right)\)
\(n_{M\left(NO_3\right)_n}=\dfrac{3,6}{M_M}\left(mol\right)\) \(\Rightarrow m_{M\left(NO_3\right)_n}=\dfrac{3,6.\left(M_M+62n\right)}{M_M}\left(g\right)\)
\(\Rightarrow\dfrac{3,6\left(M_M+62n\right)}{M_M}-\dfrac{3,6\left(M_M+35,5n\right)}{M_M}=7,95\)
\(\Rightarrow M_M=12n\left(g/mol\right)\)
Với n = 2, MM = 24 (g/mol) là thỏa mãn.
Vậy: M là Mg.

bn sửa giúp mình câu b) nhé :'((((
sơ đồ là
Catot (-) <-------ZnCl2-------> Anot (+)
Zn2+ + 2e --> Zn 2Cl- --> Cl2 + 2e
a) Gọi CTHH của muối đó là XCl2
X+2 + 2e --> X
Có \(m=\dfrac{AIt}{nF}=\dfrac{M_X.5.1800}{2.96500}\)
=> \(M_X=65\left(Zn\right)\)
b)
Ở catot: Zn2+ + 2e --> Zn
Ở anot: 2Cl- --> Cl2 + 2e
\(ZnCl_2\underrightarrow{đpdd}Zn+Cl_2\)
CTHH muối clorua: MCl2
CTHH muối nitrat: M(NO3)2
\(\left\{{}\begin{matrix}m_{muối.clorua}=n.\left(M_M+71\right)=n.M_M+71n\left(g\right)\\m_{muối.nitrat}=n\left(M_M+124\right)=n.M_M+124n\left(g\right)\end{matrix}\right.\)
=> \(m_{muối.clorua}< m_{muối.nitrat}\)
=> \(m_{muối.nitrat}=6,66+3,18=9,84\left(g\right)\)
\(n_{MCl_2}=\dfrac{6,66}{M_M+71}\left(mol\right)\Rightarrow n_{M\left(NO_3\right)_2}=\dfrac{6,66}{M_M+71}\left(mol\right)\)
=> \(M_{M\left(NO_3\right)_2}=\dfrac{9,84}{\dfrac{6,66}{M_M+71}}=M_M+124\left(g/mol\right)\)
=> MM = 40 (g/mol)
=> M là Ca
CTHH muối clorua: CaCl2
CTHH muối nitrat: Ca(NO3)2
cảm mưn ng bn rứt nhiều ạhhh
:3333