Dẫn 1 lít hỗn hợp khí X gồm N2 và CO2 (đktc) đi chậm qua 2 lít dung dịch Ca(OH)2 0,01 M thu được 1g kết tủa. Tính thể tích của N2 và CO2 trong X
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Số mol Ca(OH)2 = 2.0,02 = 0,04 mol
Số mol Ca(OH)2 = 2.0,02 = 0,04 mol
Số mol CaCO3 = 1_100=0,01 mol
Bài toán này có thể là 1 trong 2 trường hợp sau:
TH1: Số mol CO2 không đủ tác dụng với số mol Ca(OH)2
CO2 + Ca(OH)2 → CaCO3↓ + H2O
Số mol CO2 = số mol CaCO3 =0,01 mol
=>Thể tích CO2 = 22,4.0,01=0,224 lít
Vậy %thể tích CO2 = (0,224.100)/10=2,24%
TH2: Số mol CO2 nhiều hơn số mol Ca(OH)2 tham gia phản ứng:
CO2 + Ca(OH)2 → CaCO3↓ + H2O (1)
CaCO3 + CO2 + H2O → Ca(HCO3)2 (2)
Theo (1): số mol CO2 (1) = số mol CaCO3 = Số mol Ca(OH)2 = 0,04 mol
Ta có: Số mol CaCO3 (2) = 0,04-0,01 = 0,03 (mol)
Theo (2): Số mol CO2(2) = số mol CaCO3 (2) = 0,03 (mol)
Vậy tổng số mol CO2 phản ứng (1) và (2) là 0,04 + 0,03 = 0,07 mol
Do đó %thể tích CO2 = (0,07.22,4.100)/10 = 15,68%

n(Ca(OH)2) = 0,1 mol; n(CaCO3) = 0,05.
TH1: CO2 thiếu
CO2 + Ca(OH)2 → CaCO3 + H2O.
→ n(CaCO3) = n(CO2) = 0,05.=> n(N2) = 0,25 – 0,05 = 0,2.
Nên dX/H2 =\(\dfrac{0,05.44+0,2.28}{0,25.2}\) = 15,6. Không có đáp án nào.
TH2: CO2 phản ứng hết,
CO2 + Ca(OH)2 → CaCO3 + H2O.
0,05 0,05 0,05
2CO2 + Ca(OH)2 → Ca(HCO3)2
0,1 ← (0,1 – 0,05)
=> n(CO2) = 0,15 => n(N2) = 0,25 – 0,15 = 0,1.
Nên dX/H2 =\(\dfrac{0,15.44+0,1.28}{0,25.2}\) = 18,8. Thỏa mãn.

Đáp án D
Ta có nCa(OH)2= 2.0,02= 0,04 mol; nCaCO3= 1/100= 0,01 mol
Ta có nCa(OH)2 > nCaCO3 nên có 2 trường hợp:
- TH1: Ca(OH)2 dư
CO2 + Ca(OH)2 → CaCO3 + H2O (1)
Theo PT (1): nCaCO3= nCO2= 0,01 mol →VCO2=0,01.22,4=0,224 lít
→%VCO2= 2,24%→ %VN2= 100%- 2,24%=97,76%
- TH2: Ca(OH)2 phản ứng hết:
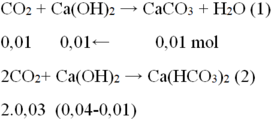
Ta có: nCO2= 0,01+ 2.0,03= 0,07 mol →VCO2= 0,07.22,4=1,568 lít
→%VCO2= 15,68%→ %VN2= 100%- 15,68%=84,32%

Đáp án A.
→ n X = 0 , 5 ; n C O 2 = 0 , 15 ; n C O = 0 , 1 → n N 2 = 0 , 25
→
n
X
=
0
,
25
→
n
C
a
C
O
3
=
n
C
O
+
n
C
O
2
=
0
,
125
→
m
=
12
,
5

Đáp án A.
![]()
![]()
→ n X = 0 , 25 → n C a C O 3 = n C O + n C O 2 = 0 , 125 → m = 12 , 5

nCa(OH)2=0,04mol
nCaCO3=0,01mol
-->CO2 có 2 TH
TH1:nCO2=nCaCO3=0,01mol-->VCO2=0,224l-->%=2,24%-->%N2=97,76%
TH2: nCO2=2nCa(2+)-nCaCO3=0,09mol-->VCO2=2,016l-->%=20,16%-->%N2=79,84%

a)Gọi \(\left\{{}\begin{matrix}n_{CO_2}=x\left(mol\right)\\n_{N_2}=y\left(mol\right)\end{matrix}\right.\)
Giả sử \(n_X=1mol\Rightarrow x+y=1\left(1\right)\)
\(d_X\)/O2=1,225\(\Rightarrow\overline{M_X}=1,225\cdot32=39,2\)
\(\Rightarrow\dfrac{44x+28y}{x+y}=39,2\Rightarrow4,8x-11,2y=0\left(2\right)\)
Từ (1) và (2) \(\Rightarrow\left\{{}\begin{matrix}x=0,7\\y=0,3\end{matrix}\right.\)
\(\%V_{N_2}=\dfrac{0,3}{1}\cdot100\%=30\%\)
b)\(n_{CaCO_3}=\dfrac{20}{100}=0,2mol\)
\(Ca\left(OH\right)_2+CO_2\rightarrow CaCO_3+H_2O\)
0,2 0,2 0,2
\(V=0,2\cdot22,4=4,48l\)

Ta có: \(n_{Ca\left(OH\right)_2}=1.0,02=0,02\left(mol\right)\)
\(n_{CaCO_3}=\dfrac{1}{100}=0,01\left(mol\right)\)
TH1: Ca(OH)2 dư.
PT: \(CO_2+Ca\left(OH\right)_2\rightarrow CaCO_3+H_2O\)
\(\Rightarrow n_{CO_2}=n_{CaCO_3}=0,01\left(mol\right)\)
\(\Rightarrow\%V_{CO_2}=\dfrac{0,01.22,4}{15,68}.100\%=\dfrac{10}{7}\%\)
TH2: Ca(OH)2 hết.
\(CO_2+Ca\left(OH\right)_2\rightarrow CaCO_3+H_2O\)
0,01_____0,01_______0,01 (mol)
\(2CO_2+Ca\left(OH\right)_2\rightarrow Ca\left(HCO_3\right)_2\)
0,02______0,01 (mol)
⇒ nCO2 = 0,01 + 0,02 = 0,03 (mol)
\(\Rightarrow\%V_{CO_2}=\dfrac{0,03.22,4}{15,68}.100\%=\dfrac{30}{7}\%\)
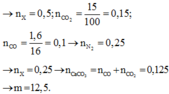
nCa(OH)2 = 2.0,01 = 0,02 (mol)
\(n_{CaCO_3}=\dfrac{1}{100}=0,01\left(mol\right)\)
TH1: Nếu kết tủa không bị hòa tan
PTHH: Ca(OH)2 + CO2 --> CaCO3 + H2O
0,01<----0,01
=> \(\left\{{}\begin{matrix}V_{CO_2}=0,01.22,4=0,224\left(l\right)\\V_{N_2}=1-0,224=0,776\left(l\right)\end{matrix}\right.\)
TH2: Nếu kết tủa bị hòa tan 1 phần
PTHH: Ca(OH)2 + CO2 --> CaCO3 + H2O
0,02---->0,02------>0,02
CaCO3 + CO2 + H2O --> Ca(HCO3)2
0,01--->0,01
=> VCO2 = (0,02 + 0,01).22,4 = 0,672 (l)
=> VN2 = 1 - 0,672 = 0,328 (l)