khi nung nóng hoàn toàn hỗn hợp bột Fe và S trong bình kín không có không khí, thu được hỗn hợp rắn X tác dụng với dd HCl thu được hỗn hợp khí H2 và H2S. Vậy trong chất rắn X có các chất ?
(xin cách giải chi tiết ạ)
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

`a)`
`n_{Fe}=0,1(mol);n_S=0,05(mol)`
`S+Fe` $\xrightarrow{t^o}$ `FeS`
`0,05->0,05->0,05(mol)`
`0,1>0,05->Fe` dư.
`->X` gồm `Fe:0,1-0,05=0,05(mol);FeS:0,05(mol)`
`Fe+2HCl->FeCl_2+H_2`
`FeS+2HCl->FeCl_2+H_2S`
Theo PT: `n_{H_2}=n_{Fe}=0,05(mol);n_{H_2S}=n_{FeS}=0,05(mol)`
`->\%V_{H_2}=\%V_{H_2S}={0,05}/{0,05+0,05}.100\%=50\%`
`b)`
`n_{NaOH}=0,125.0,1=0,0125(mol)`
`NaOH+HCl->NaCl+H_2O`
Theo PT: `\sum n_{HCl}=n_{NaOH}+2n_{H_2}+2n_{H_2S}=0,2125(mol)`
`->C_{M\ HCl}={0,2125}/{0,5}=0,425M`

A + H2SO4 → Hỗn hợp khí ⇒ Fe dư; khí Y gồm: H2 ( x mol) và H2S (y mol)
⇒ x + y = 0,1 mol (1)
Bảo toàn S: nH2S = nFeS = nS = y mol
nFe dư = nH2 = x
Bảo toàn Fe: nFe = nFeS + nFe dư = x + y
mX = 56(x + y ) + 32y = 7,2g (2)
Từ (1)(2) ⇒ x = 0,05 mol; y = 0,05 mol
MY = mY : nY = (0,05.2 + 0,05.34) : 0,1 = 18 ⇒ dY/H2 = 9
Gọi \(\left\{{}\begin{matrix}n_{Fe}=a\left(mol\right)\\n_{FeS}=b\left(mol\right)\end{matrix}\right.\left(đk:a,b>0\right)\)
TH1: S dư
Vậy toàn bộ lượng khí sinh ra là H2S
\(d_{Y\text{/}H_2}=d_{H_2S\text{/}H_2}=\dfrac{34}{2}=17\)
TH2: Fe dư
\(n_{khí}=\dfrac{2,24}{22,4}=0,1\left(mol\right)\)
Bảo toàn KL: \(m_A=m_X=7,2\left(g\right)\)
PTHH:
\(Fe+2HCl\rightarrow FeCl_2+H_2\uparrow\)
a----------------------------->a
\(FeS+2HCl\rightarrow FeCl_2+H_2S\uparrow\)
b-------------------------------->b
Ta có hệ phương trình: \(\left\{{}\begin{matrix}56a+88b=7,2\\a+b=0,1\end{matrix}\right.\)
\(\Leftrightarrow a=b=0,05\left(TM\right)\)
\(M_Y=\dfrac{0,05.\left(2+34\right)}{0,1}=18\left(g\text{/}mol\right)\\ \rightarrow d_{Y\text{/}H_2}=\dfrac{18}{2}=9\)

Đáp án B
Z+HCl → NO
=> Chứng tỏ trong Z chứa Fe(NO3)2 => Z không chứa AgNO3 => AgNO3 đã bị nhiệt phân hết.
Chất rắn không tan là Ag:
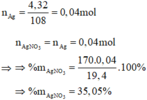
\(Fe+S\underrightarrow{t^o}FeS\)
\(FeS+2HCl\rightarrow FeCl_2+H_2S\)
\(Fe+2HCl\rightarrow FeCl_2+H_2\)
Do khí sau pư gồm H2, H2S => X chứa FeS, Fe
Fe+S-to>FeS
Fe+2HCl->FeCl2+H2
FeS+2HCl->FeCl2+H2S
=> Vẫn còn S dư