Cho 33,75 gam hỗn hợp Cl2 và Br2 có tỉ lệ số mol là 5:2 vào một dung dịch chứa NaI dư. Sản phẩm thu được chứa m gam chất X làm xanh hồ tinh bột. Tìm m?
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

- Theo bài ra \(\Rightarrow\left\{{}\begin{matrix}n_{KMnO_4}=0,1\\n_{KClO_3}=0,15\end{matrix}\right.\) ( mol )
\(2KMnO_4+16HCl\rightarrow2KCl+2MnCl_2+5Cl_2+8H_2O\)
.......0,1..........................................................0,25...........
\(KClO_3+6HCl\rightarrow KCl+3Cl_2+3H_2O\)
....0,15................................0,45....................
\(\Rightarrow n_{HCl}=0,7\left(mol\right)\)
\(6KOH+3Cl_2\rightarrow KClO_3+5KCl+3H_2O\)
Ta có : \(m=m_{KOH}+m_{Cl_2}=139,3\left(g\right)\)
Vậy ...

nHCl cần = 2nO trong oxit = 0,24 mol → nHCl đã dùng (dư 25%) = 0,3 mol.
Ghép cụm có nH2O = nO trong oxit + 2nNO
→ nNO = 0,015 mol.
∑nCl = 0,36 mol đi hết vào 53,28 gam tủa
→ về nguyên tố nAg trong tủa = 0,375 mol
Bảo toàn N có nFe(NO3)3 = (0,375 – 0,015) ÷ 3 = 0,12 mol.
→ Yêu cầu m = mFe = 0,12 × 56 = 6,72 gam.
Đáp án A

Đáp án A
Ta có nHCl cần dùng = 2∑nO trong oxit = 0,24 mol → ∑nHCl đã dùng (dư 25%) = 0,3 mol.
* Gộp cả quá trình có sơ đồ:
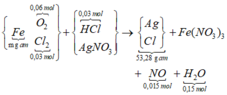
Ghép cụm NO3 bảo toàn O hoặc bảo toàn electron mở rộng ta có:
![]()
∑nCl = 0,36 mol đi hết vào 53,28 gam tủa → về mặt nguyên tố ∑nAg trong tủa = 0,375 mol.
→ Bảo toàn nguyên tố N có
![]()
Theo đó, m gam Fe ban đầu tương ứng với 0,12 mol → m = 0,12 × 56 = 6,72 gam.

Đáp án A
nHCl cần = 2nO trong oxit = 0,24 mol → nHCl đã dùng (dư 25%) = 0,3 mol.
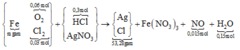
Sơ đồ phản ứng
{ Fe (m gam) + (O2 0,06 mol; Cl2 0,03 mol)} + (HCl: 0,3 mol; AgNO3)
→ (Ag-Cl : 53,28 gam) + Fe(NO3)3 + NO 0,015 mol) + H2O 0,15 mol)
Ta có nH2O = nO trong oxit + 2nNO ||→ nNO = 0,015 mol.
∑nCl = 0,36 mol đi hết vào 53,28 gam tủa → về nguyên tố nAg trong tủa = 0,375 mol
Bảo toàn N có nFe(NO3)3 = (0,375 – 0,015) ÷ 3 = 0,12 mol.
||→ m = mFe = 0,12 × 56 = 6,72 gam.
A:Vì
nHCl cần = 2nO trong oxit = 0,24 mol → nHCl đã dùng (dư 25%) = 0,3 mol.Sơ đồ phản ứng
{ Fe (m gam) + (O2 0,06 mol; Cl2 0,03 mol)} + (HCl: 0,3 mol; AgNO3)
→ (Ag-Cl : 53,28 gam) + Fe(NO3)3 + NO 0,015 mol) + H2O 0,15 mol)
Ta có nH2O = nO trong oxit + 2nNO ||→ nNO = 0,015 mol.∑nCl = 0,36 mol đi hết vào 53,28 gam tủa → về nguyên tố nAg trong tủa = 0,375 molBảo toàn N có nFe(NO3)3 = (0,375 – 0,015) ÷ 3 = 0,12 mol.||→ m = mFe = 0,12 × 56 = 6,72 gam.

Đáp án A
nHCl cần = 2nO trong oxit = 0,24 mol
→ nHCl đã dùng (dư 25%) = 0,3 mol.
Gộp quá trình:

Ghép cụm có
nH2O = nO trong oxit + 2nNO
→ nNO = 0,015 mol.
∑nCl = 0,36 mol đi hết vào 53,28 gam tủa
→ về nguyên tố nAg trong tủa = 0,375 mol
Bảo toàn N có
nFe(NO3)3 = (0,375 – 0,015) ÷ 3 = 0,12 mol.
→ Yêu cầu
m = mFe = 0,12 × 56 = 6,72 gam






\(\left\{{}\begin{matrix}71.n_{Cl_2}+160.n_{Br_2}=33,75\\\dfrac{n_{Cl_2}}{n_{Br_2}}=\dfrac{5}{2}\end{matrix}\right.\)
=> \(\left\{{}\begin{matrix}n_{Cl_2}=0,25\left(mol\right)\\n_{Br_2}=0,1\left(mol\right)\end{matrix}\right.\)
PTHH: 2NaI + Br2 --> 2NaBr + I2
0,1------------>0,1
2NaI + Cl2 --> 2NaCl + I2
0,25---------->0,25
=> \(n_{I_2}=0,35\left(mol\right)\)
=> m = 0,35.254 = 88,9 (g)
Nhanh thế, em mới làm được một nửa:v