cho hh A gồm Mg và Fe ở dạng bột.Lấy 1 lượng hh đó cho tác dụng với lượng vừa đủ dd H2So4 19,6% loãng thu được dd B trong đó nồng độ của FeSO4 là 7,17%
a) Hãy tính nồng độ của muối Mg trong dd B
b)Lấy 1,92g A cho tác dụng với 100 ml dd CuSo4 1M khi khuấy đều để các pư xảy ra hoàn toàn.Hãy tính nồng độ mol của chất tan thu được trong dd sau pư đó biết rằng thể tích thực tế k thay đổi

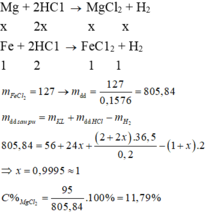
a) Gọi \(\left\{{}\begin{matrix}n_{Mg}=a\left(mol\right)\\n_{Fe}=b\left(mol\right)\end{matrix}\right.\)
PTHH: Mg + H2SO4 --> MgSO4 + H2
a--->a---------->a-------->a
Fe + H2SO4 --> FeSO4 + H2
b--->b----------->b------>b
=> \(m_{H_2SO_4}=98a+98b\left(g\right)\)
=> \(m_{ddH_2SO_4}=\dfrac{\left(98a+98b\right).100}{19,6}=500a+500b\left(g\right)\)
mdd sau pư = 24a + 56b + 500a + 500b - 2a - 2b = 522a + 554b (g)
Có: \(C\%_{FeSO_4}=\dfrac{152b}{522a+554b}.100\%=7,17\%\)
=> a = 3b
\(C\%_{MgSO_4}=\dfrac{120a}{522a+554b}.100\%=16,98\%\)
b)
Có: \(\left\{{}\begin{matrix}a=3b\\24a+56b=1,92\end{matrix}\right.\)
=> a = 0,045; b = 0,015
\(n_{CuSO_4}=0,1.1=0,1\left(mol\right)\)
PTHH: Mg + CuSO4 --> MgSO4 + Cu
0,045->0,045----->0,045
Fe + CuSO4 --> FeSO4 + Cu
0,015-->0,015----->0,015
=> \(\left\{{}\begin{matrix}n_{CuSO_4\left(dư\right)}=0,04\left(mol\right)\\n_{MgSO_4}=0,045\left(mol\right)\\n_{FeSO_4}=0,015\left(mol\right)\end{matrix}\right.\)
=> \(\left\{{}\begin{matrix}C_{M\left(CuSO_4\left(dư\right)\right)}=\dfrac{0,04}{0,1}=0,4M\\C_{M\left(MgSO_4\right)}=\dfrac{0,045}{0,1}=0,45M\\C_{M\left(FeSO_4\right)}=\dfrac{0,015}{0,1}=0,15M\end{matrix}\right.\)