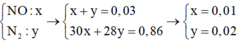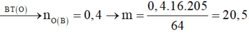1. Hòa tan hết 37,25 gam hỗn hợp B gồm những lượng bằng nhau về số mol của NaHCO3, KHCO3,
CaCl2, BaCl2 vào 130 ml nước cất, sau đó thêm tiếp 4,65 gam Na2O. Khuấy đều cho phản ứng xảy ra
hoàn toàn, sau đó lọc bỏ kết tủa, thu được dung dịch C. Tính nồng độ % của từng chất trong C. Giả
thiết các kết tủa dạng khan và các chất không bị thất thoát trong quá trình thí nghiệm.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án D
Na2O + H2O→ 2NaOH
0,04 0,08
OH-+ HCO3- → CO32-+ H2O
0,08 0,08 0,08
Ba2++ CO32- → BaCO3
0,03 0,03 0,03
Ca2++ CO32- → CaCO3
0,05 0,05 0,05
mdung dịch Z = mX+ mH2O- mkết tủa
= (0,05.111+ 0,03.100+0,05.84+0,04.62+0,03.261)+ 437,85- (0,03.197+0,05.100)
= 450 gam

Đáp án B
n(OH-) = 2n(Na2O)=0,08 ; n(HCO3-) = 0,08 ; n(Ba2+)=0,03 ; n(Ca2+) = 0,05
OH- + HCO3- → CO32- + H2O
CO32- + Ba2+ → BaCO3
CO32- + Ca2+ → CaCO3 .
Y gồm BaCO3 0,03 ; CaCO3 0,05 → m(Y) = 0,03.197 +0,05.100= 10,91
BTKL: m = 0,05.111 + 0,03.100 + 0,05.84 + 0,04.62 +0,03.261 + 437,85 - 10,91 = 450

Đáp án B
n(OH-) = 2n(Na2O)=0,08 ; n(HCO3-) = 0,08 ; n(Ba2+)=0,03 ; n(Ca2+) = 0,05
OH- + HCO3- → CO32- + H2O
CO32- + Ba2+ → BaCO3
CO32- + Ca2+ → CaCO3 .
Y gồm BaCO3 0,03 ; CaCO3 0,05 → m(Y) = 0,03.197 +0,05.100= 10,91
BTKL: m = 0,05.111 + 0,03.100 + 0,05.84 + 0,04.62 +0,03.261 + 437,85 - 10,91 = 450

n(KHSO4) = n(BaSO4) = 1,53 mol ⇒ n(Fe(NO3)3) = 0,035 mol
nT = 0,09 mol
Ta thấy 2 khí còn lại là NO và N2 với số mol lần lượt là x; y
Từ n(H2) : n(N2O) : n(NO2) = 4/9 : 1/9 : 1/9
⇒n(H2) = 0,04 mol; n(N2O) = 0,01 mol; n(NO2) = 0,01 mol
⇒mT = 30x + 28y + 0,04×2 + 0,01×44 + 0,01×46 = 1,84 g
Lại có: x + y = 0,09 − 0,04 − 0,01 − 0,01 = 0,03 mol
⇒ x = 0,01; y = 0,02 mol
Bảo toàn N: Giả sử trong muối có NH4+
n(NH4+) = 3n(Fe(NO3)3) – nN(T) = 0,025 mol
Bảo toàn H:
n(H2O) = 1/2n(KHSO4) − 2n(H2) − 4n(NH4+) = 0,675 mol
Bảo toàn O:
4n(KHSO4) + 9n(Fe(NO3)3) + nO(Y) = nH2O + nO(T) + 4nSO4
⇒ nO(Y) = 0,4 mol ⇒ mY = 0,4×16:64/205 = 20,5 g
→ Đáp án B

Đáp án B
n(KHSO4) = n(BaSO4) = 1,53 mol ⇒ n(Fe(NO3)3) = 0,035 mol
nT = 0,09 mol
Ta thấy 2 khí còn lại là NO và N2 với số mol lần lượt là x; y
Từ n(H2) : n(N2O) : n(NO2) = 4/9 : 1/9 : 1/9
⇒n(H2) = 0,04 mol; n(N2O) = 0,01 mol; n(NO2) = 0,01 mol
⇒mT = 30x + 28y + 0,04×2 + 0,01×44 + 0,01×46 = 1,84 g
Lại có: x + y = 0,09 − 0,04 − 0,01 − 0,01 = 0,03 mol
⇒ x = 0,01; y = 0,02 mol
Bảo toàn N: Giả sử trong muối có NH4+
n(NH4+) = 3n(Fe(NO3)3) – nN(T) = 0,025 mol
Bảo toàn H:
n(H2O) = 1/2n(KHSO4) − 2n(H2) − 4n(NH4+) = 0,675 mol
Bảo toàn O:
4n(KHSO4) + 9n(Fe(NO3)3) + nO(Y) = nH2O + nO(T) + 4nSO4
⇒ nO(Y) = 0,4 mol ⇒ mY = 0,4×16:64/205 = 20,5 g

gọi n là số mol mỗi chất trong hỗn hợp B là a(mol)
Ta có: 84 \(\times\)a+100\(\times\)a+111\(\times\)a+208\(\times\)a=37,728(g)
\(\Rightarrow\)a=0,075(mol)
theo đề bài:nNa2O=4,65\(\div\)(23\(\times\)2+16)=0,075(mol)
các ptpư xảy ra là:
Na2O +H2O\(\rightarrow\)2NaOH
0,075 2\(\times\)0,075 (Mol)=0,15
NaHCO3 + NaOH\(\rightarrow\)Na2CO3+ H2O
0,075 0,075 0,075 (Mol)
2KHCO3 +2NaOH \(\rightarrow\)Na2CO3 +K2CO3+2H2O
0,075 0,075 0,0375 0,0375 (Mol)
Na2CO3 + CaCl2\(\rightarrow\)CaCO3 + 2NaCl
0,075 0,075 (Mol)
Na2CO3+ BaCl2\(\rightarrow\)BaCO3 +2NaCl
0,0375 0,0375 0,0375 0,075 (Mol)
K2CO3+ BaCl2\(\rightarrow\) BaCO3 +2KCl
0,0375 0,0375 0,0375 0,075(Mol)
\(\Rightarrow\)mC=37,725+130+4,65\(-\)(0,075\(\times\)100+0,075\(\times\)197)=150,1(g)
\(\Rightarrow\)C%NaCl=\(\dfrac{\left(0,15+0,075\right)\times58,5}{150,1}\)\(\times\)100%\(\approx\)8,77%
C%KCl=\(\dfrac{0,075\times74,5}{150,1}\)\(\times\)100%\(\approx\)3,72%

Tính số mol KHSO4 = BaSO4 = 1,53 mol
→Fe(NO3)3 =0,035 mol
Hai khí còn lại là NO và N2O, số mol là x, y.
Lập hệ phương trình về tổng khối lượng và số mol tìm được x = 0,01 và y = 0,02.
Bảo toàn N tính số mol NH4+ = 0,025 mol
Bảo toàn H tính số mol H2O = 0,675 mol
Bảo toàn O:
![]()
Suy ra nO (B) = 0,4 ⟶ mB = 6,4:64 / 205 = 20,5g
Đáp án B