Cho 7,2 gam hỗn y metan và but 1 en qua dung dịch brom dư thấy có 16 gam brom tham gia pứ Tính %m của mỗi hiđrocacbon trong hỗn hợp a Đốt cháy hỗn hợp trên, viết pt pư
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


a, PT: \(C_2H_4+Br_2\rightarrow C_2H_4Br_2\)
\(C_2H_2+2Br_2\rightarrow C_2H_2Br_4\)
Giả sử: \(\left\{{}\begin{matrix}n_{C_2H_4}=x\left(mol\right)\\n_{C_2H_2}=y\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow x+y=\dfrac{1,344}{22,4}=0,06\left(1\right)\)
Ta có: \(n_{Br_2}=\dfrac{16}{160}=0,1\left(mol\right)\)
Theo PT: \(n_{Br_2}=n_{C_2H_4}+2n_{C_2H_2}=x+2y\left(mol\right)\)
⇒ x + 2y = 0,1 (2)
Từ (1) và (2) \(\Rightarrow\left\{{}\begin{matrix}x=0,02\left(mol\right)\\y=0,04\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}\%V_{C_2H_4}=\dfrac{0,02}{0,06}.100\%\approx33,33\%\\\%\text{ }V_{C_2H_2}\approx66,67\%\end{matrix}\right.\)
b, Ta có: 1/2 hỗn hợp khí gồm: 0,01 mol C2H4 và 0,02 mol C2H2.
PT: \(C_2H_4+3O_2\underrightarrow{t^o}2CO_2+2H_2O\)
\(2C_2H_2+5O_2\underrightarrow{t^o}4CO_2+2H_2O\)
Theo PT: \(n_{CO_2}=2n_{C_2H_4}+2n_{C_2H_2}=0,06\left(mol\right)\)
\(CO_2+Ca\left(OH\right)_2\rightarrow CaCO_{3\downarrow}+H_2O\)
Theo PT: \(n_{CaCO_3}=n_{CO_2}=0,06\left(mol\right)\)
\(\Rightarrow m_{cr}=m_{CaCO_3}=0,06.100=6\left(g\right)\)
Bạn tham khảo nhé!

nBr2 = 0,125 mol
Khi đốt cháy nA = 0,25 mol
mNaOH ban đầu = 36g => nNaOH = 0,9 mol
Gọi x, y lần lượt là số mol của CO2 và H2O
mdd = 180 + 44x + 18y
Vì NaOH dư do đó chỉ tạo muối trung hòa
CO2 +2NaOH → Na2CO3 + H2O
x 2x
nNaOH dư = 0,9 – 2x
có 2 , 75 % = 40 ( 0 , 9 - 2 x ) 180 + 44 x + 18 y . 100 % (1)
=> 81,21x + 0,495y = 31,05n
2,8 lít khí A tác dụng với 0,125 mol Br2
=> 5,6 lít khí A tác dụng với 0,25 mol Br2
Gọi số mol khí của CH4, C2H4 và C2H2 lần lượt là a; b; c
Ta có a + b + c = 0,25 mol
Và b + 2c = 0,25
=> a = c
=> khi đốt cháy hỗn hợp A cho nCO2 = nH2O
Thay vào (1) => x = y = 0,38 mol
Bảo toàn C, H khi đốt cháy ta có
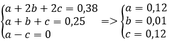
=> %VCH4 = %VC2H2 = 48%
%VC2H4 = 4%

\(n_{Br_2}=\dfrac{m_{Br_2}}{M_{Br_2}}=\dfrac{16}{160}=0,1mol\)
\(C_2H_4+Br_2\rightarrow C_2H_4Br_2\)
0,1 0,1 ( mol )
\(\%V_{C_2H_4}=\dfrac{0,1.22,4}{16,8}.100=13,33\%\)
\(\%V_{CH_4}=100\%-13,33\%=86,67\%\)

\(m_{Br_2}=80g\Rightarrow n_{Br_2}=0,5mol\)
\(C_2H_4+Br_2\rightarrow C_2H_4Br_2\)
0,5 0,5
\(n_{hh}=\dfrac{28}{22,4}=1,25mol\)
\(\Rightarrow n_{CH_4}=1,25-0,5=0,75mol\)
\(\%V_{CH_4}=\dfrac{0,75}{1,25}\cdot100\%=60\%\)
\(\%V_{C_2H_4}=100\%-60\%=40\%\)

Phương trình phản ứng:
C4H10⟶ CH4 + C3H6
C4H10⟶C2H4+C2H6
n a n k e n = n B r 2 = 25 , 6 160 = 0 , 16 ( m o l )
Gọi x là số mol butan còn dư. Số mol khí thoát ra khỏi bình bằng số mol butan ban đầu.
Khi đó: khối lượng khí đi ra khỏi bình là:
m = mbutan ban đầu - mkhí bị hấp thụ = 58.(x +0,16) - 5,32.
58 ( x + 0 , 16 ) - 5 , 32 x + 0 , 16 = 16 . 1 , 9625 ⇒ x = 0 , 04
⇒mbutan ban đầu = 58(l + x) = 11,6(g)
Đáp án D

Đáp án A
Sơ đồ phản ứng :
C 4 H 10 → crackinh CH 4 , C 3 H 6 C 2 H 6 , C 2 H 4 C 4 H 10 dư ⏟ x
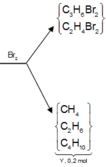
Theo giả thiết và bảo toàn khối lượng, ta có :
m C 4 H 10 = m X = m bình Br 2 tăng ⏟ 5 , 32 + m Y ⏟ 0 , 2 . 1 , 9625 . 16 = 11 , 6 n C 4 H 10 = 11 , 6 58 = 0 , 2
Đốt cháy X cũng chính là đốt cháy C4H10 ban đầu.
Áp dụng bảo toàn electron trong phản ứng đốt cháy C4H10, ta có :
4 n O 2 ⏟ ? = 26 n C 4 H 10 ⏟ 0 , 2
⇒ n O 2 = 0 , 13 mol ⇒ V O 2 = 29 , 12 lit

Đáp án B
![]()
Do vậy nếu ta hidro hóa thêm 0,4 mol H2 thì thu được 0,5 mol hỗn hợp các chất đều no
![]()
![]()
=> m = 24,3 gam
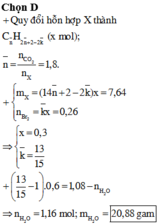
\(Metan:CH_4\\ But-1-en:CH_2=CH-CH_2-CH_3\\ n_{Br_2}=\dfrac{16}{160}=0,1\left(mol\right)\\ C_4H_8+Br_2\rightarrow C_4H_8Br_2\\ n_{C_4H_8}=n_{Br_2}=0,1\left(mol\right)\\ \%m_{C_4H_8}=\dfrac{56.0,1}{7,2}.100\approx77,778\%\\ \Rightarrow\%m_{CH_4}\approx22,222\%\\ n_{CH_4}=\dfrac{7,2-0,1.56}{16}=0,1\left(mol\right)\\ CH_4+2O_2\rightarrow\left(t^o\right)CO_2+2H_2O\\ C_4H_8+6O_2\rightarrow\left(t^o\right)4CO_2+4H_2O\)