Có một hỗn hợp bột các kim loại Al và Fe. Nếu cho a gam hỗn hợp này tác dụng với dung dịch NaOH dư, người ta thu được một thể tích khí H2 đúng bằng thể tích của 9,6 gam khí oxi (đo ở cùng điều kiện nhiệt độ và áp suất). Nếu cho a gam hỗn hợp trên tác dụng với dung dịch HCl dư, phản ứng xong thu được 8,96 lít khí H2 (đktc).
a) Viết các phương trình phản ứng xảy ra.
b) Tính a và thành phần % khối lượng mỗi kim loại trong hỗn hợp.



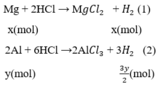
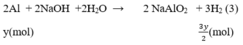
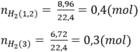
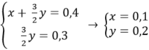

a)
2Al + 2NaOH + 2H2O --> 2NaAlO2 + 3H2
2Al + 6HCl --> 2AlCl3 + 3H2
Fe + 2HCl --> FeCl2 + H2
b)\(n_{O_2}=\dfrac{9,6}{32}=0,3\left(mol\right)\) => \(n_{H_2}=0,3\left(mol\right)\)
PTHH: 2Al + 2NaOH + 2H2O --> 2NaAlO2 + 3H2
0,2<---------------------------------------0,3
=> nAl = 0,2 (mol)
\(n_{H_2}=\dfrac{8,96}{22,4}=0,4\left(mol\right)\)
PTHH: 2Al + 6HCl --> 2AlCl3 + 3H2
0,2---------------------->0,3
Fe + 2HCl --> FeCl2 + H2
0,1<---------------------0,1
=> a = 0,2.27 + 0,1.56 = 11(g)
\(\left\{{}\begin{matrix}\%m_{Al}=\dfrac{0,2.27}{11}.100\%=49,09\%\\\%m_{Fe}=\dfrac{0,1.56}{11}.100\%=50,91\%\end{matrix}\right.\)
ban oi cho hoi fe khong tac dung voi naoh ha mik thay tren internet co bao co ma