Cho 15 gam hỗn hợp gồm 2 kim loại Cu và Fe tác dụng với dung dịch HCl dư thấy thoát ra 3,36l khí H2 ở đktc
a)Tính thành phần % khối lượng mỗi kim loại trong hỗn hợp ban đầu
b)Tính thể tích dung dịch HCl 1M đã dùng cho phản ứng trên?
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

\(Đặt:\left\{{}\begin{matrix}n_{Fe}=x\left(mol\right)\\n_{Cu}=y\left(mol\right)\end{matrix}\right.\\ Fe\rightarrow Fe^{3+}+3e\\ Cu\rightarrow Cu^{2+}+2e\\ 4H^++NO_3^-+3e\rightarrow NO+2H_2O\\ Bảotoàne:3x+2y=0,4.3\\ Tacó:56x+64y=30,4\\ \Rightarrow\left\{{}\begin{matrix}x=0,2\\y=0,3\end{matrix}\right.\\ \Rightarrow\left\{{}\begin{matrix}\%m_{Fe}=36,84\%\\\%m_{Cu}=63,16\%\end{matrix}\right.\\ n_{HNO_3}=4n_{NO}=0,4.4=1,6\left(mol\right)\\ \Rightarrow V_{HNO_3}=\dfrac{1,6}{1}=1,6\left(l\right)\\ m_{muối}=m_{Fe\left(NO_3\right)_3}+m_{Cu\left(NO_3\right)_2}=0,2.242+0,3.188=104,8\left(g\right)\)

a. PTHH:
Fe + 2HCl ---> FeCl2 + H2 (1)
Mg + 2HCl ---> MgCl2 + H2 (2)
b. Gọi x, y lần lượt là số mol của Fe và Mg
Ta có: \(n_{H_2}=\dfrac{5,6}{22,4}=0,25\left(mol\right)\)
Theo PT(1): \(n_{H_2}=n_{Fe}=x\left(mol\right)\)
Theo PT(2): \(n_{H_2}=n_{Mg}=y\left(mol\right)\)
\(\Rightarrow x+y=0,25\) (*)
Theo đề, ta lại có: 56x + 24y = 8,25 (**)
Từ (*) và (**), ta có HPT:
\(\left\{{}\begin{matrix}x+y=0,25\\56x+24y=8,25\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}x\approx0,07\\y\approx0,18\end{matrix}\right.\)
=> \(m_{Fe}=0,07.56=3,92\left(g\right)\)
=> \(\%_{m_{Fe}}=\dfrac{3,92}{8,25}.100\%=47,52\%\)
\(\%_{m_{Mg}}=100\%-47,52\%=52,48\%\)

Pt : Fe + 2HCl → FeCl2 + H2\(|\)
1 2 1 1
0,045 0,09 0,045
Số mol của khí hidro ở dktc
nH2 = \(\dfrac{V_{H2}}{22,4}=\dfrac{1,008}{22,4}=0,045\left(mol\right)\)
a) Số mol của sắt
nFe = \(\dfrac{0,045.1}{1}=0,045\left(mol\right)\)
Khối lượng của sắt
mFe = nFe . MFe
= 0,045 . 56
= 2,52 (g)
Khối lượng của bạc
mAg = 4,68 - 2,52
= 2,16 (g)
b) 0/0Fe = \(\dfrac{m_{Fe}.100}{m_{hh}}=\dfrac{2,52.100}{4,68}=\) 53,850/0
0/0Ag = \(\dfrac{m_{Ag}.100}{m_{hh}}=\dfrac{2,16.100}{4,68}=\) 46,150/0
c) Số mol của dung dịch axit clohidric
nHCl = \(\dfrac{0,045.2}{1}=0,09\left(mol\right)\)
Thể tích của dung dịch axit clohidric đã dùng
CM = \(\dfrac{n}{V}\Rightarrow V=\dfrac{n}{C_M}\) = \(\dfrac{0,09}{2}=0,045\left(M\right)\)
Chúc bạn học tốt
Mình xin lỗi bạn nhé , bạn sửa đơn vị của thể tích thành ' lít' giúp mình nhé , tại mình bấm lộn

a, Ta có: 65nZn + 27nAl = 11,9 (1)
PT: \(Zn+2HCl\rightarrow ZnCl_2+H_2\)
\(2Al+6HCl\rightarrow2AlCl_3+3H_2\)
Theo PT: \(n_{H_2}=n_{Zn}+\dfrac{3}{2}n_{Al}=\dfrac{9,916}{24,79}=0,4\left(mol\right)\left(2\right)\)
Từ (1) và (2) \(\Rightarrow\left\{{}\begin{matrix}n_{Zn}=0,1\left(mol\right)\\n_{Al}=0,2\left(mol\right)\end{matrix}\right.\)
⇒ mZn = 0,1.65 = 6,5 (g)
mAl = 0,2.27 = 5,4 (g)
b, Theo PT: nZnCl2 = nZn = 0,1 (mol)
nAlCl3 = nAl = 0,2 (mol)
⇒ m muối = 0,1.136 + 0,2.133,5 = 40,3 (g)
c, Theo PT: nHCl = 2nH2 = 0,8 (mol)
\(\Rightarrow m_{ddHCl}=\dfrac{0,8.36,5}{10\%}=292\left(g\right)\)

\(a,n_{H_2}=\dfrac{3,36}{22,4}=0,15(mol)\\ PTHH:Fe+2HCl\to FeCl_2+H_2\\ \Rightarrow n_{Fe}=n_{H_2}=0,15(mol)\\ \Rightarrow m_{Fe}=0,15.56=8,4(g)\\ \Rightarrow \%_{Fe}=\dfrac{8,4}{15}.100\%=56\%\\ \Rightarrow \%_{Cu}=100\%-56\%=44\%\\ b,n_{HCl}=2n_{H_2}=0,3(mol)\\ \Rightarrow C_{M_{HCl}}=\dfrac{0,3}{0,1}=3M\)

1.
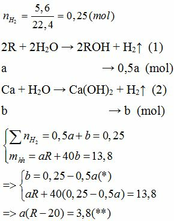
Vì b > 0, từ (*) => a < 0,25/0,5 = 0,5 thế vào (**)
=> R – 20 > 7,6
=> R > 27,6 (***)
Khi cho 8,58 gam R tác dụng với lượng dư HCl thì lượng H2 thoát ra lớn hơn 2,24 (lít)
2R + 2HCl → 2RCl + H2↑ (3)
Theo PTHH (3):
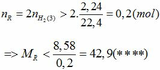
Từ (***) và (****) => 27, 6 < MR < 42,9
Vậy MR = 39 (K) thỏa mãn
2.
Ta có:
=> nKOH = nK = 0,2 (mol)
nCa(OH)2 = nCa = 0,15 (mol)
∑ nOH- = nKOH + 2nCa(OH)2 = 0,2 + 2.0,15 = 0,5 (mol)
Khi cho hỗn hợp Z ( N2, CO2) vào hỗn hợp Y chỉ có CO2 phản ứng
CO2 + OH- → HCO3- (3)
CO2 + 2OH- → CO32- + H2O (4)
CO32- + Ca2+ → CaCO3↓ (5)
nCaCO3 = 8,5/100 = 0,085 (mol) => nCO32-(5) = nCaCO3 = 0,085 (mol)
Ta thấy nCaCO3 < nCa2+ => phương trình (5) Ca2+ dư, CO32- phản ứng hết
TH1: CO2 tác dụng với OH- chỉ xảy ra phản ứng (4)
Theo (4) => nCO2 = nCO32-(4) = nCaCO3 = 0,085 (mol)
=> VCO2(đktc) = 0,085.22,4 = 1,904 (lít)
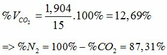
TH2: CO2 tác dụng với OH- xảy ra cả phương trình (3) và (4)
Theo (4): nCO2 = nCO32- = 0,085 (mol)
nOH- (4) = 2nCO32- = 2. 0,085 = 0,17 (mol)
=> nOH- (3)= ∑ nOH- - nOH-(4) = 0,5 – 0,17 = 0,33 (mol)
Theo PTHH (3): nCO2(3) = nOH- = 0,33 (mol)
=> ∑ nCO2(3+4) = 0,085 + 0,33 = 0,415 (mol)
=> VCO2 (ĐKTC) = 0,415.22,4 = 9,296 (lít)
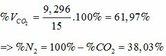
Ta có nH2 = 3,36/22,4 = 0,15 mol
Fe +2 HCl -> FeCl2 + H2
0,15. 0,3 <-. 0,15. ( Mol)
=> mFe = 0,15 × 56 = 8,4g
=> %Fe = 8,4/15×100% = 56%
=> %Cu = 100% - 56% = 44%
=>VHCl =1\0,3=10\3 l
PTHH : 2Fe + 6HCl --> 2FeCl3 + 3H2 (1)
nH2 = \(\dfrac{3.36}{22.4}=0.15\left(mol\right)\)
Từ (1) -> nFe = \(\dfrac{2}{3}n_{H_2}=0.1\left(mol\right)\)
-> mFe = n.M = 0,1 . 56 = 5.6 (g) => %mFe = \(\dfrac{5.6}{15}x100\%\approx37.3\%\)
-> %mCu = 100% - 37.3% = 62.7 %