Cho 200 gam dung dịch Na2CO3, tác dụng với 200 gam dung dịch HCl thu được 2,24 lít khí (đktc) dung dịch dung dịch thu được sau phản ứng c). Dẫn toàn bộ khi sinh ra qua dung dịch nước vôi trong Ca(OH)2 dư ta thu được bao nhiêu kết tủa biết hiệu suất của phản ứng là 90%.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Chọn đáp án A
Chú ý tỉ lệ dung dich X trong mỗi phản ứng
Gọi số mol ion Na+, NH4+, CO32- và SO42- trong 100ml lần lượt a, b, c, d mol
Khi cho X tác dụng với HCl chỉ có CO32- tham gia phản ứng → c = 0,1 mol
Khi cho X tác dụng với BaCl2 thu được BaCO3 và BaSO4 → 0,1.197 + d.233= 43 → d = 0,1 mol
Khi cho X tác dụng lượng dư dung dịch NaOH chỉ có NH4+ tham gia phản ứng → b = 0,2 mol
Bảo toàn điện tích trong dung dịch X → a = 2. 0,1 + 2. 0,1 -0,2 = 0,2 mol
Vậy trong 300ml dung dịch X gồm 0,6 mol Na+, 0,6 mol NH4+, 0,3 mol CO32- và 0,3 mol SO42-
→ m = 0,6.23 + 0,6. 18 + 0,3. 60 + 0,3. 96= 71,4 gam.
Đáp án A.

Chọn đáp án A
Chú ý tỉ lệ dung dich X trong mỗi phản ứng
Gọi số mol ion Na+, NH4+, CO32- và SO42- trong 100ml lần lượt a, b, c, d mol
Khi cho X tác dụng với HCl chỉ có CO32- tham gia phản ứng → c = 0,1 mol
Khi cho X tác dụng với BaCl2 thu được BaCO3 và BaSO4 → 0,1.197 + d.233= 43 → d = 0,1 mol
Khi cho X tác dụng lượng dư dung dịch NaOH chỉ có NH4+ tham gia phản ứng → b = 0,2 mol
Bảo toàn điện tích trong dung dịch X → a = 2. 0,1 + 2. 0,1 -0,2 = 0,2 mol
Vậy trong 300ml dung dịch X gồm 0,6 mol Na+, 0,6 mol NH4+, 0,3 mol CO32- và 0,3 mol SO42-
→ m = 0,6.23 + 0,6. 18 + 0,3. 60 + 0,3. 96= 71,4 gam.
Đáp án A.

Phần 2: nCO32- phản ứng = u và nHCO3- phản ứng = v
nCO2 = u + v = 0,06
nHCl = 2u + v = 0,075
—> u = 0,015 và v = 0,045
—> Phần 1: nCO32- = ku và nHCO3- = kv
—> nCaCO3 = ku + kv = 0,1
—> k = 5/3
Vậy X chứa nCO32- = 2ku = 0,05 và nHCO3- = 2kv = 0,15
Bảo toàn điện tích —> nNa+ = x + 2y = 0,05.2 + 0,15
Bảo toàn C —> 0,1 + y = 0,05 + 0,15
—> x = 0,05 và y = 0,1
nhớ tick nếu thấy đúng nha

Theo gt ta có: $n_{CO_2}=0,1(mol);n_{CaCO_3}=0,1(mol);n_{HCl}=0,075(mol);n_{CO_2/(2)}=0,06(mol)$
Bảo toàn C ta có: $y=0,1$
$CO_3^{2-}+2H^+\rightarrow CO_2+H_2O$
$HCO_3^-+H^+\rightarrow CO_2+H_2O$
Gọi số mol $CO_3^{2-}$ và $HCO_3^-$ phản ứng lần lượt là a;b
Ta có: $2a+b=0,075;a+b=0,06$
Giải hệ ta được $a=0,015;b=0,045$
Suy ra $n_{CO_3^{2-}}=0,05(mol);n_{HCO_3}=0,15(mol)$
Bảo toàn Na ta có: $x=0,05$

Chọn A
Gọi số mol Na + , NH 4 + , CO 3 2 - và SO 4 2 - trong 100ml dung dịch X lần lượt là x, y, z và t.
Bảo toàn điện tích có: x + y – 2z – 2t = 0 (1)
Cho 100ml X tác dụng với HCl dư:
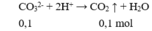
→ z = 0,1 (2)
Cho 100ml X tác dụng với BaCl2 dư:
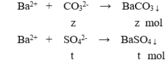
m↓ = 43 (gam) → 197z + 233t = 43 (3)
Cho 100 ml X tác dụng với NaOH
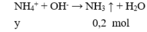
→ y = 0,2 (4)
Từ (1); (2); (3); (4) có x = y = 0,2; z = 0,1; t = 0,1.
Tổng khối lượng muối trong 300ml dung dịch là:
m = 3. (0,2.23 + 0,2.18 + 0,1.60 + 0,1.96) = 71,4 gam.
