Câu 1: Ngâm một đinh sắt sạch trong dung dịch đồng (II) sunfat. Nêu hiện tượng quan sát được? Viết PTHH xảy ra ( nếu có)
Câu 2: Nhỏ vài giọt dung dịch bạc nitrat vào ống nghiệm đựng dd Natri clorua. Nêu hiện tượng quan sát được? Viết PTHH xảy ra (nếu có).
Câu 3: Dẫn từ từ 6,72 lít khí CO2 ( ở đktc) vào dung dịch nước vôi trong dư.
a) Viết phương trình hóa học của phản ứng xảy ra.
b) Tính số gam kết tủa thu được sau phản ứng.
Câu 4: Nêu và giải thích hiện tượng xảy ra trong các trường hợp sau:
a) Nhỏ vài giọt dung dịch Ba(OH)2 vào ống nghiệm chứa dung dịch H2SO4.
b) Nhỏ từ từ đến dư dung dịch NaOH vào ống nghiệm chứa dung dịch HCl có sẵn mẩu quỳ tím.
Câu 5: Cho các chất sau: Zn(OH)2, NaOH, Fe(OH)3, KOH, Ba(OH)2.
a) Những chất nào có phản ứng với khí CO2?
b) Những chất nào bị phân hủy bởi nhiệt?
c) Những chất nào vừa có phản ứng với dung dịch HCl, vừa phản ứng với dung dịch NaOH?
Câu 6: Cho những oxit sau: BaO, Fe2O3, N2O5, SO2. Những oxit nào tác dụng với: a. Nước b. Axit clohiđric c. Natri hiroxit
Viết phương trình phản ứng xảy ra
Câu 7: Có 3 ống nghiệm, mỗi ống đựng một dung dịch các chất sau: Na2SO4 ; HCl; NaNO3. Hãy nhận biết chúng bằng phương pháp hóa học. Viết các PTHH xảy ra (nếu có).
Câu 8: Bằng phương pháp hóa học, hãy phân biệt các lọ đựng các dung dịch sau: KOH; Ba(OH)2 ; K2SO4; H2SO4; HCl. Viết các phương trình phản ứng xảy ra (nếu có).



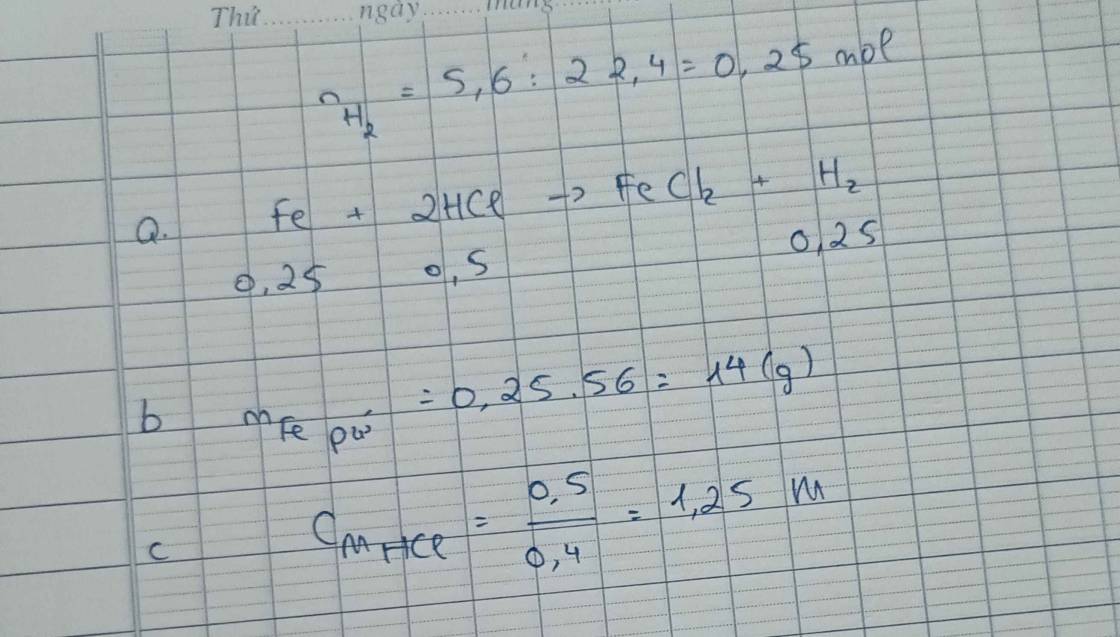
1. a) Quan sát màu sắc của các dung dịch ta thấy CuSO4 có màu xanh lam
AgNO3, NaCl không màu
Cho quỳ tím vào 2 dung dịch không màu trên
+ Quỳ hóa đỏ: AgNO3
+ Quỳ không đổi màu: NaCl
b) Cho quỳ tím vào các mẫu thử
+ Quỳ hóa đỏ: HCl
+ Quỳ hóa xanh: NaOH
+ Quỳ không đổi màu: NaNO3, NaCl
Cho AgNO3 vào 2 mẫu thử làm quỳ không đổi màu
+ Kết tủa: NaCl
\(NaCl+AgNO_3\rightarrow NaNO_3+AgCl\downarrow\)
+ Không hiện tượng: NaNO3
c) Cho quỳ tím vào từng mẫu thử
+ Quỳ hóa xanh: KOH, K2CO3
+ Quỳ không đổi màu: K2SO4, KNO3
Cho dung dịch HCl vào 2 mẫu làm quỳ hóa xanh
+ Có khí thoát ra: K2CO3
\(K_2CO_3+2HCl\rightarrow2KCl+CO_2+H_2O\)
+ Không hiện tượng: KOH
\(KOH+HCl\rightarrow KCl+H_2O\)
Cho dung dịch BaCl2 vào 2 mẫu không làm quỳ đổi màu
+ Kết tủa: K2SO4
\(BaCl_2+K_2SO_4\rightarrow BaSO_4+2KCl\)
+ Không hiện tượng: KNO3
2)\(a.Fe+2HCl\rightarrow FeCl_2+H_2\\ n_{Fe}=n_{H_2}=0,45\left(mol\right)\\ \Rightarrow m_{Fe}=0,45.56=25,2\left(g\right)\\ b.n_{HCl}=2n_{H_2}=0,9\left(mol\right)\\ \Rightarrow CM_{HCl}=\dfrac{0,9}{0,15}=6M\)