Cho 20g hỗn hợp kim loại gồm Magie và Bạc tác dụng hoàn toàn với 200ml dung dịch CuSo4 1M. Tính khối lượng mỗi chất trong hỗn hợp kim loại ban đầu.
giúp với ạ
![]()
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

\(n_{HCl}=1.0,2=0,2(mol)\\ PTHH:Mg+2HCl\to MgCl_2+H_2\\ \Rightarrow n_{Mg}=\dfrac{1}{2}n_{HCl}=0,1(mol)\\ \Rightarrow m_{Mg}=0,1.24=2,4(g)\\ \Rightarrow m_{Cu}=10-2,4=7,6(g)\)

n C u S O 4 = 0,525.0,2 = 0,105 m o l
Vì thu được kết tủa là 2 kim loại nên Fe còn dư.
Suy ra, kết tủa là Fe dư và C u , C u S O 4 phản ứng hết.
Gọi a, b, c là số mol của Al phản ứng, Fe phản ứng và Fe dư.
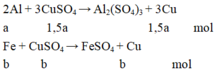
Từ phương trình phản ứng và dữ kiện đề bài cho, ta lập được hệ phương trình:
3 2 a + b = n C u S O 4 a .27 + b .56 + c .56 = m K L 3 2 a .64 + b .64 + c .56 = m k e t t u a ⇔ 3 2 a + b = 0,105 27 a + 56 b + 56 c = 4,15 96 a + 64 b + 56 c = 7,84
⇔ a = 0,05 b = 0,03 c = 0,02
Vậy n A l = 0 , 05 m o l ; n F e b đ = b + c = 0 , 05 m o l .
Đáp án C

Gọi x,y là số mol của CuO,Fe2O3
Ta có: 80x+160y=20 (1)
nHCl= 3,5.0.,2 = 0,7
PTHH:2HCl + CuO → CuCl2 + H2O
Mol: 2x x
PTHH:6HCl + Fe2O3 → 2FeCl3 + 3H2O
Mol: 6y y
⇒ 2x+6y=0,7 (2)
Từ (1)(2)⇒ x=0,05;y=0,1
\(\Rightarrow m_{CuO}=0,05.80=4\left(g\right);m_{Fe_2O_3}=0,1.160=16\left(g\right)\)

\(n_{H_2}=\dfrac{2,24}{22,4}=0,1(mol)\\ a,PTHH:Fe+2HCl\to FeCl_2+H_2\\ b,n_{Fe}=n_{H_2}=0,1(mol)\\ \Rightarrow m_{Fe}=0,1.56=5,6(g)\\ \Rightarrow \%_{Fe}=\dfrac{5,6}{12}.100\%=46,67\%\\ \Rightarrow \%_{Cu}=100\%-46,67\%=53,33\%\\ c,n_{HCl}=2n_{H_2}=0,2(mol)\\ \Rightarrow C_{M_{HCl}}=\dfrac{0,2}{0,2}=1M\)

a/ PTHH: Mg + 2HCl ===> MgCl2 + H2
x 2x x x
Fe + 2HCl ===> FeCl2 + H2
y 2y y y
Gọi số mol Mg, Fe lần lượt là x, y
Lập các số mol theo phương trình
nH2 = 8,96 / 22,4 = 0,4 mol
Theo đề ra, ta có hệ phương trình:
\(\begin{cases}24x+56y=12,8\\x+y=0,4\end{cases}\)=>\(\begin{cases}x=0,3\\y=0,1\end{cases}\)
=> mMg = 0,3 x 24 = 7,2 gam
mFe = 0,1 x 56 = 5,6 gam
b/ \(\sum nHCl\) = 0,8 mol
=> VHCl = 0,8 / 2 = 0,4 lít = 400ml
c/ PTHH: MgCl2 + 2NaOH ===> Mg(OH)2 + 2NaCl
0,3 0,6 0,3
FeCl2 + 2NaOH ===> Fe(OH)2 + 2NaCl
0,1 0,2 0,1
=> \(\sum m\downarrow\) = 0,3 x ( 24 + 16 x 2 + 2) + 0,1 x ( 56 + 16 x 2 + 2) = 26,4 gam

\(n_{H_2}=\dfrac{2,24}{22,4}=0,1\left(mol\right)\)
PT: \(Fe+2HCl\rightarrow FeCl_2+H_2\)
Theo PT: \(n_{Fe}=n_{H_2}=0,1\left(mol\right)\)
\(\Rightarrow m_{Fe}=0,1.56=5,6\left(g\right)\)
\(\Rightarrow m_{Cu}=12-5,6=6,4\left(g\right)\)
Nhận thấy rừng `Cu` không tác dụng với `HCl` nên toàn bộ lượng `H_2` là do `Fe`
\(n_{H_2\left(dktc\right)}=\dfrac{V}{22,4}=\dfrac{2,24}{22,4}=0,1\left(mol\right)\\ PTHH:Fe+2HCl->FeCl_2+H_2\)
tỉ lệ 1 : 2 : 1 : 1
n(mol) 0,1<------------------------------0,1
\(m_{Fe}=n\cdot M=0,1\cdot56=5,6\left(g\right)\\ m_{Cu}=12-5,6=6,4\left(g\right)\)
\(n_{CuSO_4}=0,2.1=0,2(mol)\\ PTHH:Mg+CuSO_4\to MgSO_4+Cu\\ \Rightarrow n_{Mg}=0,2(mol)\\ \Rightarrow m_{Mg}=0,2.24=4,8(g)\\ \Rightarrow m_{Ag}=m_{hh}-m_{Mg}=20-4,8=15,2(g)\)
Cảm ơn