trong một bình kín dung tích ko đổi chứa hỗn hợp hơi chất A (CxHyO) với O2 vừa đủ để đốt cháy hợp chất A ở 136,5 độ C và 1 atm. Sau khi đốt cháy, đưa bình về nhiệt độ ban đầu, thì áp suất trong bình là 1,2 atm. Mặt khác, khi đốt cháy 0,03 mol A lượng CO2 sinh ra được cho vô 400ml dd Ba(OH)2 0,15M thấy có hiện tượng hòa tan kết tủa, nhưng nếu cho vô 800ml dd Ba(OH)2 nói trên thì thấy Ba(OH)2 dư. Tìm ctpt A
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án D
phản ứng cháy
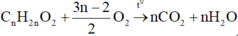
Với bài này, thông thường các bạn thường nghĩ tới tính được tổng số mol khí trước và sau phản ứng, tuy nhiên với dữ kiện giả thiết không đủ cho ta tính các số liệu trên trên.
Mà với tổng số mol khí trước phản ứng bất kì, trong điều kiện bình kín không thay đổi và nhiệt độ trước và sau phản ứng như nhau thì ta luôn có:
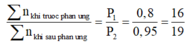
Do đó để cho đơn giản, ta chọn 1 mol CnH2nO2 ban đầu, khi đó:
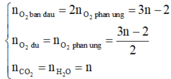
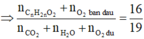
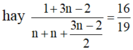
⇔ n=3
Vậy X là C3H6O2.

Chọn đáp án B
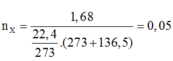
Nhận xét: tất cả các chất trong X đều có công thức dạng C H 2 n O 2
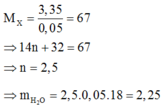

Đáp án B
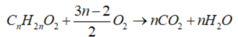
→ n t r = 2 x + 2 x 3 n - 2
n s = 2 x - x + 2 . 2 n x 3 n - 2
n t r n s = p t r p s = 16 19
⇔ 2 x + 2 x 3 n - 2 x + 4 n x 3 n - 2 = 16 19 ⇔ n = 3
⇒ X l à C 3 H 6 O 2

Đáp án : A
CnH2nO2 + (1,5n – 1) O2 -> nCO2 + nH2O
1 mol -> (1,5n – 1) -> n -> n
Xét 1 mol X
=> n O 2 = 2(1,5n – 1) = (3n – 2) (mol)
=> sau phản ứng còn (1,5n – 1) mol O2
nđầu = (1 + 3n – 2) = 3n – 1
nsau = 1,5n – 1 + n + n = 3,5n – 1
Vì PV = nRT. Do T , V không đổi
=> Pt/nt = Ps/n
=> 1,3.(3n – 1) = 1,1.(3,5n – 1)
=> n = 4
=>C4H8O2
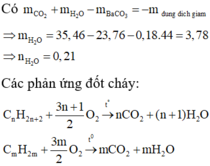
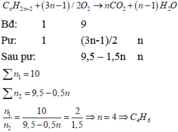
Trong một bình kín dung tích không đổi chứa hỗn hợp hơi chất X (CxHyO) với O2 vừa đủ để đốt cháy hợp chất X ở 136,5oC và?