Phản ứng hoá học xảy ra trong trường hợp nào dưới đây không thuộc loại phản ứng nhiệt nhôm?
A. Al tác dụng với Fe3O4 nung nóng
B. Al tác dụng với axit H2SO4 đặc, nóng
C. Al tác dụng với CuO nung nóng
D. Al tác dụng với Fe2O3 nung nóng
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Phản ứng nhiệt nhôm là cho nhôm khử các oxit của kim loại => Phản ứng hoá học thuộc loại phản ứng nhiệt nhôm là 1, 4, 5.
Đáp án cần chọn là: C


Số mol S O 2 = 1,5x + 0,03 = 0,06375→ x = 0,0225 mol
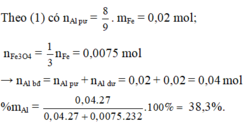
⇒ Chọn C.

Đáp án C
8 Al + 3 Fe 3 O 4 → t o 4 Al 2 O 3 + 9 Fe
Vì phản ứng xảy ra hoàn toàn và hòa tan A vào dung dịch NaOH thu được khí nên A gồm Fe, A12O3 và Al dư.


Chọn C.
(1) CaCO3 → t o CaO + CO2
(2) 2AgNO3 + H2O → đpdd 2Ag + 2HNO3 + 1/2O2
(3) 2Al + 3CuO → t o Al2O3 + 3Cu
(4) Cu + 2Fe(NO3)3 ® Cu(NO3)2 + 2Fe(NO3)2
(5) FeCl2 + 3AgNO3 ® Fe(NO3)3 + 2AgCl + Ag
(6) Không xảy ra phản ứng

2 A l + 3 H 2 S O 4 → A l 2 S O 4 3 + 3 H 2
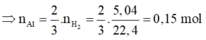
⇒ m F e 2 O 3 (bđ) = 20,05 - 0,15.27 = 16g
⇒ n F e 2 O 3 (bđ) = 16/160 = 0,1 mol
2Al + F e 2 O 3 → A l 2 O 3 + 2Fe
Bđ: 015 0,1
Pư: 0,15 0,065
Dư: 0 0,025
⇒ m F e 2 O 3 (dư) = 0,025.160=4g
⇒ Chọn A.

a) nAl=0,2(mol)
PTHH: 2 Al + 6 HCl -> 2 AlCl3 + 3 H2
H2 + CuO -to-> Cu + H2O
nAlCl3= nAl= 0,2(mol)
=> mAlCl3= 133,5. 0,2= 26,7(g)
b) nCu= nH2= 3/2 . 0,2=0,3(mol)
=> mCu= 0,3.64=19,2(g)
(Qua phản ứng nghe kì á, chắc tạo thành chứ ha)
<3

Sau phản ứng có Al dư do phản ứng với NaOH tạo H2
=> nAl dư = 2/3 .nH2 = 0,02 mol
Sau phản ứng có Al và Al2O3 + NaOH => NaAlO2
Bảo toàn Al ta có :
2nAl2O3 sau nung= nAl dư + 2nAl2O3 => nAl2O3 = 0,04 mol
=>nAl ban đầu = 0,1 mol
Do các phản ứng hàn toàn , mà khi nhiệt nhôm Al dư => oxit sắt hết
=>D chỉ có Fe
=>Bảo toàn e : 3nFe = 2nSO2 => nFe = 0,08 mol
Bảo toàn khối lượng : mA = mB = mFe + mAl + mAl2O3 = 9,1g
=>%mAl(A) = 29,67% gần nhất với giá trị 24%
=>A

Chọn B
Xét từng thí nghiệm:
(1) SiO2 + 4HF → SiF4 + 2H2O
2 2 N H 3 + 3 C u O → N 2 + 3 C u + 3 H 2 O
3
K
2
C
r
2
O
7
+
14
H
C
l
→
2
K
C
l
+
2
C
r
C
l
3
+
3
C
l
2
+
7
H
2
O
4
S
i
+
2
N
a
O
H
+
H
2
O
→
N
a
2
S
i
O
3
+
2
H
2
5
N
H
4
C
l
+
N
a
N
O
2
→
N
a
C
l
+
N
2
+
2
H
2
O
6 N a N O 3 + F e C O 3 1 : 2 → N a N O 3 → N a N O 2 + 1 2 O 2
Vì tỉ lệ 1:2 nên
2 F e C O 3 + 1 2 O 2 → F e 2 O 3 + 2 C O 2
(7) Ag+ + Fe2+ → Ag + Fe3+
Ag+ + Cl- → AgCl
(8) K2O + H2O → 2KOH
KOH + Al + H2O → NaAlO2 + 3/2H2
Các thí nghiệm có đơn chức tạo thành:
(2), (3) (4) (5) (7) (8).